1 .
(1)I.下列元素或化合物的性质变化顺序正确的是_______________
A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
II.黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
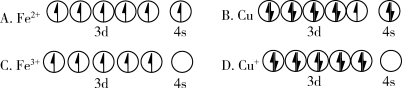
(2)CuFeS2中存在的化学键类型是________________ 。下列基态原子或离子的价层电子排布图正确的_____________ 。
(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是______ ,中心原子杂化类型为__________ ,属于_______ (填“极性”或“非极性”)分子。
②X的沸点比水低的主要原因是____________________ 。
(4)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为_____ ,共价键的类型有_________ 。
(5)四方晶系CuFeS2晶胞结构如图所示。

①Cu+的配位数为__________ ,S2-的配位数为____________ 。
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏伽德罗常数的值,CuFeS2晶体的密度是________ g•cm-3(列出计算式)。
(1)I.下列元素或化合物的性质变化顺序正确的是_______________
A.第一电离能:Cl>S>P>Si B.共价键的极性:HF>HCI>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
II.黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(2)CuFeS2中存在的化学键类型是

(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是
②X的沸点比水低的主要原因是
(4)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为
(5)四方晶系CuFeS2晶胞结构如图所示。

①Cu+的配位数为
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏伽德罗常数的值,CuFeS2晶体的密度是
您最近一年使用:0次
2018-11-28更新
|
3021次组卷
|
3卷引用:2018年普通高等学校招生全国统一考试化学(海南卷)



