名校
解题方法
1 . 完成下列问题
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
(3)关于新制饱和氯水,下列叙述正确的是_______
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2O
ii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是___________
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)_________
③配平反应i的化学方程式_________ 。
④标出反应ii中电子转移的方向和数目_________ 。
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾___________ 吨。
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
| A.钝化 | B.漂白 | C.固氮 | D.燃烧 |
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
| A.工业合成氨的过程是固氮的过程 |
| B.自然界中,氨是动物体特别是蛋白质腐败后的产物 |
| C.为防止粮食、罐头、水果等食品腐烂,常用氮气作保护气 |
| D.在雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收 |
(3)关于新制饱和氯水,下列叙述正确的是_______
| A.加入适量NaOH,溶液黄绿色褪去,说明氯水中含有Cl2分子 |
| B.加入少量NaCl粉末,溶液漂白性增强 |
| C.加入少量的碳酸钠粉末,pH增大,溶液漂白性一定减弱 |
| D.光照过程中,有气泡冒出,溶液的导电性减弱 |
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
| A.向含足量NaOH的Na2S溶液中加入Na2SO3 |
| B.常温下,向试管中加入1mL浓硫酸和一小块铜片 |
| C.将0.5g硫粉和1.0g铁粉均匀混合,在石棉网上用红热玻璃棒触及粉末一端至粉末红热 |
| D.向Na2SO3固体中加入70%的浓硫酸制备SO2 |
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

| A.O2氧化HBr生成Br2的总反应为:O2+4HBr=2Br2+2H2O |
| B.中间体HOOBr和HOBr中Br的化合价相同 |
| C.发生步骤②时,断裂的化学键既有极性键又有非极性键 |
| D.步骤③中,每生成1molBr2转移2mol电子 |
(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3
 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2Oii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)
③配平反应i的化学方程式
④标出反应ii中电子转移的方向和数目
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾
您最近一年使用:0次
2 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.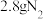 中含有质子数目为 中含有质子数目为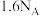 |
B.标准状况下,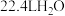 中含有共价键数目为 中含有共价键数目为 |
C.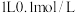 氢氧化钠溶液中含有钠离子数目为 氢氧化钠溶液中含有钠离子数目为 |
D. 与足量水充分反应,转移电子数目为 与足量水充分反应,转移电子数目为 |
您最近一年使用:0次
3 . 下列各组物质中,化学键类型完全相同的是
| A.HI和NaI | B.K2O2和NaOH |
| C.NaCl和CO2 | D.H2O和CCl4 |
您最近一年使用:0次
4 . 在抗击新冠病毒中“84消毒液(有效成分是NaClO)”发挥了重要作用。工业上,制备“84消毒液”的原理为:NaCl+H2O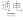 NaClO+H2↑。下列说法不正确的是
NaClO+H2↑。下列说法不正确的是
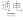 NaClO+H2↑。下列说法不正确的是
NaClO+H2↑。下列说法不正确的是| A.该反应每转移4mol电子生成149g的NaClO |
| B.NaClO的消毒原理利用了其强氧化性 |
C.NaCl的电子式为: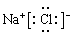 |
| D.上述制备消毒液的反应过程中只有离子键的断裂和形成 |
您最近一年使用:0次
解题方法
5 . 下列物质中,只有含极性共价键的是
| A.单质碘 | B.氢氧化钠 | C.水 | D.氯化铵 |
您最近一年使用:0次
6 . 一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大,且总和为24。下列有关叙述不正确的是
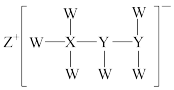

| A.该化合物中,W、X、Y之间不存在离子键 |
| B.X的氧化物的水化物一定为强酸 |
| C.原子半径:Y<X |
| D.Z的单质与冷水能反应 |
您最近一年使用:0次
解题方法
7 . 工业上将氯气通入冷的石灰乳中,可以制得漂白粉。下列与制漂白粉相关的物质中,只含有离子键的是
A. | B. | C. | D. |
您最近一年使用:0次
解题方法
8 . 下列有关碳及其化合物的说法中正确的是
A. 、 、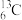 、 、 互为同素异形体 互为同素异形体 |
B.CO与 属于酸性氧化物 属于酸性氧化物 |
C. 与 与 均属于离子化合物 均属于离子化合物 |
| D.通过改变碳原子排列方式可实现石墨转化为金刚石 |
您最近一年使用:0次
9 . 化学与生活密切相关。下列说法错误的是
| A.H2O2是一种绿色增氧剂,H2O2属于共价化合物 |
| B.硬铝常用于制造飞机的外壳,原因是硬铝的密度小、强度高 |
| C.豆浆是胶体,可以产生丁达尔效应 |
| D.Na2CO3俗名小苏打,可用于治疗胃酸过多 |
您最近一年使用:0次
名校
解题方法
10 . 下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是
| A.2NaBr+Cl2=2NaCl+Br2 | B.2NaOH+CO2=Na2CO3+H2O |
| C.2Na2O2+2H2O=4NaOH+O2↑ | D.H2S+Cl2=S↓+2HCl |
您最近一年使用:0次



