1 . 下列说法中不正确的是
A. 晶体溶于水时,离子键被破坏,共价键不受影响 晶体溶于水时,离子键被破坏,共价键不受影响 |
| B.“天宫课堂”中过饱和乙酸钠溶液析晶放热与形成新的化学键有关 |
| C.将熔融状态下的HCl和NaCl进行导电性实验可证明HCl由共价键形成而NaCl由离子键形成 |
| D.H元素与其他元素化合可能形成共价化合物也可能形成离子化合物 |
您最近一年使用:0次
2023-04-27更新
|
191次组卷
|
2卷引用:山东省德州市2022-2023学年高一下学期4月期中考试化学试题
名校
2 . 1869年门捷列夫提出元素周期表,根据元素周期表和周期律,回答问题。
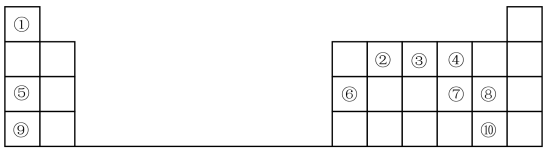
(1)元素⑦在周期表中的位置_______ 。
(2)元素①和⑤形成的化合物中化学键类型是_______ 。
(3)在①~⑧元素中,原子半径最大的是_______ (填元素名称);其某种氧化物可用于潜水艇中的供氧剂,该氧化物中阴离子与阳离子个数比为_______ 。
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是_______ (用离子符号表示),元素⑨的最高价氧化物对应水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(5)元素的非金属性⑩_______ ⑧(填“>”或“<”);下列事实不能证明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的氢化物的还原性比元素⑩的弱
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
E.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
(6)⑤的最高价氧化物对应的水化物的电子式为_______ ,用电子式表示氯化钠的形成过程_______ 。

(1)元素⑦在周期表中的位置
(2)元素①和⑤形成的化合物中化学键类型是
(3)在①~⑧元素中,原子半径最大的是
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是
(5)元素的非金属性⑩
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的氢化物的还原性比元素⑩的弱
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
E.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
(6)⑤的最高价氧化物对应的水化物的电子式为
您最近一年使用:0次
3 . 几种主族元素在周期表中的位置如图
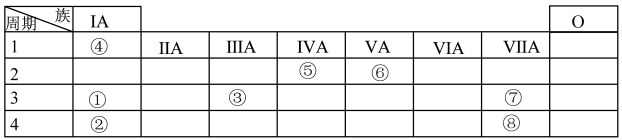
根据图表回答下列问题:
(1)⑥元素的氢化物的电子式是_______
(2)①③⑦三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素在周期表中的位置是_______ ,其最高价氧化物对应的水化物所含的化学键有_______
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_______ (填化学式);①与③最高价氧化物对应水化物反应的离子方程式为_______ 。
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是_______(填字母)。

根据图表回答下列问题:
(1)⑥元素的氢化物的电子式是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素在周期表中的位置是
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是_______(填字母)。
| A.⑦的氢化物比⑧的氢化物稳定 |
| B.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性 |
| C.⑦的单质能将⑧从其钠盐溶液中置换出来 |
| D.⑦的氢化物酸性比⑧的氢化物酸性弱 |
您最近一年使用:0次
4 . 短周期主族元素W、X、Y、Z、M的原子序数依次增大,W的单质是空气的主要成分,X与Z的原子序数相差8,Y的原子半径是所有短周期主族元素中最大的,X与Y可形成化合物 。请回答下列问题:
。请回答下列问题:
(1)X、M的元素符号分别为_______ 、_______ 。W在元素周期表中的位置是_______ 。
(2)W、X简单氢化物的热稳定性由强到弱的顺序为_______ (用化学式表示);上述元素形成的含氧酸中酸性最强的为_______ (填化学式)。
(3)元素W与M能形成化合物Q,Q的结构式为_______ (用元素符号表示),其含有的化学键类型为_______ 。
(4)用电子式表示 的形成过程:
的形成过程:_______ 。
(5)化合物 与M的单质反应能证明Z、M的非金属性强弱,则该反应的化学方程式为
与M的单质反应能证明Z、M的非金属性强弱,则该反应的化学方程式为_______ 。
 。请回答下列问题:
。请回答下列问题:(1)X、M的元素符号分别为
(2)W、X简单氢化物的热稳定性由强到弱的顺序为
(3)元素W与M能形成化合物Q,Q的结构式为
(4)用电子式表示
 的形成过程:
的形成过程:(5)化合物
 与M的单质反应能证明Z、M的非金属性强弱,则该反应的化学方程式为
与M的单质反应能证明Z、M的非金属性强弱,则该反应的化学方程式为
您最近一年使用:0次
名校
5 . 回答下列问题
(1)请用下列10种物质的序号填空:
①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2
其中既含离子键又含非极性键的是_______ ;既含离子键又含极性键的是_______ 。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为_______ ;若XY2为共价化合物时(已知硫磺易溶于其中),其结构式为_______ 。
(3)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190 ℃,但在180 ℃就开始升华。据此判断,氯化铝是_______ (填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据是_______ 。
(4)现有a~g 7种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:
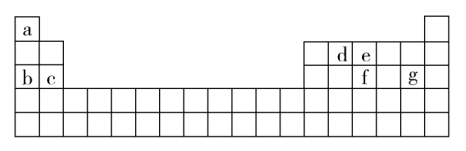
①元素的原子间反应最容易形成离子键的是_______ (填选项,下同),容易形成共价键的是_______ 。
A.c和f B.b和g C.d和g D.b和e
②写出a~g 7种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式_______ 。
(5)a与e能形成氢化物的空间构型为_______ ,其所含化学键类型为_______ ,将其通入到炽热的黑色氧化铜粉末中,出现了红色固体,其他产物对环境友好,请写出相关方程:_______ 。
(1)请用下列10种物质的序号填空:
①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2
其中既含离子键又含非极性键的是
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为
(3)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190 ℃,但在180 ℃就开始升华。据此判断,氯化铝是
(4)现有a~g 7种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:

①元素的原子间反应最容易形成离子键的是
A.c和f B.b和g C.d和g D.b和e
②写出a~g 7种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式
(5)a与e能形成氢化物的空间构型为
您最近一年使用:0次
2022-10-24更新
|
270次组卷
|
2卷引用:陕西省延安市第一中学2021-2022学年高一下学期期中考试化学试题
21-22高二上·吉林通化·开学考试
名校
解题方法
6 . 下表是元素周期表的一部分,用化学用语回答下列有关问题:
(1)写出下列元素符号:①_______ ,画出原子的结构示意图:④_______ 。
(2)在①—⑫元素中,金属性最强的元素与⑦元素形成化合物中化学键是_______ 。
(3)元素⑦与元素⑧相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ 。
a.常温下⑦的单质和⑧的单质状态不同
b.③的氢化物比⑦的氢化物稳定
c.一定条件下⑦和③的单质都能与氢氧化钠溶液反应
(4)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素可以形成_______ (填“离子”或“共价”)化合物,用电子式表示其形成过程:_______ 。①的+4价氧化物被烧碱溶液吸收生成两种钠盐的离子方程是_______ 。
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,它可与⑧形成一种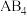 型化合物,请写出该化合物的电子式:
型化合物,请写出该化合物的电子式:_______ 。
(6) 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成
在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成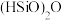 等,写出该反应的化学方程式
等,写出该反应的化学方程式_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ⑧ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在①—⑫元素中,金属性最强的元素与⑦元素形成化合物中化学键是
(3)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同
b.③的氢化物比⑦的氢化物稳定
c.一定条件下⑦和③的单质都能与氢氧化钠溶液反应
(4)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素可以形成
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,它可与⑧形成一种
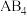 型化合物,请写出该化合物的电子式:
型化合物,请写出该化合物的电子式:(6)
 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成
在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成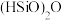 等,写出该反应的化学方程式
等,写出该反应的化学方程式
您最近一年使用:0次
名校
解题方法
7 . 根据元素周期表和元素周期律判断,下列叙述不正确 的是
| A.氢元素与其他元素既可形成共价化合物也可形成离子化合物 |
| B.气态氢化物的稳定性:H2O > NH3 > SiH4 |
C.用中文“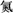 ”(ào)命名的第118号元素在周期表中位于第七周期0族 ”(ào)命名的第118号元素在周期表中位于第七周期0族 |
D.下图所示实验可证明元素的非金属性:Cl > C > Si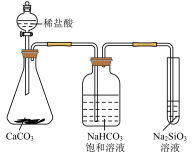 |
您最近一年使用:0次
2020-11-03更新
|
600次组卷
|
6卷引用:山东省济南市山东师范大学附属中学2019-2020学年高一下学期5月学业水平检测化学试题
山东省济南市山东师范大学附属中学2019-2020学年高一下学期5月学业水平检测化学试题(已下线)第4章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)黑龙江省大庆铁人中学2020-2021学年高一下学期开学考试化学试题安徽省蚌埠田家炳中学2020-2021学年高一4月月考化学试题辽宁省朝阳市建平县实验中学2021-2022学年高一下学期第一次月考化学试题(已下线)第16单元 物质的结构与性质(选考)(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷
解题方法
8 . 下列每一序号代表一种元素。元素①是常见的过渡元素,其氧化物为黑色且具有磁性。元素②~⑤的性质如表1和元素⑥~⑩在周期表中的位置如表2所示。请回答下列有关问题:
表1

(1)元素⑤的简单离子的结构示意图是_ ;所给元素中,其含氧化合物能用于漂白,该元素可能是_ (填元素符号)。
(2)元素④在元素周期表中的位置是___ ,该元素的氢化物与元素⑤的单质在高温催化剂条件下反应的化学方程式为_____ 。
(3)元素③的单质与元素①的磁性氧化物在高温条件下发生反应的化学方程式为______ 。
(4)元素⑥的单质在元素⑤的单质中燃烧的产物含有的化学键为___ 。
(5)元素⑦ 、⑧、⑨的氢化物的稳定性由弱到强的顺序为__ (填化学式)。设计实验证明单质氧化性顺序为⑩>⑧____ 。
元素序号 | ② | ③ | ④ | ⑤ |
原子半径/pm | 130 | 118 | 75 | 73 |
主要化合价 | +2 | +3 | +5、+3、-3 | -2 |

(1)元素⑤的简单离子的结构示意图是
(2)元素④在元素周期表中的位置是
(3)元素③的单质与元素①的磁性氧化物在高温条件下发生反应的化学方程式为
(4)元素⑥的单质在元素⑤的单质中燃烧的产物含有的化学键为
(5)元素⑦ 、⑧、⑨的氢化物的稳定性由弱到强的顺序为
您最近一年使用:0次
2020-07-23更新
|
27次组卷
|
2卷引用:山西省朔州市怀仁市第一中学云东校区2019-2020学年高一期末考试化学试题
解题方法
9 . 下列说法正确的是
| A.氯化钠熔化时克服离子键,碘升华克服共价键 |
| B.HF分子很稳定是由于HF分子之间能形成氢键 |
| C.一氯甲烷只有一种空间结构,证明甲烷是正四面体的空间结构而不是平面结构 |
| D.分子式为C5H12O且能与钠反应的有机物的同分异构体有8种 |
您最近一年使用:0次
10 . 下表列出了9种元素在元素周期表中的位置示意。
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_____
(2)画出元素⑧形成的简单离子的结构示意图_________________
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_________
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是__________________
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是_______ (填化学式),写出元素⑥的单质与水反应的离子反应方程式___________________ ,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式__________
| 周期 | ⅠA 1 | 0 18 | ||||||
| 1 | ⅡA 2 | ⅢA 13 | ⅣA 14 | ⅤA 15 | ⅥA 16 | ⅦA 17 | ||
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | |||||
| 4 | ⑨ | |||||||
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
您最近一年使用:0次
2020-01-26更新
|
189次组卷
|
2卷引用:山东省济宁市2019-2020学年高一上学期期末考试化学试题



