1 . 中国航天科技发展举世瞩目。2020年“嫦娥五号”成功携带月球样品返回地球,2021年“天问一号”着陆火星,它们都是由以液氢为燃料的“长征五号”火箭搭载升空的。下列有关说法错误的是
| A.氢气燃烧时有非极性键的断裂和形成 |
| B.氢气燃烧的产物不污染环境,有利于实现“碳中和” |
| C.低温液态储氢可以大大提高氢气的密度,降低储运成本 |
| D.氢气的来源较多,包括水的电解、煤的气化、乙烷裂解和氯碱工业等 |
您最近一年使用:0次
2021-11-13更新
|
254次组卷
|
3卷引用:山西省太原市2021-2022学年高三上学期期中检测化学试题
山西省太原市2021-2022学年高三上学期期中检测化学试题(已下线)第六单元 化学反应与能量(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)湖南省衡阳八中2022-2023学年高三第四次月考化学试题
名校
解题方法
2 .  可以催化
可以催化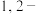 丙二醇(
丙二醇( )获得多种有机物,其反应历程如图所示。下列说法正确的是
)获得多种有机物,其反应历程如图所示。下列说法正确的是

 可以催化
可以催化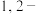 丙二醇(
丙二醇( )获得多种有机物,其反应历程如图所示。下列说法正确的是
)获得多种有机物,其反应历程如图所示。下列说法正确的是
| A.转化过程中涉及非极性共价键断裂与形成 |
B.反应过程中 形成共价键的数目始终保持不变 形成共价键的数目始终保持不变 |
| C.如果原料是乙二醇,则主要有机产物是乙二醛和乙烯 |
D. 催化氧化 催化氧化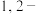 丙二醇所得产物与 丙二醇所得产物与 催化时相同 催化时相同 |
您最近一年使用:0次
2021-11-12更新
|
567次组卷
|
5卷引用:江苏省苏州市2021-2022学年高三上学期期中考试调研化学试题
江苏省苏州市2021-2022学年高三上学期期中考试调研化学试题江苏省苏州市相城区陆慕高级中学2021-2022学年高三上学期期中调研考试化学试题(已下线)3.2.1 醇-2021-2022学年高二化学课后培优练(人教版2019选择性必修3)江苏省泰州中学2022-2023学年高三上学期第一次月度检测化学试题18 2024年苏州高新区吴县高级中学高二3月月考
名校
解题方法
3 . 下列电子式书写正确的是
A.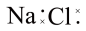 | B. | C. | D. |
您最近一年使用:0次
名校
4 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.pH=1的H2SO4溶液中含有0.1NA个H+ |
| B.3.1gP4(正四面体结构)中的共价键数目为0.4NA |
| C.2.3gNa在空气中点燃,完全反应转移的电子数一定为0.1NA |
| D.11g由3H和16O组成的超重水中,中子数和电子数之和为10NA |
您最近一年使用:0次
2021-11-03更新
|
867次组卷
|
6卷引用:四川省绵阳市2021-2022学年高三上学期第一次考试理综化学试题
四川省绵阳市2021-2022学年高三上学期第一次考试理综化学试题重庆市凤鸣山中学教育集团2021-2022学年高三上学期期中考试化学试题广东省湛江市第二十一中学2021—2022学年高三上学期11月月考化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)卷04 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)福建省龙岩市上杭县第一中学2022-2023学年高三上学期12月月考化学试题
5 . 某化合物为有机强酸,常用作医药和农药原料,其结构式如图所示。已知X、Y、Z、W均为短周期元素且原子序数依次递增,X、Y、W位于不同周期,Z、W位于同一主族。下列叙述正确的是


| A.Z的简单氢化物沸点高于W的简单氢化物 |
| B.W的氧化物对应水化物一定为强酸 |
C.原子半径大小顺序为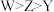 |
| D.该化合物中所有原子最外层均满足8电子稳定结构 |
您最近一年使用:0次
名校
解题方法
6 . 亚硝酰氯( ,熔点:
,熔点: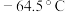 ,沸点:
,沸点: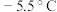 )是一种黄色气体,遇水易水解生成
)是一种黄色气体,遇水易水解生成 和
和 。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
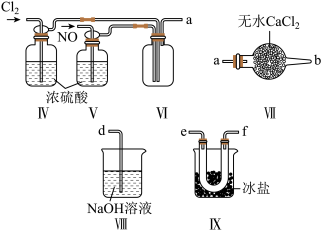
(1)甲组的同学拟制备原料气 和
和 ,制备装置如图所示:
,制备装置如图所示:
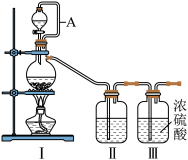
为制备纯净干燥的气体,补充表中缺少的药品
(2)乙组同学利用甲组制得的 和
和 制备
制备 ,装置如图所示:
,装置如图所示:
① 分子中各原子均满足8电子稳定结构,则
分子中各原子均满足8电子稳定结构,则 的电子式为
的电子式为_______ ;
②装置连接顺序为a→_______ (按气流自左向右方向,用小写字母表示);
③装置Ⅳ、Ⅴ除了可进一步干燥 、
、 外,另一作用是
外,另一作用是_______ ;
④装置Ⅷ中吸收尾气时, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
 ,熔点:
,熔点: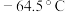 ,沸点:
,沸点: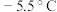 )是一种黄色气体,遇水易水解生成
)是一种黄色气体,遇水易水解生成 和
和 。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。(1)甲组的同学拟制备原料气
 和
和 ,制备装置如图所示:
,制备装置如图所示:
为制备纯净干燥的气体,补充表中缺少的药品
| 装置I | 装置Ⅱ | ||
| 烧瓶中 | 分液漏斗中 | ||
制备纯净的 |  | ①浓盐酸 | ② |
制备纯净的 |  | ③ | ④水 |
 和
和 制备
制备 ,装置如图所示:
,装置如图所示:
①
 分子中各原子均满足8电子稳定结构,则
分子中各原子均满足8电子稳定结构,则 的电子式为
的电子式为②装置连接顺序为a→
③装置Ⅳ、Ⅴ除了可进一步干燥
 、
、 外,另一作用是
外,另一作用是④装置Ⅷ中吸收尾气时,
 发生反应的化学方程式为
发生反应的化学方程式为
您最近一年使用:0次
7 . 回答下列问题
(1)①写出金刚砂的化学式:_______ ;②写出S2Cl2的电子式:_______ ;
(2)NH2OH 显弱碱性的原因和NH3类似,写出 NH2OH 在水溶液中的电离方程式_______ 。
(3)用一个化学方程式证明碳酸的酸性强于硅酸:_______ 。
(1)①写出金刚砂的化学式:
(2)NH2OH 显弱碱性的原因和NH3类似,写出 NH2OH 在水溶液中的电离方程式
(3)用一个化学方程式证明碳酸的酸性强于硅酸:
您最近一年使用:0次
8 . 甲学生对 与
与 和KSCN混合溶液的反应进行实验探究。
和KSCN混合溶液的反应进行实验探究。
(1)B中反应的离子方程式是____________________ 。
(2)A中溶液变红的原因是(用离子方程式回答)①___________ ;②___________
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验:
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在______ 。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是 与Cl2发生了反应。
与Cl2发生了反应。
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN-的电子式为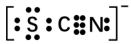 。
。
①甲同学认为SCN-中碳元素没有被氧化,理由是___________ 。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中的___________ 元素被氧化。
 与
与 和KSCN混合溶液的反应进行实验探究。
和KSCN混合溶液的反应进行实验探究。| 操作 | 现象 |
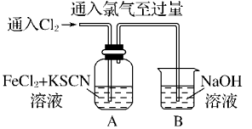 | Ⅰ.A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
(2)A中溶液变红的原因是(用离子方程式回答)①
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验:
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是
 与Cl2发生了反应。
与Cl2发生了反应。(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN-的电子式为
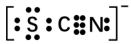 。
。①甲同学认为SCN-中碳元素没有被氧化,理由是
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中的
您最近一年使用:0次
9 . 下列关于化学键的说法,认识错误的有几个
①s-s σ键与s-p σ键的电子云对称性不同
② 键不能单独存在,一定要和
键不能单独存在,一定要和 键共存
键共存
③含有 键的化合物与只含
键的化合物与只含 键的化合物的化学性质不同
键的化合物的化学性质不同
④两个非金属元素的原子之间形成的化学键都是共价键
⑤分子中含有共价键,则一定只含有一个 键
键
⑥成键的原子间原子轨道重叠越多,共价键越牢固
⑦1个N原子最多只能与3个H原子结合形成NH3分子,是由共价键的饱和性决定的
①s-s σ键与s-p σ键的电子云对称性不同
②
 键不能单独存在,一定要和
键不能单独存在,一定要和 键共存
键共存③含有
 键的化合物与只含
键的化合物与只含 键的化合物的化学性质不同
键的化合物的化学性质不同④两个非金属元素的原子之间形成的化学键都是共价键
⑤分子中含有共价键,则一定只含有一个
 键
键⑥成键的原子间原子轨道重叠越多,共价键越牢固
⑦1个N原子最多只能与3个H原子结合形成NH3分子,是由共价键的饱和性决定的
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
10 . 氮元素是空气中含量最多的元素,在自然界中的分布十分广泛,在生物体内亦有极大作用。一定条件下,含氮元素的物质可发生如图所示的循环转化。回答下列问题:
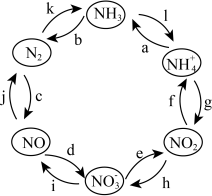
(1)氮分子的电子式为________ 。
(2)图中属于“氮的固定”的是______ (填字母)。
(3)若反应h是在NO2与H2O的作用下实现,则该反应中氧化剂与还原剂物质的量之比为_____ 。
(4)若反应i是在酸性条件下由 与Fe2+的作用实现,则该反应的离子方程式为
与Fe2+的作用实现,则该反应的离子方程式为___ 。

(1)氮分子的电子式为
(2)图中属于“氮的固定”的是
(3)若反应h是在NO2与H2O的作用下实现,则该反应中氧化剂与还原剂物质的量之比为
(4)若反应i是在酸性条件下由
 与Fe2+的作用实现,则该反应的离子方程式为
与Fe2+的作用实现,则该反应的离子方程式为
您最近一年使用:0次



