解题方法
1 . 如图为元素周期表的一部分,图中所列字母分别代表一种化学元素。

(1)元素b、c、e形成的常见稳定单质中最易与H2化合的是___________ (填化学式)。
(2)元素d、c所形成的某化合物的摩尔质量为78g/mol,该化合物的化学式为___________ ,其中所含化学键的类型有___________ 。
(3)推测原子序数为35的元素在元素周期表中的位置是___________ 。
(4)依据元素周期律推测,元素f的单质及其化合物的性质正确的是___________(填字母)。
(5)含有非极性键的c的氢化物,其电子式为___________ 。(ab)2称为拟卤素,性质与卤素单质相似,常温下其与NaOH溶液反应的化学方程式为___________ 。

(1)元素b、c、e形成的常见稳定单质中最易与H2化合的是
(2)元素d、c所形成的某化合物的摩尔质量为78g/mol,该化合物的化学式为
(3)推测原子序数为35的元素在元素周期表中的位置是
(4)依据元素周期律推测,元素f的单质及其化合物的性质正确的是___________(填字母)。
| A.f的单质常温下呈气态 | B.f的单质具有强氧化性 |
| C.fc2属于酸性氧化物 | D.fc2既有氧化性又有还原性 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法正确的是
①常温下白磷可自燃而氮气需在放电时才与氧气反应,则非金属性:P>N
②第IA族元素铯的两种同位素137Cs比133Cs多4个质子
③因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
④离子化合物中既可以含有极性共价键又可以含有非极性共价键
⑤C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强
⑥从上到下,卤族元素的非金属性逐渐减弱,所以酸性HCl>HI
⑦离子半径:K+>Cl->S2-
①常温下白磷可自燃而氮气需在放电时才与氧气反应,则非金属性:P>N
②第IA族元素铯的两种同位素137Cs比133Cs多4个质子
③因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
④离子化合物中既可以含有极性共价键又可以含有非极性共价键
⑤C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强
⑥从上到下,卤族元素的非金属性逐渐减弱,所以酸性HCl>HI
⑦离子半径:K+>Cl->S2-
| A.②③④⑤⑥⑦ | B.④⑤ | C.②③④⑦ | D.④⑤⑥ |
您最近一年使用:0次
2022-12-13更新
|
298次组卷
|
6卷引用:陕西省西安市雁塔区第二中学、渭北中学2022-2023学年高一上学期期末联考化学试题
3 . 化合物M(结构如图所示)是一种重要的有机盐,常用作食品和洗涤剂的添加剂,W、X、Y、Z、R是原子序数依次增大的短周期主族元素。下列说法正确的是
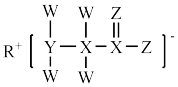
| A.最高价含氧酸的酸性:X>Y |
| B.R的单质在同周期中还原性最强 |
| C.简单气态氢化物的稳定性:Y>Z |
| D.W、Y、Z均为非金属元素,三元素之间只能形成共价化合物 |
您最近一年使用:0次
2023-12-21更新
|
668次组卷
|
3卷引用:陕西省汉中市2023-2024学年高三上学期第一次质量检测化学试题
4 . 如图为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:
(1)②的最高价氧化物的结构式为_______ 。
(2)④⑥元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:_______ 。
(3)⑤和⑨的简单氢化物的稳定性强弱顺序是_______ (填化学式,用“>”连接)。
(4)写出⑨的单质与⑥的最高价氧化物对应的水化物反应的离子方程式_______ 。
(5)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。Se是第四周期与④同主族的元素,下列推断正确的是_______(填字母)。
(6)元素周期表中,某些主族元素与右下方的主族元素的性质具有相似性,如Be与Al,这种规律称为“对角线原则”。Be(OH)2与NaOH溶液反应的离子方程式为_______ 。
族 周期 | IA | 0 | |||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | ||
2 | ② | ③ | ④ | ⑤ | |||||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)④⑥元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:
(3)⑤和⑨的简单氢化物的稳定性强弱顺序是
(4)写出⑨的单质与⑥的最高价氧化物对应的水化物反应的离子方程式
(5)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。Se是第四周期与④同主族的元素,下列推断正确的是_______(填字母)。
| A.SeO2具有还原性 | B.Se的最低负化合价为-1 |
| C.H2SeO3的酸性强于H2SO4 | D. SeO2在一定条件下可与NaOH溶液反应 |
您最近一年使用:0次
5 . 下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
(1)画出①和③两种元素的原子1:2组成的化合物的电子式_______ 。
(2)元素①-⑩中化学性质最不活泼的元素是_______ (填元素符号)。
(3)⑧的离子结构示意图为_______ 。
(4)用电子式表示③与⑤形成的原子个数比为1 ∶2的化合物的形成过程_______ 。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有_______ 。
(6)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。周期表中元素Se的位置在⑧的下方,下列推断正确的是_______(填字母序号)
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素①-⑩中化学性质最不活泼的元素是
(3)⑧的离子结构示意图为
(4)用电子式表示③与⑤形成的原子个数比为1 ∶2的化合物的形成过程
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有
(6)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。周期表中元素Se的位置在⑧的下方,下列推断正确的是_______(填字母序号)
| A.SeO2具有还原性 | B.H2Se的稳定性比H2S强 |
| C.H2SeO4的酸性强于H2SO4 | D.SeO2在一定条件下可与NaOH溶液反应 |
您最近一年使用:0次
解题方法
6 . 四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,W原子的L层电子数是K层的三倍,X的原子半径是短周期主族元素原子中最大的,Y与W同族。下列说法正确的是
| A.简单离子半径:W<X<Z | B.W与X形成的化合物溶于水后溶液呈碱性 |
| C.最简单气态氢化物的热稳定性:W<Y | D.最高价氧化物的水化物的酸性:Y>Z |
您最近一年使用:0次
解题方法
7 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W和Y同族,X和Z同族,X的简单离子和Y的简单离子具有相同的电子层结构,W和X、Z均能形成共价化合物,W和X、Y分别形成的化合物溶于水均呈碱性。下列说法正确的是
| A.4种元素中Y的金属性最弱 |
| B.最高价氧化物对应的水化物的酸性:Z>X |
| C.W和Y形成的化合物与水反应能生成一种还原性气体 |
| D.W和X形成的共价化合物各原子均满足8电子稳定结构 |
您最近一年使用:0次
名校
8 . 下表中相关物质的信息都正确的一项是
| 选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
| A | NaClO | 离子键、共价键 | 强氧化性 | 消毒液 |
| B | H2O2 |  | 不稳定,易分解 | 医用消毒剂 |
| C | NH3 | 共价键 | 水溶液呈弱碱性 | 工业制硝酸 |
| D | NaHCO3 | 离子键 | 受热易分解 | 泡沫灭火器 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-02-04更新
|
648次组卷
|
5卷引用:陕西省渭南市华州区咸林中学2020-2021学年高三下学期第1次教学质量检测化学试题
陕西省渭南市华州区咸林中学2020-2021学年高三下学期第1次教学质量检测化学试题2016届西藏日喀则一中高三下学期二模考试理综化学试卷【全国百强校】山东省山东师范大学附属中学2019届高三上学期第五次模拟考试化学试题新疆巴音郭楞蒙古自治州第一中学2021届高三上学期期中考试化学试题(已下线)第13讲 原子结构 化学键(练)-2023年高考化学一轮复习讲练测(新教材新高考)
名校
9 . 原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。
(1)写出Y2O2的电子式:__________ ,其中含有的化学键是_________ 。
(2)Z元素在周期表中的位置是第________ 周期、第________ 族。X和Z形成的一种二元化合物具有温室效应,其相对分子质量在170~190之间,且Z的质量分数约为70%。该化合物的化学式为____________________ 。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是________ (填化学式)。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是_________ (填化学式)。
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式________________ 。
(1)写出Y2O2的电子式:
(2)Z元素在周期表中的位置是第
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式
您最近一年使用:0次



