解题方法
1 . 在元素周期表的一百多种化学元素中,非金属元素仅有24种,但在社会生活中占有着重要的位置。
(1)根据元素周期表的分区,非金属元素分布在元素周期表的__________ 区。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用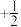 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的磷原子,其核外电子占据的最高能层符号为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其核外电子占据的最高能层符号为__________ ,自旋磁量子数的代数和为__________ 。
(3)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示。试分析碳元素的
变化趋势如图所示。试分析碳元素的 大于氮元素的
大于氮元素的 的原因
的原因__________ 。

(4)写出一种与 互为等电子体的一种分子的化学式:
互为等电子体的一种分子的化学式:__________ 。
(5)乙醇( )能与水以任意比例互溶,但与其结构相似的乙硫醇(
)能与水以任意比例互溶,但与其结构相似的乙硫醇(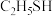 )微溶于水,原因是
)微溶于水,原因是__________ 。
(6)分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,则与苯分子具有相似结构的吡啶(
键的电子数,则与苯分子具有相似结构的吡啶(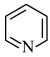 )中的大
)中的大 键应表示为
键应表示为__________ 。
(7)由两种不同的卤素组成的化合物叫卤素互化物(如BrCl等),其性质与卤素单质相似。试写出BrCl与水发生反应的化学方程式:__________ 。
(1)根据元素周期表的分区,非金属元素分布在元素周期表的
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
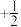 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的磷原子,其核外电子占据的最高能层符号为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其核外电子占据的最高能层符号为(3)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示。试分析碳元素的
变化趋势如图所示。试分析碳元素的 大于氮元素的
大于氮元素的 的原因
的原因
(4)写出一种与
 互为等电子体的一种分子的化学式:
互为等电子体的一种分子的化学式:(5)乙醇(
 )能与水以任意比例互溶,但与其结构相似的乙硫醇(
)能与水以任意比例互溶,但与其结构相似的乙硫醇(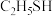 )微溶于水,原因是
)微溶于水,原因是(6)分子中的大
 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,则与苯分子具有相似结构的吡啶(
键的电子数,则与苯分子具有相似结构的吡啶( )中的大
)中的大 键应表示为
键应表示为(7)由两种不同的卤素组成的化合物叫卤素互化物(如BrCl等),其性质与卤素单质相似。试写出BrCl与水发生反应的化学方程式:
您最近一年使用:0次
2024-04-08更新
|
66次组卷
|
2卷引用:河南省南阳市六校联考2023-2024学年高二下学期3月月考化学试卷
名校
2 . 回答下列问题
(1)基态S原子的价电子中,两种自旋状态的电子数之比为___________ 。
(2) 与
与 相比,第二电离能与第一电离能差值更大的是
相比,第二电离能与第一电离能差值更大的是___________ 。
(3) 成为阳离子时首先失去
成为阳离子时首先失去___________ 轨道电子, 的价层电子排布式
的价层电子排布式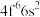 ,
,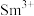 价层电子排布式为
价层电子排布式为___________ 。
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是___________ (填标号),第三电离能的变化图是___________ (填标号)。
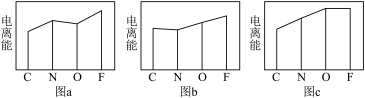
(5)氟原子激发态的电子排布式有___________ ,其中能量较高的是___________ 。(填标号)
a、 b、
b、 c、
c、 d、
d、
(6)对于基态 原子,下列叙述正确的是
原子,下列叙述正确的是___________ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为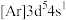
B.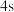 电子能量较高,总是在比
电子能量较高,总是在比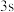 电子离核更远的地方运动
电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(7)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
(8)H、B、N中,原子半径最大的是___________ 。根据对角线规则,B的一些化学性质与元素___________ 的相似。
(9)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(1)基态S原子的价电子中,两种自旋状态的电子数之比为
(2)
 与
与 相比,第二电离能与第一电离能差值更大的是
相比,第二电离能与第一电离能差值更大的是(3)
 成为阳离子时首先失去
成为阳离子时首先失去 的价层电子排布式
的价层电子排布式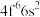 ,
,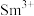 价层电子排布式为
价层电子排布式为(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(5)氟原子激发态的电子排布式有
a、
 b、
b、 c、
c、 d、
d、
(6)对于基态
 原子,下列叙述正确的是
原子,下列叙述正确的是A.轨道处于半充满时体系总能量低,核外电子排布应为
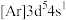
B.
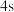 电子能量较高,总是在比
电子能量较高,总是在比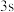 电子离核更远的地方运动
电子离核更远的地方运动C.电负性比钾高,原子对键合电子的吸引力比钾大
(7)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(8)H、B、N中,原子半径最大的是
(9)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A.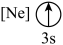 | B.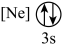 | C.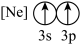 | D.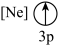 |
您最近一年使用:0次



