解题方法
1 . 铁、铜、锌在医药、催化及材料等领域中都有广泛的应用。回答下列问题:
(1)写出Fe在元素周期表中的位置为_______ 。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,
表示, 即称为电子的自旋磁量子数。对于基态的氧原子,其价电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态的氧原子,其价电子自旋磁量子数的代数和为_______ 。下列现象与原子核外电子跃迁有关的是_______ (填序号)。
a.焰火 b.LED灯光 c.金属导电 d.核辐射
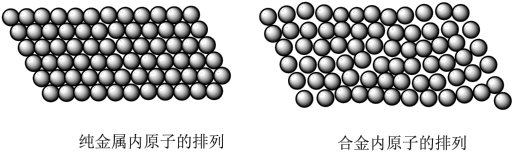
(2)纯金属内加入其他元素形成合金之后,合金硬度变大。结合纯金属和合金的结构如图所示,从微观的角度原因是_______ 。
(3)与铜同周期,N能层电子数与铜相同,熔点最低的金属是_______ 。铜的第一电离能为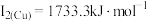 ,第二电离能为
,第二电离能为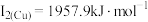 ,锌的第一电离能为
,锌的第一电离能为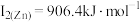 ,第二电离能为
,第二电离能为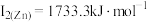 ,
,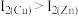 的原因是
的原因是_______ 。
(4)甘氨酸铜有顺式和反式两种同分异构体,结构如下图。
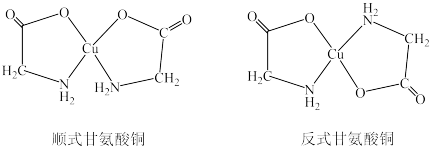
分析顺式甘氨酸铜能溶于水,反式甘氨酸铜难溶于水的原因_______ 。
(1)写出Fe在元素周期表中的位置为
 表示,与之相反的用
表示,与之相反的用 表示,
表示, 即称为电子的自旋磁量子数。对于基态的氧原子,其价电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态的氧原子,其价电子自旋磁量子数的代数和为a.焰火 b.LED灯光 c.金属导电 d.核辐射
(2)纯金属内加入其他元素形成合金之后,合金硬度变大。结合纯金属和合金的结构如图所示,从微观的角度原因是

(3)与铜同周期,N能层电子数与铜相同,熔点最低的金属是
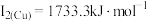 ,第二电离能为
,第二电离能为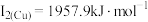 ,锌的第一电离能为
,锌的第一电离能为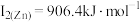 ,第二电离能为
,第二电离能为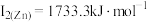 ,
,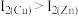 的原因是
的原因是(4)甘氨酸铜有顺式和反式两种同分异构体,结构如下图。

分析顺式甘氨酸铜能溶于水,反式甘氨酸铜难溶于水的原因
您最近一年使用:0次
2014·山东淄博·二模
2 . 氮族元素包括N、P、As、Sb和Bi五种元素。
(1)下列关于氮族元素的说法正确的是___ 。
a.N2可用于填充霓虹灯。其发光原理是电子从能量较低的轨道跃迁到能量较高的轨道,以光的形式释放能量
b.P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na
c.基态As原子中,电子占据的最高能级为4d
d.Bi原子中最外层有5个能量相同的电子
(2)NH3在水中的溶解度比PH3大得多,其原因是___  向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有
向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有___ 和___ 。
(3)PCl3分子中,Cl-P-Cl键的键角___ 109°28'(填“>”“<”或“2” 。
。
(4)白磷(P4)是磷的一种单质,它属于分子晶体,其晶胞结构如图。已知该晶体的密度为ρg·cm-3,晶胞的边长为acm,则阿伏加 德罗常数为___ mol-1(用含p、a的式子表示 。
。

(1)下列关于氮族元素的说法正确的是
a.N2可用于填充霓虹灯。其发光原理是电子从能量较低的轨道跃迁到能量较高的轨道,以光的形式释放能量
b.P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na
c.基态As原子中,电子占据的最高能级为4d
d.Bi原子中最外层有5个能量相同的电子
(2)NH3在水中的溶解度比PH3大得多,其原因是
 向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有
向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有(3)PCl3分子中,Cl-P-Cl键的键角
 。
。(4)白磷(P4)是磷的一种单质,它属于分子晶体,其晶胞结构如图。已知该晶体的密度为ρg·cm-3,晶胞的边长为acm,则阿伏加 德罗常数为
 。
。
您最近一年使用:0次
2019-12-27更新
|
94次组卷
|
3卷引用:2013-2014山东省淄博市高三二模理综化学试卷



