名校
解题方法
1 . 原子序数小于等于36的Q、W、X、Y、Z五种元素,原子序数逐渐增大,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含成单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子,回答下列问题(涉及元素时用对应的元素符号表示):
(1)X、Y、Z三种元素的电负性由大到小的顺序是___________ 。
(2)1mol QWX与1mol 所含
所含 键的比值为
键的比值为___________ 。
(3)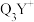 中心原子采用
中心原子采用___________ 杂化,其键角比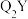 中键角
中键角___________ (填“大”或“小”),原因是:___________ 。
(4)根据VSEPR理论预测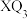 的空间构型为
的空间构型为___________ 。
(5)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为___________ 。
①该化合物的化学式为:___________ 。
②预测该化合物熔点应___________ 金刚石(填“高于”或“低于”),原因是:___________ 。
(1)X、Y、Z三种元素的电负性由大到小的顺序是
(2)1mol QWX与1mol
 所含
所含 键的比值为
键的比值为(3)
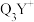 中心原子采用
中心原子采用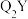 中键角
中键角(4)根据VSEPR理论预测
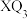 的空间构型为
的空间构型为(5)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为
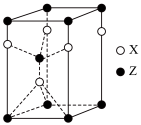
①该化合物的化学式为:
②预测该化合物熔点应
您最近一年使用:0次



