1 . 通常情况下,氯化钠、氯化铯、二氧化碳和二氧化硅的晶体晶胞结构分别如图所示,下列关于这些晶体晶胞结构和性质的叙述不正确的是




| A.同一主族的元素与另一相同元素所形成的化学式相似的物质一定具有相同的晶体结构 |
| B.氯化钠、氯化铯和二氧化碳的晶体都是立方的晶胞结构,它们具有相似的物理性质 |
| C.二氧化碳晶体是分子晶体,其中不仅存在分子间作用力,而且也存在共价键 |
| D.在二氧化硅晶体中,平均每个Si形成4个Si-O共价单键 |
您最近一年使用:0次
2022-12-18更新
|
286次组卷
|
2卷引用:吉林省长春市第五中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
2 . 下列说法错误的是
A.从CH4、 、 、 为正四面体结构,可推测PH 为正四面体结构,可推测PH 、 、 也为正四面体结构 也为正四面体结构 |
| B.1mol金刚石晶体中,平均含有2molC-C键 |
| C.水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键 |
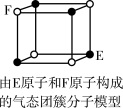
| D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
您最近一年使用:0次
2022-10-31更新
|
243次组卷
|
8卷引用:贵州省思南中学2018-2019学年高二下学期期末考试化学试题
22-23高二上·浙江·期末
解题方法
3 . 下列说法正确的是
| A.金刚石晶体中每个碳原子被12个最小碳环共用 |
| B.石墨为混合型晶体,因层间存在分子间作用力,故熔点低于金刚石 |
| C.金属能导热是因为自由电子在热的作用下相互碰撞,从而发生热的传导 |
| D.NaCl晶体中每个Na+周围有6个距离最近且相等的Na+ |
您最近一年使用:0次
4 . 下面的排序不正确的是
| A.晶体沸点由低到高:CF4<CCl4<CBr4 | B.晶格能由大到小: NaF> NaCl> NaBr |
| C.硬度由大到小:金刚石>碳化硅>晶体硅 | D.熔点由高到低:Na>Mg>Al |
您最近一年使用:0次
5 . 2017年1月,南京理工大学胡炳成教授团队成功合成世界首个全氮阴离子盐,全氮阴离子化学式为N 。下列关于全氮阴离子盐的说法正确的是
。下列关于全氮阴离子盐的说法正确的是
 。下列关于全氮阴离子盐的说法正确的是
。下列关于全氮阴离子盐的说法正确的是A.每个N 含有26个电子 含有26个电子 | B.N 的摩尔质量为71g·mol-1 的摩尔质量为71g·mol-1 |
| C.全氮阴离子盐既含离子键又含共价键 | D.全氮阴离子盐属于原子晶体 |
您最近一年使用:0次
6 . 有关晶体的结构如图所示,下列说法中不正确 的是。
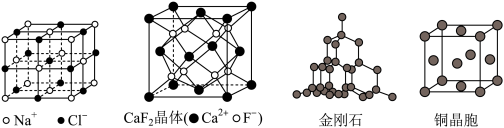

| A.在NaCl晶体中,每个晶胞平均占有4个Cl- |
| B.在CaF2晶体中,每个晶胞平均占有6个Ca2+ |
| C.在金刚石晶体中,碳原子数与碳碳键个数之比为1∶4 |
| D.铜晶体为面心立方最密堆积,该晶体中含有正八面体空隙和正四面体空隙 |
您最近一年使用:0次
2022-09-23更新
|
318次组卷
|
2卷引用:山东省菏泽市单县二中2021-2022学年高二下学期期末测试化学试题
7 . 下列说法错误的是
| A.离子晶体在熔化状态下一定能导电 |
| B.分子间作用力越大,分子越稳定 |
| C.原子晶体中可能存在极性键 |
| D.分子晶体的状态变化,需克服分子间作用力 |
您最近一年使用:0次
8 . 关于元素或物质的结构与性质的说法正确的是
| A.最外层电子数为2的元素全部分布在元素周期表s区 |
B.依据对角线规则可知锂在过量氧气中燃烧的产物为 |
| C.等质量的石墨与金刚石含有相同数目的σ键 |
| D.晶体中有阴离子必有阳离子,反之有阳离子也必有阴离子 |
您最近一年使用:0次
9 . 关于元素或物质的结构与性质的说法正确的是
| A.最外层电子数为2的元素全部分布在元素周期表s区 |
B.依据对角线规则可知锂在过量氧气中燃烧的产物为 |
| C.等质量的石墨与金刚石含有相同数目的σ键 |
| D.晶体中有阴离子必有阳离子,反之有阳离子也必有阴离子 |
您最近一年使用:0次
解题方法
10 . 下列各组物质中,化学键类型相同,形成的晶体类型也相同的是
A. 和 和 | B. 和 和 | C. 和 和 | D.KCl和HCl |
您最近一年使用:0次



