解题方法
1 . 某元素X的激发态原子的电子排布式为1s22s22p63s13p3,则该元素基态原子的电子排布式为_______ ,其最高价氧化物属于_______ 晶体;Z原子的核电荷数为33,其在元素周期表中的位置是_______ ,属于_______ 区的元素。
您最近一年使用:0次
解题方法
2 . (1)离子化合物MgO2可被用于治疗消化道疾病,各原子均满足8电子稳定结构。写出MgO2的电子式___ 。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是___ 。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是
您最近一年使用:0次
解题方法
3 . (1)写出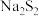 的电子式
的电子式 ___________ 。
(2)硼元素可形成多种化合物。其中氮化硼( )熔点为3774℃,而丁硼烷(
)熔点为3774℃,而丁硼烷( )熔点仅
)熔点仅 ℃。氮化硼熔点远高于丁硼烷的可能原因是
℃。氮化硼熔点远高于丁硼烷的可能原因是___________ 。
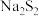 的电子式
的电子式 (2)硼元素可形成多种化合物。其中氮化硼(
 )熔点为3774℃,而丁硼烷(
)熔点为3774℃,而丁硼烷( )熔点仅
)熔点仅 ℃。氮化硼熔点远高于丁硼烷的可能原因是
℃。氮化硼熔点远高于丁硼烷的可能原因是
您最近一年使用:0次
2021-06-27更新
|
269次组卷
|
2卷引用:浙江省衢州市2020-2021学年高二下学期(6月)教学质量检测化学试题
4 . (1)1mol金刚石中有___ molC—C键,1mol二氧化硅中含有___ molSi—O键。
(2)N2H4的电子式为___ 。
(3)有机物乙醇和乙酸都可以和水互溶的原因是:___ 。
(2)N2H4的电子式为
(3)有机物乙醇和乙酸都可以和水互溶的原因是:
您最近一年使用:0次
5 . I.氮化硼晶体的结构与金刚石相似,其晶胞如图所示。
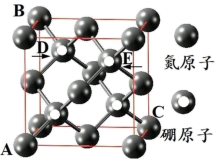
(1)在一个晶胞中,含有硼原子_______ 个,氮原子_______ 个。
(2)已知氮化硼晶胞参数为γcm,则在此晶胞中,任意两个原子之间的最短距离是___ cm,DE原子之间的距离是____ cm。
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。已知三个原子分数坐标参数:A为(0,0,0)、B为(0,1,1)、C为(1,1,0);则E原子为________ 。
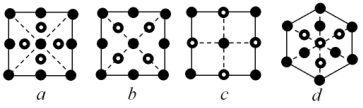
(4)氮化硼晶胞的俯视投影图是_______ 。
(5)设NA为阿伏加德罗常数的值,则氮化硼晶体的密度为_______ g/cm3(用代数式表示)。
II.在硅酸盐中,SiO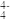 四面体(如图为俯视投影图)通过共用顶角氧原子可形成链状、环状等多种结构型式。
四面体(如图为俯视投影图)通过共用顶角氧原子可形成链状、环状等多种结构型式。
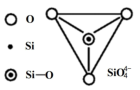
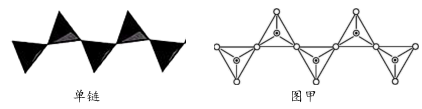
(6)图甲为一种无限长单链结构的多硅酸根,其中Si与O的原子数之比为_______ ,化学式为_______ 。

(1)在一个晶胞中,含有硼原子
(2)已知氮化硼晶胞参数为γcm,则在此晶胞中,任意两个原子之间的最短距离是
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。已知三个原子分数坐标参数:A为(0,0,0)、B为(0,1,1)、C为(1,1,0);则E原子为
(4)氮化硼晶胞的俯视投影图是

(5)设NA为阿伏加德罗常数的值,则氮化硼晶体的密度为
II.在硅酸盐中,SiO
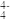 四面体(如图为俯视投影图)通过共用顶角氧原子可形成链状、环状等多种结构型式。
四面体(如图为俯视投影图)通过共用顶角氧原子可形成链状、环状等多种结构型式。
(6)图甲为一种无限长单链结构的多硅酸根,其中Si与O的原子数之比为

您最近一年使用:0次
2021-03-06更新
|
1169次组卷
|
3卷引用:山东省淄博市2020-2021学年高二上学期期末考试化学试题
山东省淄博市2020-2021学年高二上学期期末考试化学试题(已下线)3.2 分子晶体与共价晶体(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)内蒙古通辽市重点学校2022-2023学年高二下学期3月质量检测化学试题
6 . (1)已知酸性H2CO3>HClO>HCO ,用一个离子方程式表示ClO-与CO
,用一个离子方程式表示ClO-与CO 结合H+的相对强弱:
结合H+的相对强弱:_______ 。
(2)NaCN是离子化合物,各原子都满足8电子稳定结构,写出NaCN电子式_______ 。
(3)已知金刚石中C-C键能小于C60中C-C键能,有同学据此认为C60的熔点高于金刚石,你认为此说法是否正确_______ (填“正确”或“不正确”),并阐述理由_______ 。
 ,用一个离子方程式表示ClO-与CO
,用一个离子方程式表示ClO-与CO 结合H+的相对强弱:
结合H+的相对强弱:(2)NaCN是离子化合物,各原子都满足8电子稳定结构,写出NaCN电子式
(3)已知金刚石中C-C键能小于C60中C-C键能,有同学据此认为C60的熔点高于金刚石,你认为此说法是否正确
您最近一年使用:0次
解题方法
7 . 碳及其化合物广泛存在于自然界中,回答下列问题:
(1)C原子的价电子轨道表达式为_______ ,碳元素在周期表中_______ 区,它所在的周期,第一电离能最大的元素是_______ 。
(2) 和N2是等电子体,
和N2是等电子体, 的电子式为
的电子式为_______ 。
(3)C60和金刚石互为同素异形体,熔点较高者为_______ ,其原因是_______ 。
(4)丙烯醇的结构简式为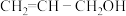 ,其中碳原子的杂化类型为
,其中碳原子的杂化类型为_______ ,σ键和π键的个数比为_______ 。
(1)C原子的价电子轨道表达式为
(2)
 和N2是等电子体,
和N2是等电子体, 的电子式为
的电子式为(3)C60和金刚石互为同素异形体,熔点较高者为
(4)丙烯醇的结构简式为
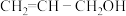 ,其中碳原子的杂化类型为
,其中碳原子的杂化类型为
您最近一年使用:0次
解题方法
8 . 碳元素的单质有多种形式,如图依次是金刚石、石墨和C60的结构示意图:

分析上图可知:
(1)金刚石的晶体类型是_______________ ,晶体中每个最小环上的碳原子的个数是___________ 。
(2)石墨晶体呈层状结构,层内每个正六边形拥有的碳原子的个数是________ ,层与层之间的作用力是______________ 。
(3)C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则Co分子中σ键与π键数目之比为_______________ 。

分析上图可知:
(1)金刚石的晶体类型是
(2)石墨晶体呈层状结构,层内每个正六边形拥有的碳原子的个数是
(3)C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则Co分子中σ键与π键数目之比为
您最近一年使用:0次
名校
解题方法
9 . CCl4、SiC,P4是空间构型均为正四面体的三种物质,其中形成的晶体类型与其他两种物质不同的是__ ,键角与其他两种物质不同的是__ 。
您最近一年使用:0次
10 . (1)比较S与Cl非金属性相对强弱:S________ Cl(填“>”、“<”或“=”);用一个置换反应的离子方程式说明S与Cl非金属性相对强弱________ 。
(2)等电子体具有相似的化学键特征,CO2分子与SCN-离子为等电子体,写出离子化合物KSCN的电子式________ 。
(3)金刚石晶体和石墨晶体都是由碳原子构成,但金刚石晶体的硬度比石墨晶体的大的多,主要原因是_______ 。
(2)等电子体具有相似的化学键特征,CO2分子与SCN-离子为等电子体,写出离子化合物KSCN的电子式
(3)金刚石晶体和石墨晶体都是由碳原子构成,但金刚石晶体的硬度比石墨晶体的大的多,主要原因是
您最近一年使用:0次



