名校
解题方法
1 . 工业上以赤泥[主要成分是Sc2O3,另含有少量Fe2O3、SiO2(不溶于酸)、Al2O3等]为主要原料提取氧化钪,其工艺流程如图所示(P2O4是一种磷酸酯萃取剂,草酸化学式为H2C2O4)。
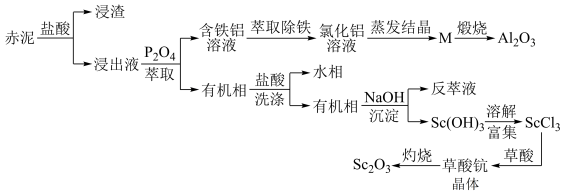
回答下列问题:
(1)赤泥经盐酸处理后所得“浸渣”主要成分为____ (化学式)。
(2)赤泥“盐酸酸浸”时不宜温度过高,原因是____ 。
(3)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时P2O4最佳浓度及料液温度分别为____ 、____ ;
P2O4浓度对萃取率的影响如表:
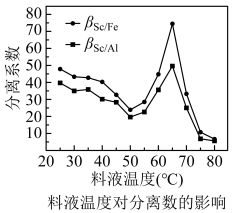
料液温度对分离系数的影响如图:
(4)M经煅烧后可得到Al2O3,则M成分为____ 。
(5)为探究所得草酸钪晶体Sc2(C2O4)3·xH2O中结晶水的含量,取2.96g样品(纯度为75%),灼烧得到0.69gSc2O3固体,则x=____ 。
(6)草酸钪晶体在空气中灼烧分解反应方程式为____ 。

回答下列问题:
(1)赤泥经盐酸处理后所得“浸渣”主要成分为
(2)赤泥“盐酸酸浸”时不宜温度过高,原因是
(3)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时P2O4最佳浓度及料液温度分别为
P2O4浓度对萃取率的影响如表:
试验编号 | P2O4浓度/% | 分相情况 | 钪萃取率/% | 铁萃取率/% |
1-1 | 1 | 分相快 | 90.76 | 15.82 |
1-2 | 2 | 分相容易 | 91.53 | 19.23 |
1-3 | 3 | 分相容易 | 92.98 | 13.56 |
1-4 | 4 | 有第三相 | 90.69 | 30.12 |
1-5 | 5 | 轻微乳化 | 91.74 | 39.79 |
料液温度对分离系数的影响如图:

(4)M经煅烧后可得到Al2O3,则M成分为
(5)为探究所得草酸钪晶体Sc2(C2O4)3·xH2O中结晶水的含量,取2.96g样品(纯度为75%),灼烧得到0.69gSc2O3固体,则x=
(6)草酸钪晶体在空气中灼烧分解反应方程式为
您最近一年使用:0次
解题方法
2 . 为探索工业含铝、铁、铜合金废料的再利用,某同学设计的回收利用方案如下:
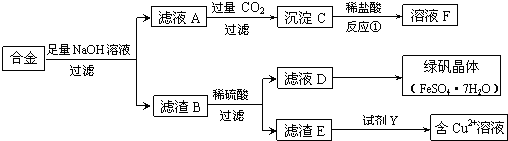
(1)合金与足量氢氧化钠溶液反应的离子方程式是____________________ 。
(2)若D中含有Fe3+,除去Fe3+的常用试剂____________________ 。
(3)若要从滤液D中得到绿矾晶体,必须进行的实验操作步骤:____________________ 、冷却结晶、过滤、自然干燥。
(4)若由滤渣E得到含Cu2+的溶液,试剂Y可能是____________________ (填选项字母)。
根据所选试剂写出一个由滤渣E得到含Cu2+溶液的化学方程式:____________________ 。

(1)合金与足量氢氧化钠溶液反应的离子方程式是
(2)若D中含有Fe3+,除去Fe3+的常用试剂
(3)若要从滤液D中得到绿矾晶体,必须进行的实验操作步骤:
(4)若由滤渣E得到含Cu2+的溶液,试剂Y可能是
| A.稀硝酸 | B.浓硫酸 | C.浓盐酸 | D.稀硫酸 |
根据所选试剂写出一个由滤渣E得到含Cu2+溶液的化学方程式:
您最近一年使用:0次
解题方法
3 . 从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取Al2O3的两种工艺流程如下:

请回答下列问题:
(1)流程甲加入盐酸后生成Fe3+的离子方程式为________________ ;
(2)铝土矿中固体A 是__________ (填化学式),写出沉淀F转化为氧化铝的化学方程式_____________ ;
(3)流程乙中,烧碱与Al2O3反应的离子方程式为________________________ ;
(4)固体X 是__________________ (填化学式)

请回答下列问题:
(1)流程甲加入盐酸后生成Fe3+的离子方程式为
(2)铝土矿中固体A 是
(3)流程乙中,烧碱与Al2O3反应的离子方程式为
(4)固体X 是
您最近一年使用:0次
2016-12-09更新
|
976次组卷
|
2卷引用:2015-2016学年广东省惠来一中、揭东一中高一上期末化学试卷



