解题方法
1 . 氯代叔丁烷(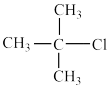 )常用于香料的合成,某实验小组设计了如下合成路线:
)常用于香料的合成,某实验小组设计了如下合成路线:
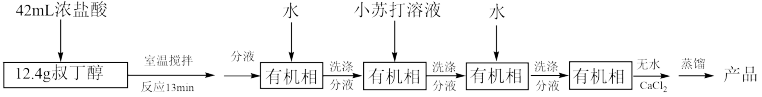
已知:
①部分试剂的性质见下表:
②反应原理: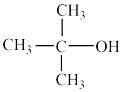 +HCl
+HCl
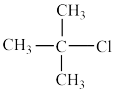 +H2O。
+H2O。
回答下列问题:
(1)浓盐酸和叔丁醇适宜在___________mL(填字母)的圆底烧瓶中进行反应。
(2)洗涤操作需要在分液漏斗中进行,使用分液漏斗前首先要___________ (填操作名称),小苏打溶液洗涤的目的是___________ ,每次洗涤后,静置,待分层后,分出有机层的操作为:打开分液漏斗上口玻璃塞,___________ 。
(3)用无水氯化钙处理有机相的目的是___________ ,某同学认为蒸馏之前,还需要进行过滤,请对该同学的观点进行评价:___________ 。
(4)本次实验氯代叔丁烷的实际产量为8g,则产率为___________ %(结果保留1位小数)。
 )常用于香料的合成,某实验小组设计了如下合成路线:
)常用于香料的合成,某实验小组设计了如下合成路线:
已知:
①部分试剂的性质见下表:
| 试剂 | 相对分子质量 | 密度( ) ) | 熔点(℃) | 沸点(℃) | 溶解性 |
| 叔丁醇 | 74 | 0.79 | 25 | 82.2 | 溶于水、乙醇 |
| 氯代叔丁烷 | 92.5 | 0.87 | -25.4 | 52 | 微溶于水、溶于乙醇 |
 +HCl
+HCl
 +H2O。
+H2O。回答下列问题:
(1)浓盐酸和叔丁醇适宜在___________mL(填字母)的圆底烧瓶中进行反应。
| A.50 | B.100 | C.250 | D.500 |
(3)用无水氯化钙处理有机相的目的是
(4)本次实验氯代叔丁烷的实际产量为8g,则产率为
您最近一年使用:0次
2023-06-11更新
|
32次组卷
|
2卷引用:甘肃省武威市民勤县等2地2022-2023学年高二下学期6月月考化学试题
2 . 化合物Ⅳ(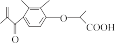 )是合成中药的一种中间体,以邻二甲苯为原料制备化合物Ⅳ的一种合成路线如图所示。下列说法错误的是
)是合成中药的一种中间体,以邻二甲苯为原料制备化合物Ⅳ的一种合成路线如图所示。下列说法错误的是
 )是合成中药的一种中间体,以邻二甲苯为原料制备化合物Ⅳ的一种合成路线如图所示。下列说法错误的是
)是合成中药的一种中间体,以邻二甲苯为原料制备化合物Ⅳ的一种合成路线如图所示。下列说法错误的是 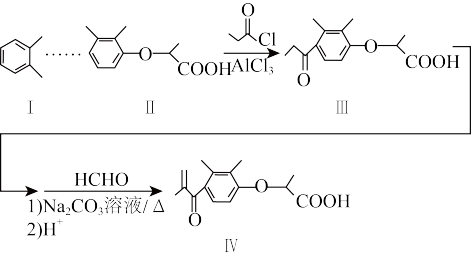
| A.由Ⅱ生成Ⅲ的反应类型为取代反应 | B.Ⅱ和Ⅳ均能使酸性高锰酸钾溶液褪色 |
C.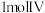 能与 能与 发生加成反应 发生加成反应 | D.I能从碘水中萃取碘,有机相在上层 |
您最近一年使用:0次
2022-04-13更新
|
1031次组卷
|
10卷引用:辽宁省沈阳市郊联体2022届高三下学期4月份线上考试化学试题
辽宁省沈阳市郊联体2022届高三下学期4月份线上考试化学试题(已下线)化学-2022年高考押题预测卷02(福建卷)(已下线)化学-2022年高考押题预测卷03(全国甲卷)(已下线)三轮冲刺卷2-【赢在高考黄金20卷】备战2022年高考化学模拟卷(辽宁专用)河北省部分重点中学2022届高三模拟化学试题江西省景德镇一中2021-2022学年高一下学期18班期末考化学试题湖南省衡阳市第一中学2022-2023学年高三下学期3月月考化学试题江苏省盐城市实验高级中学2022-2023学年高三下学期第三次模拟考试化学试题江苏省盐城市射阳中学2023-2024学年高二上学期1月期末化学试题重庆缙云教育联盟2024届高三高考第一次诊断性检测(一模) 化学试卷
名校
解题方法
3 . 物质a(环戊二烯)为原料制备物质d(金刚烷)的合成路线如图所示。

关于以上有机物的说法中正确的是

关于以上有机物的说法中正确的是
A.物质a的分子式为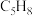 | B.b能萃取溴水中的溴单质,且上层有颜色 |
| C.物质c与物质d互为同分异构体 | D.物质d的一氯代物只有1种 |
您最近一年使用:0次
名校
解题方法
4 . 2021年9月28日,国务院新闻办公室发表《中国的全面小康》白皮书,宣布中国全面进入小康社会。化学学科正以独特学科价值为全面小康社会保驾护航。
I.屠呦呦制备青蒿素是高效的抗疟药。青蒿素为无色针状晶体,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差。已知:乙醚沸点为35℃,乙醚浸取法是从青蒿中提取青蒿素的方法。其主要工艺如图所示:
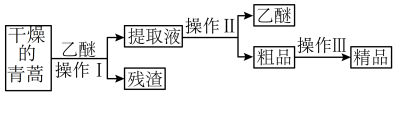
(1)乙醚浸取青蒿时,为增大青蒿素的浸出率,可采取的措施是_______ 。
(2)操作I需要的玻璃仪器主要有烧杯、玻璃棒、_______ ,操作II的名称是_______ 。
(3)操作III的主要过程可能是_______ (填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
II.我国正努力争取2060年前实现碳中和,用化学手段实现碳中和主要是对CO2进行捕获收集和资源化利用。
(4)利用低浓度氨水吸收烟气中CO2生成NH4HCO3,其化学方程式为_______ 。
(5)下列说法有利于实现碳中和的是_______ 。
A.积极鼓励植树造林,降低空气中CO2含量
B.研发利用二氧化碳合成淀粉的人工路线,实现CO2的资源化利用
C.开发可燃冰(CH4·nH2O)作为新的替代能源
I.屠呦呦制备青蒿素是高效的抗疟药。青蒿素为无色针状晶体,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差。已知:乙醚沸点为35℃,乙醚浸取法是从青蒿中提取青蒿素的方法。其主要工艺如图所示:

(1)乙醚浸取青蒿时,为增大青蒿素的浸出率,可采取的措施是
(2)操作I需要的玻璃仪器主要有烧杯、玻璃棒、
(3)操作III的主要过程可能是
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
II.我国正努力争取2060年前实现碳中和,用化学手段实现碳中和主要是对CO2进行捕获收集和资源化利用。
(4)利用低浓度氨水吸收烟气中CO2生成NH4HCO3,其化学方程式为
(5)下列说法有利于实现碳中和的是
A.积极鼓励植树造林,降低空气中CO2含量
B.研发利用二氧化碳合成淀粉的人工路线,实现CO2的资源化利用
C.开发可燃冰(CH4·nH2O)作为新的替代能源
您最近一年使用:0次
名校
解题方法
5 . 完成下列问题。
(1)有机化合物的官能团和空间结构与有机化合物的性质密切相关。
①下列物质中与乙烯互为同系物的是___________ (填字母)。
A. B.
B.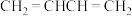
C.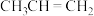 D.
D.
②下列物质与乙醇互为同分异构体的是___________ (填字母)。
A. B.
B.
C. D.
D.
③下列物质中所有原子在同一平面上的是___________ (填字母)。
A.乙烷 B.乙烯 C.四氯化碳 D.苯
④下列几组物质可以用分液法进行分离的是___________ (填字母)。
A.苯和水 B.乙酸和水 C.乙醇和水 D.四氯化碳和水
(2)用石油裂化和裂解过程中得到的乙烯、丙烯来合成丙烯酸乙酯的路线如下:
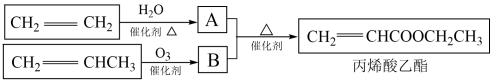
根据以上材料和所学的化学知识回答下列问题:
①分子B中所含官能团的名称为___________ 。
②由写出丙烯酸乙酯的分子式___________ 。
③ 制得有机化合物A的化学方程式为
制得有机化合物A的化学方程式为___________ ,反应类型是___________ 。
(1)有机化合物的官能团和空间结构与有机化合物的性质密切相关。
①下列物质中与乙烯互为同系物的是
A.
 B.
B.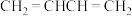
C.
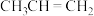 D.
D.
②下列物质与乙醇互为同分异构体的是
A.
 B.
B.
C.
 D.
D.
③下列物质中所有原子在同一平面上的是
A.乙烷 B.乙烯 C.四氯化碳 D.苯
④下列几组物质可以用分液法进行分离的是
A.苯和水 B.乙酸和水 C.乙醇和水 D.四氯化碳和水
(2)用石油裂化和裂解过程中得到的乙烯、丙烯来合成丙烯酸乙酯的路线如下:

根据以上材料和所学的化学知识回答下列问题:
①分子B中所含官能团的名称为
②由写出丙烯酸乙酯的分子式
③
 制得有机化合物A的化学方程式为
制得有机化合物A的化学方程式为
您最近一年使用:0次
名校
6 . 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
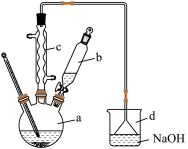
I.合成步骤:在a中加入15mL无水苯和少量铁屑。在b中小心加入5.0mL液溴。打开活塞,向a中滴入液溴,发生反应。
请回答下列问题:
(1)实验室制取溴苯的化学方程式为___________ 。
(2)反应过程中仪器a外壁温度升高,为提高原料利用率可利用温度计控制温度,适宜的温度范围为___________(填标号)。
(3)装置d的作用除了能防倒吸外,还有___________ 。
II.待反应完成后,取出a装置中的混合物,设计如下流程分离、提纯溴苯:
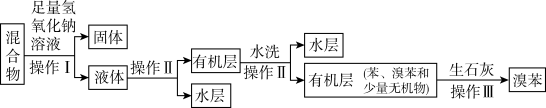
(4)流程中“固体”的化学式为___________ ,操作II所需主要玻璃仪器有___________ 。
(5)设计实验检验水洗是否达到目的:___________ 。
(6)若经过操作III后得纯溴苯11.30g.则溴苯的产率是___________ (计算结果保留2位有效数字)。

| 苯 | 溴 | 溴苯 | |
密度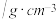 | 0.88 | 3.20 | 1.50 |
沸点/ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
请回答下列问题:
(1)实验室制取溴苯的化学方程式为
(2)反应过程中仪器a外壁温度升高,为提高原料利用率可利用温度计控制温度,适宜的温度范围为___________(填标号)。
A. | B. | C.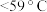 | D.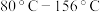 |
II.待反应完成后,取出a装置中的混合物,设计如下流程分离、提纯溴苯:

(4)流程中“固体”的化学式为
(5)设计实验检验水洗是否达到目的:
(6)若经过操作III后得纯溴苯11.30g.则溴苯的产率是
您最近一年使用:0次
解题方法
7 . 己二酸是一种重要的化工原料,科学家在现有工业路线基础上,提出了一条“绿色”合成路线:
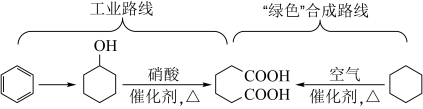
下列说法错误的是

下列说法错误的是
| A.分别向苯和环己烷中加入溴水,充分振荡后静置,上层溶液均呈橙红色 |
| B.环己醇分子中所有原子可能处于同一平面 |
| C.一定条件下,己二酸可以发生缩聚反应 |
| D.用饱和碳酸氢钠溶液可以鉴别环己醇和己二酸 |
您最近一年使用:0次
解题方法
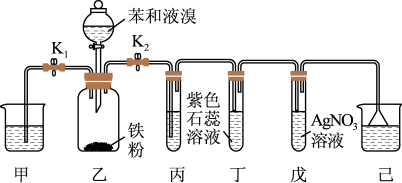
8 . 溴苯用途广泛,常用作溶剂、汽车燃料、有机合成原料、医药中间体等。溴苯由苯和溴反应制得,某化学兴趣小组设计了如图所示的装置研究溴苯的制备原理并检验产物。
已知:
请回答下列问题:
(1)装置乙中苯参与反应的化学方程式为_______ 。
(2)装置丙中应该盛装_______ (填试剂名称),当装置丁和戊中现象分别为_______ 、_______ 时,则说明该反应为取代反应;若撤去装置丙,_______ (填“能”或“不能”)说明该反应为取代反应。
(3)当反应结束后,为了让甲中的蒸馏水倒吸入乙中,需进行的操作是_______ 。
(4)取反应后的混合物,经过一系列操作得到纯净的溴苯:
①水洗,分液;
②用 稀溶液洗涤,除去
稀溶液洗涤,除去_______ ,分液;
③水洗,分液;
④用干燥剂干燥,过滤;
⑤_______ ,分离溴苯和苯。
(5)关于该实验,下列说法正确的是_______ (填标号)。
a.可用溴水代替液溴进行实验
b.装置己的作用是吸收尾气,防止污染空气
c.装置丁和戊中的导管可以插入溶液中
d.洗涤分液后,可用 干燥产物
干燥产物

已知:
| 苯 | 溴 | 溴苯 | |
| 沸点/℃ | 80 | 59 | 156 |
| 水溶性 | 微溶 | 微溶 | 微溶 |
(1)装置乙中苯参与反应的化学方程式为
(2)装置丙中应该盛装
(3)当反应结束后,为了让甲中的蒸馏水倒吸入乙中,需进行的操作是
(4)取反应后的混合物,经过一系列操作得到纯净的溴苯:
①水洗,分液;
②用
 稀溶液洗涤,除去
稀溶液洗涤,除去③水洗,分液;
④用干燥剂干燥,过滤;
⑤
(5)关于该实验,下列说法正确的是
a.可用溴水代替液溴进行实验
b.装置己的作用是吸收尾气,防止污染空气
c.装置丁和戊中的导管可以插入溶液中
d.洗涤分液后,可用
 干燥产物
干燥产物
您最近一年使用:0次
解题方法
9 . 碘是人体必不可少的一种微量元素,它是合成甲状腺激素必不可少的重要原料,缺乏碘会导致甲状腺肿大。为了从海带浸取液中提取碘,某同学设计了如下实验方案,下列有关说法正确的是
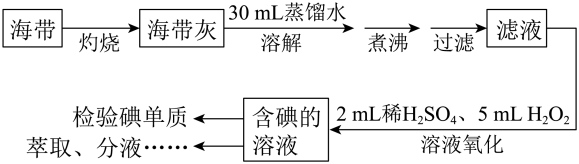

| A.灼烧过程中使用的仪器有酒精灯、蒸发皿、玻璃棒 |
| B.氧化过程中发生反应的离子方程式为2I-+H2O2=I2+2OH- |
| C.检验碘单质时,可选用淀粉,若淀粉变蓝说明海带中一定含有碘单质 |
| D.分液时,先打开分液漏斗活塞放出下层液体,再关闭活塞,从上口倒出上层液体 |
您最近一年使用:0次
10 . 稀土元素包括钪、钇和镧系共17种元素,是重要的战略资源,我国稀土资源丰富。从氟碳铈矿(主要化学成分为CeFCO3)提取铈族稀土元素的一种工艺流程如图:

已知:①焙烧后铈元素主要以CeO2形式存在,Ce(OH)3的Ksp=10×10-20
②Ce4+能与SO42-结合成[CeSO4]2+,Ce3+能被萃取剂HR萃取
(1)为提高原料的利用率,焙烧前应将矿石____ 处理。
(2)“浸取”过程中铈元素发生反应的离子方程式为___ 。
(3)“转化”过程中H2O2的作用是___ 。
(4)“萃取”过程中发生反应:Ce3+(水层)+3HR(有机层)⇌CeR3(有机层)+3H+(水层)设计“萃取”和“反萃取”操作的目的是___ ;HR应该具有的特点是____ 。
a.萃取剂HR的密度一定比水大
b.萃取剂HR不溶于水,也不和水反应
c.萃取剂HR和Ce3+不反应
d.Ce3+在萃取剂中溶解度大于水中
(5)“调节pH”时,为了使Ce3+完全沉淀(浓度小于1×10-5mol/L),溶液的pH应大于___ 。
(6)“氧化”操作得到产品的化学方程式为____ 。
(7)CeO2是汽车尾气净化器中的关键催化剂,能在还原性气氛中供氧,在氧化性气氛中耗氧,过程为:2CeO2⇌2CeO2-x+xO2↑(0≤x≤0.5)。写出CeO2消除CO的化学方程式____ 。

已知:①焙烧后铈元素主要以CeO2形式存在,Ce(OH)3的Ksp=10×10-20
②Ce4+能与SO42-结合成[CeSO4]2+,Ce3+能被萃取剂HR萃取
(1)为提高原料的利用率,焙烧前应将矿石
(2)“浸取”过程中铈元素发生反应的离子方程式为
(3)“转化”过程中H2O2的作用是
(4)“萃取”过程中发生反应:Ce3+(水层)+3HR(有机层)⇌CeR3(有机层)+3H+(水层)设计“萃取”和“反萃取”操作的目的是
a.萃取剂HR的密度一定比水大
b.萃取剂HR不溶于水,也不和水反应
c.萃取剂HR和Ce3+不反应
d.Ce3+在萃取剂中溶解度大于水中
(5)“调节pH”时,为了使Ce3+完全沉淀(浓度小于1×10-5mol/L),溶液的pH应大于
(6)“氧化”操作得到产品的化学方程式为
(7)CeO2是汽车尾气净化器中的关键催化剂,能在还原性气氛中供氧,在氧化性气氛中耗氧,过程为:2CeO2⇌2CeO2-x+xO2↑(0≤x≤0.5)。写出CeO2消除CO的化学方程式
您最近一年使用:0次



