解题方法
1 . 下列有关说法正确的是
| A.为了除去Na2CO3溶液中的NaHCO3,可滴加适量的稀盐酸 |
| B.为了除去NaHCO3固体中的Na2CO3,可通过加热除去 |
C.热稳定性: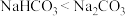 |
D.将某溶液与稀盐酸反应产生的气体通入澄清石灰水中,石灰水变浑浊,说明该溶液中含有CO |
您最近半年使用:0次
名校
2 . 某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:

已知:煅烧时,Cu2Te发生的反应为:Cu2Te+2O2→2CuO+TeO2
(1)在整个流程的反应中涉及到______ 种单质。
(2)煅烧时,Cr2O3发生反应的化学方程式为______ 。
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还含有______ (填化学式),写出生成TeOSO4的离子方程式______ 。
(4)“还原”步骤生成碲单质的离子方程式为______ ,得到的粗碲经洗涤后可以得到较为纯净的碲单质,检验碲单质是否洗涤干净的实验操作:______ 。

已知:煅烧时,Cu2Te发生的反应为:Cu2Te+2O2→2CuO+TeO2
(1)在整个流程的反应中涉及到
(2)煅烧时,Cr2O3发生反应的化学方程式为
(3)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还含有
(4)“还原”步骤生成碲单质的离子方程式为
您最近半年使用:0次
名校
解题方法
3 . 鉴别浓度均为0.1mol/L的Na2CO3、NH4Br、KI三种溶液,仅用下列一种方法不可行的是
| A.测定溶液pH | B.滴加0.1mol·L-1AgNO3溶液 |
| C.滴加0.1mol·L-1Ba(OH)2溶液 | D.滴加0.1mol·L-1AlCl3溶液 |
您最近半年使用:0次
名校
解题方法
4 . (一)某同学为研究浓硝酸与KSCN溶液的反应,进行如下实验:
资料: 能被氧化为(SCN)2,(SCN)2迅速聚合为红色的(SCN)x。
能被氧化为(SCN)2,(SCN)2迅速聚合为红色的(SCN)x。
(1)KSCN中,C、N元素的化合价分别为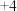 价和
价和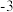 价,则S元素的化合价为
价,则S元素的化合价为_________ 。
(2)I中溶液立即变红是因为生成了__________________ (填化学式)。
(二)研究 的最终转化产物。
的最终转化产物。
(3)取少量Ⅱ中试管内的溶液,_________ (填操作和现象),证明 中S元素的转化产物是
中S元素的转化产物是 。
。
(4)经检验Ⅱ中“红棕色气体”含有 ,但不能说明
,但不能说明 一定是
一定是 中N元素的转化产物,原因是
中N元素的转化产物,原因是__________________ 。
将Ⅱ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量 溶液,不褪色。证明了红棕色气体中不含
溶液,不褪色。证明了红棕色气体中不含 。
。
(5)综合上述实验, 的最终转化产物中一定有
的最终转化产物中一定有__________________ 。
| 实验操作 | 实验现象 |
I.取1支试管,加入 浓硝酸,滴加5滴 浓硝酸,滴加5滴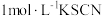 溶液 溶液 | 溶液立即变红 |
| Ⅱ.将试管静置一段时间 | 突然剧烈反应,红色迅速褪去,放出大量红棕色气体 |
Ⅲ.将Ⅱ中的气体通入 和 和 的混合溶液中 的混合溶液中 | 有白色沉淀生成 |
 能被氧化为(SCN)2,(SCN)2迅速聚合为红色的(SCN)x。
能被氧化为(SCN)2,(SCN)2迅速聚合为红色的(SCN)x。(1)KSCN中,C、N元素的化合价分别为
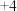 价和
价和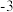 价,则S元素的化合价为
价,则S元素的化合价为(2)I中溶液立即变红是因为生成了
(二)研究
 的最终转化产物。
的最终转化产物。(3)取少量Ⅱ中试管内的溶液,
 中S元素的转化产物是
中S元素的转化产物是 。
。(4)经检验Ⅱ中“红棕色气体”含有
 ,但不能说明
,但不能说明 一定是
一定是 中N元素的转化产物,原因是
中N元素的转化产物,原因是将Ⅱ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量
 溶液,不褪色。证明了红棕色气体中不含
溶液,不褪色。证明了红棕色气体中不含 。
。(5)综合上述实验,
 的最终转化产物中一定有
的最终转化产物中一定有
您最近半年使用:0次
5 . 向稀硝酸酸化的某溶液滴加AgNO3溶液,有白色沉淀生成,则该溶液一定含有
| A.Na+ | B.Cl- | C.Al3+ | D.CO |
您最近半年使用:0次
名校
6 . 能够鉴定氯乙烷中氯元素的存在的操作是
| A.在氯乙烷中直接加入AgNO3溶液 |
| B.加蒸馏水,充分搅拌后,加入AgNO3溶液 |
| C.加入NaOH溶液,加热,然后加入AgNO3溶液 |
| D.加入热的NaOH醇溶液,充分反应后,加入稀硝酸酸化,再加入AgNO3溶液 |
您最近半年使用:0次
解题方法
7 . 铟(In)是制造半导体、电光源等的重要原料,广泛用于航空航天、光电信息、太阳能电池等领域。从铜冶炼过程中产生的铟砷烟灰(主要含有ZnO、PbO、Fe2O3、In2O3、As2O3、In2S3、SiO2)中提取铟的流程如图所示:
②“萃取”过程中萃取剂可用 H2A2表示,其在酸性溶液中可萃取三价金属离子。
③ln3+与Al3+相似,易水解。
请回答下列问题:
(1)滤渣的主要成分除SiO2外还有___________ (填化学式);“氧化酸浸”过程中,As2O3中的砷元素被氧化为最高价的含氧酸,写出此反应的离子方程式:___________ 。
(2)“还原铁”操作的目的是___________ 。
(3)萃取是化学实验中常用的分离方法,其操作过程为:检查分液漏斗是否漏液→加萃取剂和萃取液→振荡→___________ →静置→……
(4)“萃取”过程的离子方程式In3++3H2A2=In(HA2)3+3H+, 实验证明,在有机相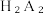 体积分数为55%、温度为25°C时,水相的 pH 对 ln3+萃取率的影响如图所示。结果表明,pH>2.1时, In³+ 萃取率快速下降,其原因是
体积分数为55%、温度为25°C时,水相的 pH 对 ln3+萃取率的影响如图所示。结果表明,pH>2.1时, In³+ 萃取率快速下降,其原因是___________ 。___________ g(用含a 的分数表示);“置换”后所得浊液需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已经洗涤干净的具体操作为 ___________ 。
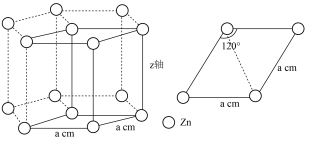
(6)锌是一种重要的金属,晶体结构属于六方晶系,其晶体结构、晶胞沿z轴的投影图如图所示,设Zn原子半径为r1nm,,晶胞边长为a cm,高为 h cm,则该晶体的空间利用率为___________ (列出计算式即可)。

②“萃取”过程中萃取剂可用 H2A2表示,其在酸性溶液中可萃取三价金属离子。
③ln3+与Al3+相似,易水解。
请回答下列问题:
(1)滤渣的主要成分除SiO2外还有
(2)“还原铁”操作的目的是
(3)萃取是化学实验中常用的分离方法,其操作过程为:检查分液漏斗是否漏液→加萃取剂和萃取液→振荡→
(4)“萃取”过程的离子方程式In3++3H2A2=In(HA2)3+3H+, 实验证明,在有机相
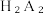 体积分数为55%、温度为25°C时,水相的 pH 对 ln3+萃取率的影响如图所示。结果表明,pH>2.1时, In³+ 萃取率快速下降,其原因是
体积分数为55%、温度为25°C时,水相的 pH 对 ln3+萃取率的影响如图所示。结果表明,pH>2.1时, In³+ 萃取率快速下降,其原因是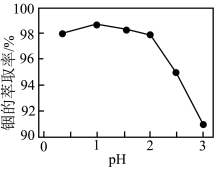
(6)锌是一种重要的金属,晶体结构属于六方晶系,其晶体结构、晶胞沿z轴的投影图如图所示,设Zn原子半径为r1nm,,晶胞边长为a cm,高为 h cm,则该晶体的空间利用率为
您最近半年使用:0次
2024-04-02更新
|
153次组卷
|
2卷引用:安徽省示范高中皖北协作区2024届高三联考化学试题
8 . 下列有关离子检验的操作及现象与结论之间对应关系正确的是
选项 | 操作及现象 | 结论 |
A | 向某溶液中加稀盐酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中含 |
B | 向某溶液中加入过量盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中含 |
C | 向某溶液中加入NaOH溶液,未产生能使红色石蕊试纸变蓝的气体 | 该溶液中一定不含 |
D | 向某溶液滴加稀硝酸酸化的 | 该溶液中含 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 下列实验操作及现象和结论不相符的是
操作及现象 | 结论 | |
A | 用醋酸浸泡水壶中的水垢,可将其清除 | 乙酸的酸性大于碳酸的酸性 |
B | 向某溶液中加入盐酸酸化的 | 该溶液中可能含有 |
C | 把一块绿豆大的钠放入滴有酚酞的水中,溶液变红 | 钠和水反应后溶液显碱性 |
D | 用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 | 溶液中有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 下列有关物质检验的操作、现象及结论均正确的是
选项 | 实验操作及现象 | 实验结论 |
A | 用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色 | 原溶液中一定有 无 无 |
B | 向某溶液中加入稀盐酸,产生无色无味气体,该气体能使澄清石灰水变浑浊 | 该溶液中一定含 |
C | 向新制氯水中加入稀硝酸酸化的 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 氯水中有 |
D | 某溶液中加入氯化钡,产生白色沉淀 | 溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次


 溶液,产生白色沉淀
溶液,产生白色沉淀

