1 . 甲、乙两同学欲验证乙醇的性质,现做如下实验:
Ⅰ.甲同学做乙醇的催化氧化实验并考查催化剂的催化机理,现设计了如下图所示的装置(夹持装置仪器已省略):
(1)M处乙醇参与反应的化学方程式为_______ 。
(2)从M管中可观察到红、黑交替现象。从中可认识到该实验过程中催化剂_______ (填“参加”或“不参加”)化学反应,还可以认识到催化剂起催化作用需要一定的_______ 。
(3)用银氨溶液可以检验F中的产物,写出配置银氨溶液的过程:_______ (必须用到的试剂:2%的 溶液,2%的稀氨水)
溶液,2%的稀氨水)
Ⅱ.乙同学采用如图装置以乙醇为原料制备乙烯并研究乙烯与溴水的反应。_______ 。
(5)除杂试剂A为_______ 。
(6)实验观察到溴水褪色,得到无色透明的溶液。进一步分析发现反应产物主要为 ,含少量
,含少量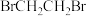 。乙烯与溴水反应后的溶液呈
。乙烯与溴水反应后的溶液呈_______ (填“中性”、“碱性”或“酸性”)。
Ⅰ.甲同学做乙醇的催化氧化实验并考查催化剂的催化机理,现设计了如下图所示的装置(夹持装置仪器已省略):

(1)M处乙醇参与反应的化学方程式为
(2)从M管中可观察到红、黑交替现象。从中可认识到该实验过程中催化剂
(3)用银氨溶液可以检验F中的产物,写出配置银氨溶液的过程:
 溶液,2%的稀氨水)
溶液,2%的稀氨水) Ⅱ.乙同学采用如图装置以乙醇为原料制备乙烯并研究乙烯与溴水的反应。

(5)除杂试剂A为
(6)实验观察到溴水褪色,得到无色透明的溶液。进一步分析发现反应产物主要为
 ,含少量
,含少量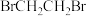 。乙烯与溴水反应后的溶液呈
。乙烯与溴水反应后的溶液呈
您最近一年使用:0次
名校
2 . 探究硫元素单质及其化合物的性质,下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A | SO2是否具有漂白性 | 将SO2通入酸性KMnO4溶液中,溶液褪色 |
| B | SO2是否具有氧化性 | 将SO2通入Na2S溶液中,产生淡黄色沉淀 |
| C | Na2SO3溶液是否变质 | 向Na2SO3溶液中加入盐酸酸化的Ba(NO3)2溶液,产生白色沉淀 |
| D | S与C的非金属性强弱 | 将SO2通入饱和NaHCO3溶液中,产生使澄清石灰水变浑浊的气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 依据下列实验得出的结论正确的是

| A.常温下,在水中苯酚的溶解度大于苯酚钠的溶解度 |
| B.酸性:乙酸>碳酸>苯酚 |
C.实验1用 溶液替代NaOH溶液现象相同 溶液替代NaOH溶液现象相同 |
D.向实验1变澄清的溶液中通入过量的 ,无明显现象 ,无明显现象 |
您最近一年使用:0次
2023-06-29更新
|
168次组卷
|
3卷引用:江苏省常州市北郊高级中学2023-2024学年高二下学期期中考试化学试题
江苏省常州市北郊高级中学2023-2024学年高二下学期期中考试化学试题江西省抚州市2022-2023学年高二下学期学生学业质量监测化学试题 (已下线)专题03 烃的衍生物-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)
解题方法
4 . 常温下 与
与 反应能生成
反应能生成 和
和 。实验室探究
。实验室探究 与
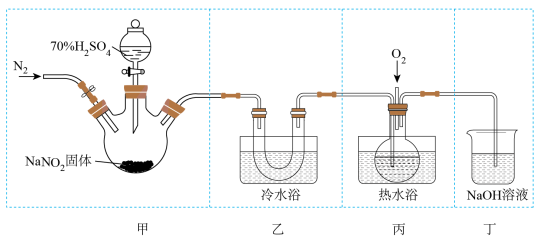
与 反应及气体产物的成分。下列实验装置和操作不能达到实验目的的是
反应及气体产物的成分。下列实验装置和操作不能达到实验目的的是
 与
与 反应能生成
反应能生成 和
和 。实验室探究
。实验室探究 与
与 反应及气体产物的成分。下列实验装置和操作不能达到实验目的的是
反应及气体产物的成分。下列实验装置和操作不能达到实验目的的是
| A.用装置甲制取气体 | B.用装置乙收集生成的 |
C.用装置丙检验 生成 生成 | D.蒸发丁中所得溶液得到纯净 晶体 晶体 |
您最近一年使用:0次
5 . 室温下,下列关于铁化合物的实验探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向 和 和 的混合溶液中滴入酸化的 的混合溶液中滴入酸化的 溶液振荡,观察溶液颜色的变化 溶液振荡,观察溶液颜色的变化 | 比较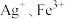 氧化性的强弱 氧化性的强弱 |
| B | 用 还原 还原 ,所得到的产物中加入稀盐酸,滴加 ,所得到的产物中加入稀盐酸,滴加 溶液,观察颜色变化 溶液,观察颜色变化 |  是否已全部被还原 是否已全部被还原 |
| C | 向 溶液中加入几滴氯水,振荡,再加 溶液中加入几滴氯水,振荡,再加 萃取,观察 萃取,观察 层颜色变化 层颜色变化 | 比较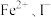 还原性的强弱 还原性的强弱 |
| D | 将铁锈溶于浓盐酸中再向溶液中滴入几滴 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 | 铁锈中是否含有二价铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 实验室用如下图所示装置探究 与
与 溶液的反应(实验前先通入
溶液的反应(实验前先通入 排除装置中的空气)。下列说法不正确的是
排除装置中的空气)。下列说法不正确的是
 与
与 溶液的反应(实验前先通入
溶液的反应(实验前先通入 排除装置中的空气)。下列说法不正确的是
排除装置中的空气)。下列说法不正确的是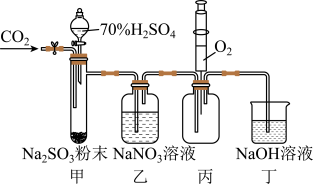
A.用装置甲产生 |
B.装置乙中无明显现象,则 与 与 未发生反应 未发生反应 |
C.装置丙中注入 ,产生红棕色气体,说明装置乙中 ,产生红棕色气体,说明装置乙中 发生了氧化反应 发生了氧化反应 |
| D.装置丁吸收尾气并防止空气进入装置丙 |
您最近一年使用:0次
2023-03-23更新
|
1382次组卷
|
7卷引用:江苏省南京市六校联合体2023-2024学年高二上学期期末调研测试化学试卷
名校
7 . 用如图所示实验装置进行相应实验,能达到实验目的的是
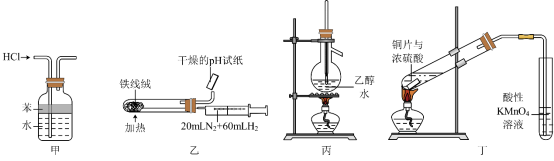

| A.装置甲吸收HCl气体,并防止液体倒吸 |
| B.装置乙合成氨并检验氨的存在 |
| C.装置丙实验室分离乙醇和水(部分装置已省略) |
| D.装置丁验证铜片与浓硫酸反应生成SO2 |
您最近一年使用:0次
2022-10-19更新
|
154次组卷
|
2卷引用:江苏省响水中学2022-2023学年高二下学期期中考试化学(创新班)试题
8 . 某化学实验小组对CO还原CuO的固体产物进行探究,装置如下图所示。
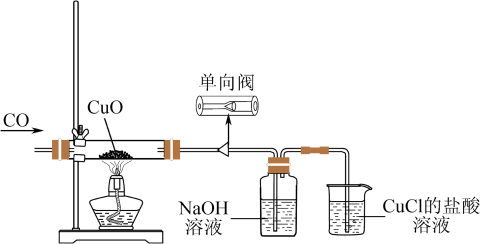
查阅资料:
I.CO还原CuO的温度需要控制在500℃以上;
II.CuO在高温下可分解生成红色Cu2O。
(1)CO还原CuO制得Cu的化学方程式是_______ 。
(2)单向阀的作用是_______ 。
(3)尾气通入CuCl盐酸溶液的目的是_______ 。
(4)为探究还原后的红色固体产物Cu中是否含有Cu2O,设计方案如下:
步骤1:准确称取1.50g固体产物,加适当过量的稀硫酸和双氧水使固体全部溶解,此时固体产物中的铜元素完全转化为Cu2+。
步骤2:微热,除去过量的过氧化氢,加水稀释成250.00mL溶液。
步骤3:取25.00mL溶液于锥形瓶中,加入适当过量的KI溶液,滴加少量淀粉溶液,再滴加0.1000mol·L-1Na2S2O3溶液,恰好完全反应时,消耗Na2S2O3溶液的体积为23.00mL。
已知:①2Cu2++4I-=2CuI↓+I2;②2 +I2=
+I2= +2I-。
+2I-。
通过计算数据判断固体产物中是否含有Cu2O_______ (写出计算过程)。

查阅资料:
I.CO还原CuO的温度需要控制在500℃以上;
II.CuO在高温下可分解生成红色Cu2O。
(1)CO还原CuO制得Cu的化学方程式是
(2)单向阀的作用是
(3)尾气通入CuCl盐酸溶液的目的是
(4)为探究还原后的红色固体产物Cu中是否含有Cu2O,设计方案如下:
步骤1:准确称取1.50g固体产物,加适当过量的稀硫酸和双氧水使固体全部溶解,此时固体产物中的铜元素完全转化为Cu2+。
步骤2:微热,除去过量的过氧化氢,加水稀释成250.00mL溶液。
步骤3:取25.00mL溶液于锥形瓶中,加入适当过量的KI溶液,滴加少量淀粉溶液,再滴加0.1000mol·L-1Na2S2O3溶液,恰好完全反应时,消耗Na2S2O3溶液的体积为23.00mL。
已知:①2Cu2++4I-=2CuI↓+I2;②2
 +I2=
+I2= +2I-。
+2I-。通过计算数据判断固体产物中是否含有Cu2O
您最近一年使用:0次
2022-09-02更新
|
82次组卷
|
2卷引用:江苏省扬州市2021-2022学年高二上学期1月学业水平合格性模拟考试化学试题
9 .  发生催化氧化反应生成
发生催化氧化反应生成 ,强碱条件下能被
,强碱条件下能被 氧化生成
氧化生成 ;
; 可被
可被 继续氧化生成
继续氧化生成 ,也可被
,也可被 氧化生成
氧化生成 ,
, 能与
能与 溶液反应产生银镜;
溶液反应产生银镜; 是一种弱酸,酸性与醋酸相当。下列有关含氮化合物的性质与制备说法正确的是
是一种弱酸,酸性与醋酸相当。下列有关含氮化合物的性质与制备说法正确的是
 发生催化氧化反应生成
发生催化氧化反应生成 ,强碱条件下能被
,强碱条件下能被 氧化生成
氧化生成 ;
; 可被
可被 继续氧化生成
继续氧化生成 ,也可被
,也可被 氧化生成
氧化生成 ,
, 能与
能与 溶液反应产生银镜;
溶液反应产生银镜; 是一种弱酸,酸性与醋酸相当。下列有关含氮化合物的性质与制备说法正确的是
是一种弱酸,酸性与醋酸相当。下列有关含氮化合物的性质与制备说法正确的是A.分析结构可推得, 难溶于水 难溶于水 |
B.分析结构可推得,相同条件下 还原性应强于 还原性应强于 |
C.制备 时应将 时应将 慢慢通入 慢慢通入 溶液中 溶液中 |
D.可向 溶液中通 溶液中通 来制备 来制备 |
您最近一年使用:0次
2022-08-04更新
|
703次组卷
|
3卷引用:江苏省泰州中学2022-2023学年高二5月检测化学试题
10 .  是一种重要的杀菌消毒剂,也是一种烟气(主要含
是一种重要的杀菌消毒剂,也是一种烟气(主要含 、
、 )脱硫脱硝的吸收剂。已知:
)脱硫脱硝的吸收剂。已知: 溶液呈碱性;随溶液
溶液呈碱性;随溶液 增大,
增大, 氧化性降低;生产成本随着
氧化性降低;生产成本随着 的浓度增大明显增加。
的浓度增大明显增加。
(1)① 和
和 反应可制得
反应可制得 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。
② 和
和 按一定比例与
按一定比例与 溶液反应也可制得
溶液反应也可制得 ,理论上
,理论上 与
与 完全反应的物质的量之比为
完全反应的物质的量之比为_______ 。
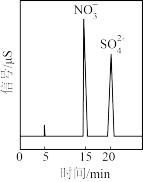
③在反应釜中用 吸收烟气,所得产物的离子色谱如下图所示。写出
吸收烟气,所得产物的离子色谱如下图所示。写出 溶液在脱硫过程中的离子方程式
溶液在脱硫过程中的离子方程式_______ 。
(2) 浓度对脱除效率的影响如下图所示。
浓度对脱除效率的影响如下图所示。
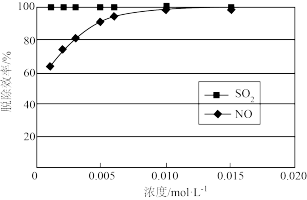
①综合考虑脱除效率和生产成本,选用 溶液浓度为
溶液浓度为_______ 。
②相对于 ,
, 更难脱除,可能的原因是
更难脱除,可能的原因是_______ 。
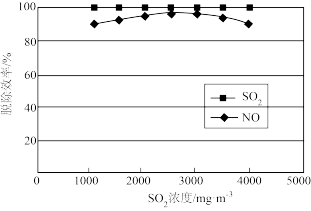
(3)烟气中 含量对脱硝的影响如下图所示,在
含量对脱硝的影响如下图所示,在 浓度小于
浓度小于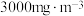 时,
时, 的浓度增大,脱硝效率提高,可能的原因是
的浓度增大,脱硝效率提高,可能的原因是_______ 。
 是一种重要的杀菌消毒剂,也是一种烟气(主要含
是一种重要的杀菌消毒剂,也是一种烟气(主要含 、
、 )脱硫脱硝的吸收剂。已知:
)脱硫脱硝的吸收剂。已知: 溶液呈碱性;随溶液
溶液呈碱性;随溶液 增大,
增大, 氧化性降低;生产成本随着
氧化性降低;生产成本随着 的浓度增大明显增加。
的浓度增大明显增加。(1)①
 和
和 反应可制得
反应可制得 ,写出该反应的化学方程式
,写出该反应的化学方程式②
 和
和 按一定比例与
按一定比例与 溶液反应也可制得
溶液反应也可制得 ,理论上
,理论上 与
与 完全反应的物质的量之比为
完全反应的物质的量之比为③在反应釜中用
 吸收烟气,所得产物的离子色谱如下图所示。写出
吸收烟气,所得产物的离子色谱如下图所示。写出 溶液在脱硫过程中的离子方程式
溶液在脱硫过程中的离子方程式
(2)
 浓度对脱除效率的影响如下图所示。
浓度对脱除效率的影响如下图所示。
①综合考虑脱除效率和生产成本,选用
 溶液浓度为
溶液浓度为②相对于
 ,
, 更难脱除,可能的原因是
更难脱除,可能的原因是(3)烟气中
 含量对脱硝的影响如下图所示,在
含量对脱硝的影响如下图所示,在 浓度小于
浓度小于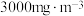 时,
时, 的浓度增大,脱硝效率提高,可能的原因是
的浓度增大,脱硝效率提高,可能的原因是
您最近一年使用:0次



