1 . 亚硝酸钠(NaNO2)主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用NOx制备亚硝酸钠,简易流程如图。
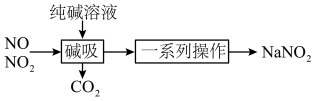
已知:NO2 + NO+ Na2CO3=2NaNO2 + CO2,2NO2 + Na2CO3= NaNO2 + NaNO3 +CO2。

(1)N2的结构式为___________ ;利用饱和NH4Cl溶液和饱和NaNO2溶液在加热条件下反应可制得N2,该反应的化学方程式为___________ 。
(2)装置C中盛装饱和Na2CO3溶液的仪器的名称是___________ ;NO不能单独被纯碱溶液吸收,为了使NOx完全被碱液吸收且产品纯度高,x=___________ 。
(3)装置D的作用是___________ ,采用“倒置漏斗”措施的目的是___________ 。
(4)实验完毕后,从装置C中分离出NaNO2固体产品(不含Na2CO3杂质)。设计实验探究NaNO2的性质。取少量NaNO2固体产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
上述实验___________ (填标号 )的结论不可靠,理由是___________ 。以上经实验测得实验丙反应后的溶液中氮元素仅以 的形式存在,酸性KMnO4溶液与
的形式存在,酸性KMnO4溶液与 反应的离子方程式为
反应的离子方程式为___________ 。
(5)吸光光度法是借助分光光度计测定溶液的吸光度,根据朗伯一比耳定律确定物质溶液的浓度。亚硝酸钠标准曲线数据如表所示。(已知:稀溶液的吸光度与浓度成正比)
取0.001gNaNO2样品溶于蒸馏水配成1000mL稀溶液,取4.00mL该稀溶液测得吸光度为2.7000,对比标准曲线数据可知,该亚硝酸钠产品纯度为___________ (结果保留三位有效数字,已知1 μg=10-6 g)。

已知:NO2 + NO+ Na2CO3=2NaNO2 + CO2,2NO2 + Na2CO3= NaNO2 + NaNO3 +CO2。

(1)N2的结构式为
(2)装置C中盛装饱和Na2CO3溶液的仪器的名称是
(3)装置D的作用是
(4)实验完毕后,从装置C中分离出NaNO2固体产品(不含Na2CO3杂质)。设计实验探究NaNO2的性质。取少量NaNO2固体产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
| 实验 | 实验操作及现象 | 结论 |
| 甲 | 滴入无色酚酞溶液中,无色酚酞溶液变红 | HNO2是弱酸 |
| 乙 | 滴入少量酸性KI-淀粉溶液中,振荡,酸性KI-淀粉溶液变蓝 | 酸性条件下,  具有氧化性 具有氧化性 |
| 丙 | 滴入少量酸性KMnO4溶液中,振荡,酸性KMnO4溶液褪色 | 酸性条件下 ,  具有还原性 具有还原性 |
 的形式存在,酸性KMnO4溶液与
的形式存在,酸性KMnO4溶液与 反应的离子方程式为
反应的离子方程式为(5)吸光光度法是借助分光光度计测定溶液的吸光度,根据朗伯一比耳定律确定物质溶液的浓度。亚硝酸钠标准曲线数据如表所示。(已知:稀溶液的吸光度与浓度成正比)
| 标准使用液浓度/(μg·mL−1) | 取标准液体积/mL | 相当于亚硝酸钠的质量/μg | 吸光度A |
| 1 | 4 | 4 | 2.7045 |
您最近一年使用:0次
解题方法
2 . 某化学兴趣小组制取SO2并探究SO2与FeCl3溶液的反应,所用装置如图所示。下列说法错误的是
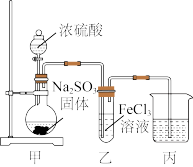

| A.甲中浓硫酸浓度不宜过大,以防止氧化亚硫酸钠 |
| B.乙中反应的氧化剂与还原剂物质的量之比为2:1 |
| C.为尽快观察到乙中的实验现象,可增大FeCl3溶液浓度或加热 |
| D.丙装置的作用是吸收剩余的SO2,防止污染空气,但是应该连接倒扣漏斗 |
您最近一年使用:0次
名校
解题方法
3 . 铜与浓硫酸反应的装置如图所示。下列描述合理的是
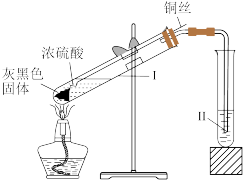

| A.反应过程中,试管Ⅰ中出现灰黑色固体是Cu2O |
| B.反应结束后,为观察溶液颜色需向试管Ⅰ中加入水 |
| C.若试管Ⅱ盛放紫色石蕊溶液,可观察到溶液由紫色褪为无色 |
| D.为验证气体产物具有还原性,试管Ⅱ盛放酸性KMnO4溶液 |
您最近一年使用:0次
2021-04-05更新
|
491次组卷
|
5卷引用:陕西省咸阳市2021届高三第二次模拟考试理综化学试题
陕西省咸阳市2021届高三第二次模拟考试理综化学试题(已下线)第13讲 硫及其化合物(精练)-2022年高考化学一轮复习讲练测(已下线)专题12 硫及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练江苏省苏州市第三中学校2022-2023学年高一上学期12月采点评价考试化学试题广东省江门市某校2023-2024学年高一下学期第一次质量检测化学试题
4 . 下列依据实验方案和现象对浓硫酸性质做出的判断合理的是
| 实验方案 | 实验I: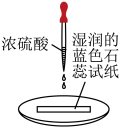 | 实验II: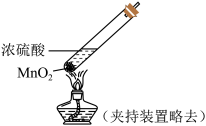 |
| 实验现象 | 试纸中心区域变黑,边缘变红 | 黑色固体溶解,溶液接近无色(溶液中锰元素仅以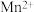 存在),产生能使带火星的木条复燃的无色气体 存在),产生能使带火星的木条复燃的无色气体 |
| A.由I可知,浓硫酸具有脱水性 | B.由I可知,浓硫酸具有弱酸性 |
| C.由II可知,浓硫酸具有强氧化性 | D.由II可知,浓硫酸具有吸水性 |
您最近一年使用:0次
2020-06-07更新
|
978次组卷
|
12卷引用:陕西省榆林市第十中学2020-2021学年高三上学期期中考试化学试题
陕西省榆林市第十中学2020-2021学年高三上学期期中考试化学试题北京市海淀区2020届高三二模化学试题湖北省黄冈市麻城市实验高级中学2020届高三模拟(五)考试理综化学试题(已下线)第11讲 硫及其化合物-2021年高考化学一轮复习名师精讲练山西省太原市2021届高三上学期期末考试化学试题山西省晋城市2021届高三上学期期末考试化学试题山西省长治市2021届高三上学期期末考试化学试题山东省聊城市2021-2022学年下学期高三一模化学试题北京市中国人民大学附属中学2023-2024学年高三下学期一模模拟化学试题北京市第十二中学2021-2022学年高一下学期6月月考化学试题北京十二中2021-2022学年高一下学期六月月考(等级考)化学试题新疆生产建设兵团第一师高级中学2022-2023学年高一下学期3月月考化学试题
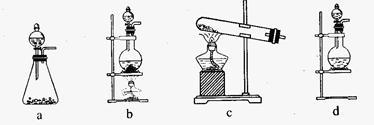
5 . 某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4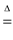 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
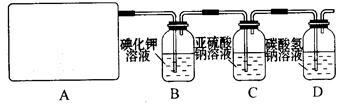
试回答:
(1)该实验中A部分的装置是_________ (填写装置的序号)。
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
___________________________________________________________________ 。
(3)写出D装置中发生反应的离子方程式______________________________________ 。
(4)该实验存在明显的缺陷,请你提出改进的方法_______________________________ 。
 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
试回答:
(1)该实验中A部分的装置是

(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
(3)写出D装置中发生反应的离子方程式
(4)该实验存在明显的缺陷,请你提出改进的方法
您最近一年使用:0次



