解题方法
1 . (1)如图甲所示,在平底烧瓶底部有一块钠,剩余空间充有干燥的空气。一段时间后可观察到银白色的钠变暗,发生反应的化学方程式为__________________________________________ 。
(2)如图乙,先用弹簧夹夹住橡胶管,点燃钠(足量),迅速伸入瓶中并塞上瓶塞,发生反应的化学方程式为_________________________________ ,生成物的颜色是_______________ ,待反应完全并冷却至原温度后,打开弹簧夹,则广口瓶内流入的水的体积约占瓶内原有空气体积的________________ (假设装置的气密性良好且操作正确,生成物与水不接触)。
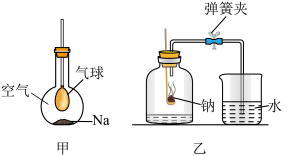
(2)如图乙,先用弹簧夹夹住橡胶管,点燃钠(足量),迅速伸入瓶中并塞上瓶塞,发生反应的化学方程式为

您最近一年使用:0次
2020-10-01更新
|
313次组卷
|
2卷引用:人教版(2019)高一必修第一册 第二章 海水中的重要元素 第一节 钠及其化合物 方法帮
解题方法
2 . 如图所示装置,持续通入气体X,可看到a处有红色物质生成,假设各步均反应完全,回答下列问题:
已知: 能还原CuO生成Cu。
能还原CuO生成Cu。
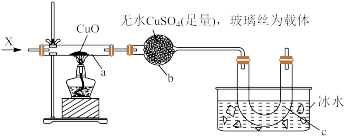
(1)若X为 ,反应前需要先通入
,反应前需要先通入 ,其目的是
,其目的是__________ 。
(2)若X为 ,a处的反应方程式为
,a处的反应方程式为____________ ,b处现象为___________ 。
(3)若X为乙醇蒸气,a处的反应方程式为___________ ;c处收集到的液体有刺激性气味,该液体物质的官能团为_________________ 。
已知:
 能还原CuO生成Cu。
能还原CuO生成Cu。
(1)若X为
 ,反应前需要先通入
,反应前需要先通入 ,其目的是
,其目的是(2)若X为
 ,a处的反应方程式为
,a处的反应方程式为(3)若X为乙醇蒸气,a处的反应方程式为
您最近一年使用:0次
解题方法
3 . 羟基是重要的官能团,某化学小组以①碳酸、②乙醇、③乙酸3种物质的溶液作为研究对象,比较不同物质的羟基中氢原子的活泼性。甲同学设计并实施了如下实验方案:
序号 | 实验操作 | 实现现象 | 结论及解释 |
I | 分别取3种溶液,滴加紫色石蕊试液 | 溶液变红的是①③溶液 | |
II | 向含酚酞的NaOH溶液中,各滴加等量的②③两种溶液 | ②中无明显现象,③中红色明显变浅 | 滴加③溶液时反应的化学方程式: |
III | 将 溶液加入 溶液加入 溶液中 溶液中 | 有无色气泡冒出 | 反应的化学方程式: |
| 结论:3种物质羟基中氢原子的活泼性由强到弱的顺序(填序号): | |||
您最近一年使用:0次
4 . 化学兴趣小组的同学们设计了如图装置验证乙醇催化氧化的产物(加热仪器、夹持装置已略去)。
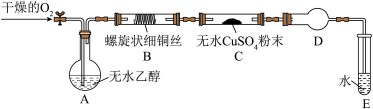
已知:乙醇的沸点为78℃,易溶于水;乙醛的沸点为20.8℃,易溶于水。
(1)乙醇催化氧化反应的化学方程式是________ 。
(2)实验时上述装置中需要加热的是_______ (填序号,下同),其中应该先加热的是____ ,为使装置A中的乙醇成为蒸气,最简单的加热方法是______ 。
(3)实验室制取氧气的化学方程式是________ 。
(4)实验开始后,装置B中能观察到的现象是______ ;装置C中能观察到的现象是______ ,由此得出的结论是_______ 。
(5)装置E的作用是_______ ,能初步判定反应后有乙醛生成的依据是________ 。
(6)装置D中的药品是______ ,其作用是_______ 。

已知:乙醇的沸点为78℃,易溶于水;乙醛的沸点为20.8℃,易溶于水。
(1)乙醇催化氧化反应的化学方程式是
(2)实验时上述装置中需要加热的是
(3)实验室制取氧气的化学方程式是
(4)实验开始后,装置B中能观察到的现象是
(5)装置E的作用是
(6)装置D中的药品是
您最近一年使用:0次
5 . 在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管中,装置如图所示。
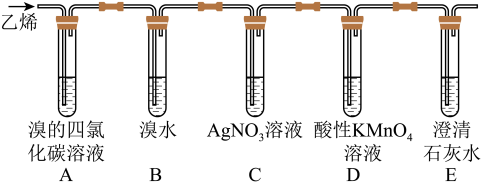
根据上述装置,回答下列问题:
(1)C装置的作用是___ 。
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。预测:
A装置中的现象是__ ,B装置中的现象是___ 。分离A装置中产物的操作名称是___ ,分离B装置中产物需要的玻璃仪器名称是___ 。
(3)D装置中溶液由紫色变为无色,发生反应的反应类型为___ 。E装置的作用是___ ,当观察到___ 的现象时能验证E装置的功能。
(4)写出A装置中发生反应的化学方程式:___ ,反应类型为___ 。教材中用溴的四氯化碳溶液替代溴水与乙烯反应,其目的是___ 。
(5)做乙烯燃烧实验之前必须进行的操作是___ ,燃烧实验中可能观察到的现象是__ 。

根据上述装置,回答下列问题:
(1)C装置的作用是
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。预测:
A装置中的现象是
(3)D装置中溶液由紫色变为无色,发生反应的反应类型为
(4)写出A装置中发生反应的化学方程式:
(5)做乙烯燃烧实验之前必须进行的操作是
您最近一年使用:0次
6 . 某同学在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题。
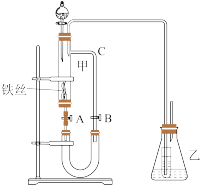
(1)第一步,在分液漏斗中依次加入10mL苯和5mL液溴,使之混合均匀,此时观察到溴溶于苯,不反应,溶液呈红棕色。
第二步,关闭胶皮管夹A和B,打开分液漏斗活塞,将苯、溴的混合液按一定速率逐滴滴加到玻璃管甲中的铁丝上,观察到的现象是_______________ ;从上述两步实验观察到的现象的差异可得出的结论是___________________ 。
(2)第三步,几分钟后,打开胶皮管夹A和B,使反应混合液流入U形管中,打开胶皮管夹B的原因是___________ ;然后通过分液漏斗向U形管中加入适量的氢氧化钠溶液,目的是___________________ 。
(3)第四步,关闭胶皮管夹A和B,连同胶皮管夹A和B一起取下U形管,用力振荡并静置后,观察到溴苯的颜色是__________ ,它在U形管中液体的__________ (填“上”或“下”)层,此步关闭胶皮管夹A和B的目的是______________________________ 。
(4)要证明上述溴与苯的反应是取代反应而不是加成反应,则装置乙中:小试管内的液体是_________ (填名称,下同),作用是____________ ;锥形瓶内的液体是__________ ,作用是____________________ ;反应后,向锥形瓶内滴加__________ 溶液,作用是___________ ;此外,装置乙的作用还有___________ 。

(1)第一步,在分液漏斗中依次加入10mL苯和5mL液溴,使之混合均匀,此时观察到溴溶于苯,不反应,溶液呈红棕色。
第二步,关闭胶皮管夹A和B,打开分液漏斗活塞,将苯、溴的混合液按一定速率逐滴滴加到玻璃管甲中的铁丝上,观察到的现象是
(2)第三步,几分钟后,打开胶皮管夹A和B,使反应混合液流入U形管中,打开胶皮管夹B的原因是
(3)第四步,关闭胶皮管夹A和B,连同胶皮管夹A和B一起取下U形管,用力振荡并静置后,观察到溴苯的颜色是
(4)要证明上述溴与苯的反应是取代反应而不是加成反应,则装置乙中:小试管内的液体是
您最近一年使用:0次
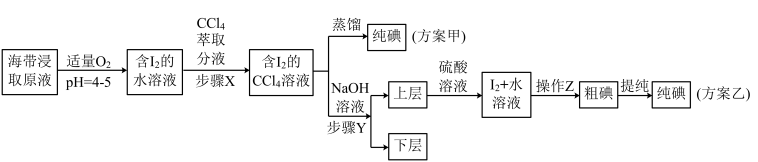
7 . 某学习小组按如图所示的甲、乙两种实验方案制备碘:
已知: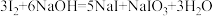 。
。
请回答下列问题:
(1)分液漏斗使用前须检漏,检漏方法为_____________ 。
(2)步骤X中,萃取后分液漏斗内观察到的现象是_________ 。
(3)下列有关步骤Y的说法,正确的是_____ (填标号,双选)。
A 应控制NaOH溶液的浓度和体积
B 将碘转化成离子进入水层
C 主要是除去海带浸取原液中的有机杂质
D NaOH溶液可以由乙醇代替
(4)操作Z的名称是_______ 。
(5)方案甲中采用蒸馏不合理,理由是_____________ 。

已知:
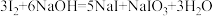 。
。请回答下列问题:
(1)分液漏斗使用前须检漏,检漏方法为
(2)步骤X中,萃取后分液漏斗内观察到的现象是
(3)下列有关步骤Y的说法,正确的是
A 应控制NaOH溶液的浓度和体积
B 将碘转化成离子进入水层
C 主要是除去海带浸取原液中的有机杂质
D NaOH溶液可以由乙醇代替
(4)操作Z的名称是
(5)方案甲中采用蒸馏不合理,理由是
您最近一年使用:0次
2020-09-24更新
|
232次组卷
|
2卷引用:鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律微项目 海带提碘与海水提溴
8 . 某同学想通过比较硫和碳的最高价氧化物对应的水化物的酸性强弱来验证硫与碳的得电子能力的强弱,他采用了如图所示的装置。

请回答下列问题:
(1)仪器a的名称是________________ ,应盛放下列药品中的________ (填标号)。
A 稀硫酸 B 亚硫酸 C 氢硫酸 D 盐酸
(2)仪器b的名称是________________ ,应盛放下列药品中的________ (填标号)。
A 硫酸钙 B 硫酸钠 C 氯化钠 D 碳酸钠
(3)仪器c中应盛放的药品是_________ ,如果看到的现象是_________ ,即可证明________ 比________ 酸性强,得电子能力____ 比________ 强,b中发生反应的化学方程式为________ 。

请回答下列问题:
(1)仪器a的名称是
A 稀硫酸 B 亚硫酸 C 氢硫酸 D 盐酸
(2)仪器b的名称是
A 硫酸钙 B 硫酸钠 C 氯化钠 D 碳酸钠
(3)仪器c中应盛放的药品是
您最近一年使用:0次
9 . 某研究小组为探究 和
和 溶液的反应实质,设计了如图所示装置进行实验。
溶液的反应实质,设计了如图所示装置进行实验。
已知: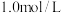 的
的 溶液呈酸性。请回答:
溶液呈酸性。请回答:
(1)装置A中用于添加浓硫酸的仪器名称为________ 。
(2)实验前通入 的目的是
的目的是________________ 。
(3)装置B中产生了白色沉淀,其成分是________ ,说明 具有
具有________ 性。

(4)分析装置B中产生白色沉淀的原因。
观点1: 与
与 反应;
反应;
观点2:在酸性条件下 与
与 反应。
反应。
①若观点1正确,除产生沉淀外,还应观察到的现象是________ 。
②有人认为,如将装置B中的 溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是
溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是________ (填标号)。
A.1mol/L稀硝酸
B.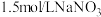 溶液
溶液
C.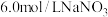 溶液和
溶液和 盐酸等体积混合的溶液
盐酸等体积混合的溶液
D. 溶液和
溶液和 硫酸溶液等体积混合的溶液
硫酸溶液等体积混合的溶液
 和
和 溶液的反应实质,设计了如图所示装置进行实验。
溶液的反应实质,设计了如图所示装置进行实验。已知:
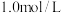 的
的 溶液呈酸性。请回答:
溶液呈酸性。请回答:(1)装置A中用于添加浓硫酸的仪器名称为
(2)实验前通入
 的目的是
的目的是(3)装置B中产生了白色沉淀,其成分是
 具有
具有
(4)分析装置B中产生白色沉淀的原因。
观点1:
 与
与 反应;
反应;观点2:在酸性条件下
 与
与 反应。
反应。①若观点1正确,除产生沉淀外,还应观察到的现象是
②有人认为,如将装置B中的
 溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是
溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是A.1mol/L稀硝酸
B.
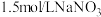 溶液
溶液C.
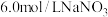 溶液和
溶液和 盐酸等体积混合的溶液
盐酸等体积混合的溶液D.
 溶液和
溶液和 硫酸溶液等体积混合的溶液
硫酸溶液等体积混合的溶液
您最近一年使用:0次
解题方法
10 . 某同学在研究Fe与 的反应时,进行了如图所示实验(部分夹持装置已略去)。
的反应时,进行了如图所示实验(部分夹持装置已略去)。

(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为________________ 。
(2)实验Ⅱ中,铁丝表面迅速变黑,反应很快停止,其原因是________________ 。
(3)实验Ⅲ中,加热试管A,产生大量气体,B中品红溶液褪色,D处始终未检测到可燃性气体,则试管A中产生的气体是________ (填化学式),C的作用是________________ 。
(4)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性源于+6价的硫元素,稀硫酸的氧化性源于________ 。
②造成反应多样性的因素有________ 。
 的反应时,进行了如图所示实验(部分夹持装置已略去)。
的反应时,进行了如图所示实验(部分夹持装置已略去)。
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为
(2)实验Ⅱ中,铁丝表面迅速变黑,反应很快停止,其原因是
(3)实验Ⅲ中,加热试管A,产生大量气体,B中品红溶液褪色,D处始终未检测到可燃性气体,则试管A中产生的气体是
(4)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性源于+6价的硫元素,稀硫酸的氧化性源于
②造成反应多样性的因素有
您最近一年使用:0次
2020-09-23更新
|
522次组卷
|
5卷引用:高一必修第一册(鲁科2019)第3章 第2节 硫的转化 方法帮



