1 . 利用下图装置进行乙醇的催化氧化实验。已知:乙醛可进一步被氧化为乙酸。
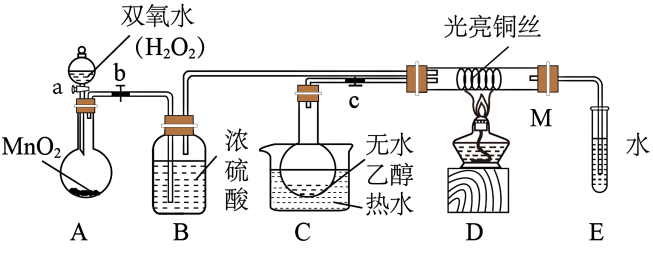
(1)C中热水的作用是_________ 。在装入实验药品之前,应进行的操作是___________ 。
(2)装入实验药品后,打开活塞a、b、c,在铜丝的中间部分加热,通过控制活塞a和b,间歇性地通入氧气,即可在M处观察到受热部分的铜丝___________ (填实验现象)。写出乙醇催化氧化的化学反应方程式___________ 。
(3)若试管E中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有___________ 。要除去该物质,可先在混合液中加入___________ (填字母),然后通过蒸馏即可。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳

(1)C中热水的作用是
(2)装入实验药品后,打开活塞a、b、c,在铜丝的中间部分加热,通过控制活塞a和b,间歇性地通入氧气,即可在M处观察到受热部分的铜丝
(3)若试管E中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
您最近一年使用:0次
解题方法
2 . 二氧化硫是大气污染物之一,充分了解它的性质具有非常重要的意义。
(1)实验室中用下列装置测定SO2被催化氧化为SO3的转化率。(已知SO3的熔点为16.8 ℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响)
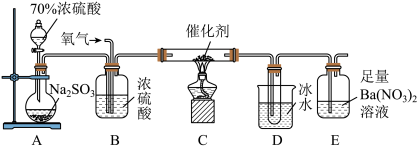
①当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是__________ 。
②实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是___________ (用含字母的代数式表示,不用化简)。
(2)某学习小组设计用如图所示装置验证二氧化硫的化学性质。
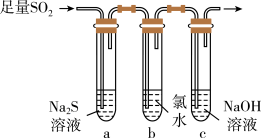
①能说明二氧化硫具有氧化性的实验现象为___________ 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验。
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案中合理的是_____ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为________ 。
(1)实验室中用下列装置测定SO2被催化氧化为SO3的转化率。(已知SO3的熔点为16.8 ℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响)

①当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
②实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是
(2)某学习小组设计用如图所示装置验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验。
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案中合理的是
您最近一年使用:0次
解题方法
3 . 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
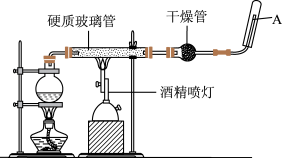
请回答该实验中的问题:
(1)写出该反应的化学方程式:_______ ;并指明该氧化还原反应的还原剂是_______ ,氧化剂是_______ 。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是_______ ;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是_______ 。
(3)酒精灯和酒精喷灯点燃的顺序是_______ ,原因是_______ 。
(4)干燥管中盛装的物质是_______ ,作用是_______ 。
(5)试管中收集的气体是_______ ,如果要在A处玻璃管处点燃该气体,则必须对该气体进行_______ 。

请回答该实验中的问题:
(1)写出该反应的化学方程式:
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是
(3)酒精灯和酒精喷灯点燃的顺序是
(4)干燥管中盛装的物质是
(5)试管中收集的气体是
您最近一年使用:0次
解题方法
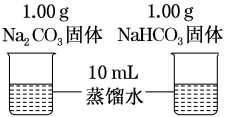
4 . 为探究Na2CO3和NaHCO3的性质,利用传感器继续做如下实验:
提示:溶液pH越小,OH-的浓度越小,溶液碱性越弱。
(1)澄清石灰水显碱性,用电离方程式表示其原因是__________________ 。
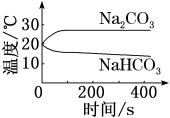
(2)实验③中,溶解时吸收热量的物质是____________________ (填化学式)。
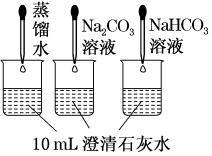
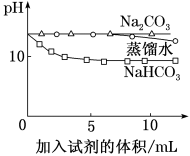
(3)实验④中,Na2CO3溶液和澄清石灰水反应的离子方程式为_________ ,OH-未参与该反应的实验证据是___________ 。
(4)实验④中,滴加NaHCO3溶液的烧杯中溶液pH的变化与滴加Na2CO3溶液的pH有明显差异,原因是滴加NaHCO3溶液的烧杯中________ (填离子符号)参与了反应,写出反应初期的离子方程式:_____________ 。
序号 | 操作 | 数据 |
③ | 测量下面实验过程中温度的变化
|
|
④ | 测量下面实验过程中溶液pH的变化
注:Na2CO3溶液和NaHCO3溶液的浓度相等 |
|
(1)澄清石灰水显碱性,用电离方程式表示其原因是
(2)实验③中,溶解时吸收热量的物质是
(3)实验④中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(4)实验④中,滴加NaHCO3溶液的烧杯中溶液pH的变化与滴加Na2CO3溶液的pH有明显差异,原因是滴加NaHCO3溶液的烧杯中
您最近一年使用:0次
5 . I.铁及其化合物之间的相互转化可用下式表示:
Fe2+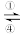 Fe3+
Fe3+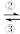

回答下列有关问题:
(1)Fe与过量盐酸反应可以制取FeCl2。若用反应所得的酸性溶液,实现上述①④的转化,要求产物纯净,可选用___________ (填字母)。
a.Cl2 b.Fe c.Cu d.KMnO4
Ⅱ.硫酸亚铁是一种重要的工业原料,同时可以用于制造补血药物,但具有毒性,故严禁在食品中滥用硫酸亚铁。某同学为探究富含硫酸亚铁且保存时间较长的糕点的情况,设计了如图所示实验方案:

该同学在实验中加入了过量新制氯水,放置一段时间后,发现红色褪去,现对褪色原因进行探究(已知SCN-有还原性)。
【提出假设】
(2)假设1:溶液中的+3价铁被氧化为更高的价态;
假设2:___________ 。
【设计方案】
(3)为了对你所提出的假设2进行验证,实验方案是___________ 。
Fe2+
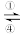 Fe3+
Fe3+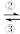

回答下列有关问题:
(1)Fe与过量盐酸反应可以制取FeCl2。若用反应所得的酸性溶液,实现上述①④的转化,要求产物纯净,可选用
a.Cl2 b.Fe c.Cu d.KMnO4
Ⅱ.硫酸亚铁是一种重要的工业原料,同时可以用于制造补血药物,但具有毒性,故严禁在食品中滥用硫酸亚铁。某同学为探究富含硫酸亚铁且保存时间较长的糕点的情况,设计了如图所示实验方案:

该同学在实验中加入了过量新制氯水,放置一段时间后,发现红色褪去,现对褪色原因进行探究(已知SCN-有还原性)。
【提出假设】
(2)假设1:溶液中的+3价铁被氧化为更高的价态;
假设2:
【设计方案】
(3)为了对你所提出的假设2进行验证,实验方案是
您最近一年使用:0次
6 . 过氧化钙(CaO2)广泛应用于水产养殖、污水处理,是优良的供氧剂。
实验探究一:过氧化钙与水反应除生成氧气外,还生成什么物质?
(1)进行实验:取适量过氧化钙放入试管中加适量水,向试管中滴加酚酞溶液,液体变成红色,说明生成了Ca(OH)2,写出该反应的化学方程式:______________ 。
(2)此供氧剂长期暴露在空气中,会变质生成CaCO3,为检验此供氧剂是否变质,可向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。有同学不认同上述方案的理由是_______________________ 。
实验探究二:测定久置过氧化钙纯度。
方案一:通过测定产生氧气的体积,最终计算出供氧剂中过氧化钙的含量。
(3)取一定质量的供氧剂溶于水,按照图1装置进行装配。读出体积时要注意:①该反应为放热反应,待气体恢复至室温再读数;②____________________________ ;③视线和凹液面最低处保持水平再读数。
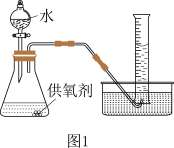
(4)用此装置测得的含量会偏大,原因是________________ ,为了避免此误差可将发生装置换成图2中的装置B或C。
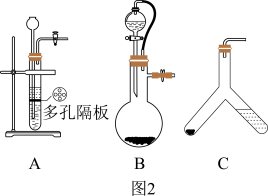
方案二:把样品中的过氧化钙转化为碳酸钙,通过测定碳酸钙沉淀的质量,根据钙元素守恒,求得过氧化钙的质量,具体流程如图3。
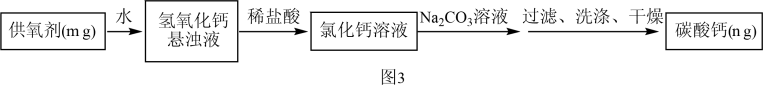
(5)滴加的Na2CO3溶液要过量的原因是_________________________ 。
实验探究一:过氧化钙与水反应除生成氧气外,还生成什么物质?
(1)进行实验:取适量过氧化钙放入试管中加适量水,向试管中滴加酚酞溶液,液体变成红色,说明生成了Ca(OH)2,写出该反应的化学方程式:
(2)此供氧剂长期暴露在空气中,会变质生成CaCO3,为检验此供氧剂是否变质,可向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。有同学不认同上述方案的理由是
实验探究二:测定久置过氧化钙纯度。
方案一:通过测定产生氧气的体积,最终计算出供氧剂中过氧化钙的含量。
(3)取一定质量的供氧剂溶于水,按照图1装置进行装配。读出体积时要注意:①该反应为放热反应,待气体恢复至室温再读数;②

(4)用此装置测得的含量会偏大,原因是

方案二:把样品中的过氧化钙转化为碳酸钙,通过测定碳酸钙沉淀的质量,根据钙元素守恒,求得过氧化钙的质量,具体流程如图3。

(5)滴加的Na2CO3溶液要过量的原因是
您最近一年使用:0次
7 . 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:

(1)I、II、III、IV装置可盛放的试剂是:I___________ ;II___________ ;III___________ ;IV___________ (将下列有关试剂的序号填入空格内)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是___________ 。
(3)使用装置II的目的是___________ 。
(4)使用装置III的目的是___________ 。
(5)确定含有乙烯的现象是___________ 。

(1)I、II、III、IV装置可盛放的试剂是:I
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是
(3)使用装置II的目的是
(4)使用装置III的目的是
(5)确定含有乙烯的现象是
您最近一年使用:0次
2023-06-29更新
|
60次组卷
|
18卷引用:2012年人教版高中化学选修5 2.1脂肪烃练习卷
(已下线)2012年人教版高中化学选修5 2.1脂肪烃练习卷(已下线)2014年高一化学人教版必修2 3.2.1乙烯练习卷课时1 石油的炼制 乙烯——A学习区 夯实基础(鲁科版必修2)课时1 甲烷 石油的炼制与乙烯——A学习区 夯实基础(鲁科版(2019)第二册)内蒙古北京八中乌兰察布分校2016-2017学年高一下学期第二次调考化学试题高二人教版选修5 第三章 烃的含氧衍生物 第一节 醇酚云南省绥江县一中2018-2019学年高一下学期期末考试化学试题吉林省公主岭市范家屯镇第一中学2019-2020学年高二上学期第二次月考化学试题黑龙江省大兴安岭地区漠河县第一中学2018-2019学年高二上学期第一次月考化学试题山东省德州市齐河县实验中学2019-2020学年高一下学期期中考试化学试题福建省莆田第七中学2020-2021学年高二上学期第一次月考化学试题上海市奉城高级中学2018-2019学年高二上学期期末考试化学试题安徽省安庆桐城市第八中学2020-2021学年高二上学期第一次段考化学试题黑龙江省双鸭山市第一中学2020-2021学年高二下学期4月月考化学试题云南省元阳县一中2020-2021学年高一下学期6月份考试化学试题陕西省西安市蓝田县大学区联考2022-2023学年高二下学期6月期末考试化学试题2.1.1有机化学反应的主要类型(课前)-鲁科版选择性必修3陕西省西安市蓝田县大学区联考2022-2023学年高二下学期4月期中考试化学试题
8 . 为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
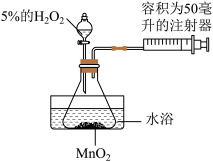
(1)实验2中应加入5%H2O2_______ 毫升:
(2)在两次实验中,可通过_______ 来比较H2O2分解反应速率的大小:
(3)实验2中水浴温度控制在80°C时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有_______ ;
(4)实验结束后若要将MnO2从混合物汇总分离出来,可采取的方法是_______ 。

| 实验1 | 实验2 | |
| MnO2的质量/克 | 0.5 | 0.5 |
| 5%的H2O2的体积/毫升 | 40 | 待填 |
| 水浴温度/°C | 20 | 80 |
(2)在两次实验中,可通过
(3)实验2中水浴温度控制在80°C时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有
(4)实验结束后若要将MnO2从混合物汇总分离出来,可采取的方法是
您最近一年使用:0次
名校
解题方法
9 . 实验小组利用传感器探究Na2CO3和NaHCO3的性质。
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱
【实验过程】
【分析与解释】
(1)实验I中,溶解时吸收热量的物质是_______ 。
(2)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为_______ ,OH-未参与该反应的实验证据是_______ 。
(3)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,造成这种差异是由于滴加NaHCO3溶液的烧杯中有_______ (填写离子符号)参与反应。
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱
【实验过程】
| 编号 | 实验操作 | 实验数据 |
| 实验I | 测量下述实验过程的温度变化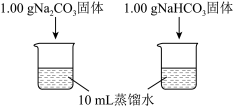 | 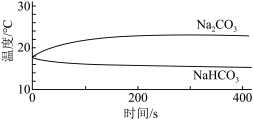 |
| 实验II | 测量下述实验过程的pH变化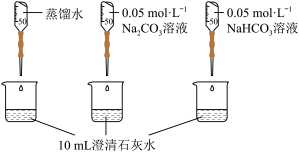 |  |
(1)实验I中,溶解时吸收热量的物质是
(2)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(3)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,造成这种差异是由于滴加NaHCO3溶液的烧杯中有
您最近一年使用:0次
2022-11-30更新
|
294次组卷
|
13卷引用:高一必修第一册(苏教2019)专题3 第二单元 金属钠及钠的化合物4
高一必修第一册(苏教2019)专题3 第二单元 金属钠及钠的化合物4北京市2020年普通高中学业水平合格性模拟考试化学试题2020年北京市第一次普通高中学业水平合格性考试化学试题北京市回民学校2020-2021学年高一上学期期中考试化学试题北京市第三十一中学2020—2021学年度高一下学期期中考试化学试题北京第七中学2020-2021学年高一下学期期中考试化学试题天津市红桥区2020-2021学年高一下学期期末考试化学试题(已下线)北京市第四中学2022-2023学年高一上学期期中考试化学试题北京市第四十三中学2022-2023学年高一上学期期中考试化学试题北京市第八中学2022-2023学年高一下学期期末考试化学试题(已下线)专题八 钠及其化合物北京市第十一中学2023-2024学年高一上学期期中考试化学试题北京市月坛中学2023-2024学年高一上学期期中考试化学试题
10 . 某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明,浓硝酸能将一氧化氮氧化成二氧化氮,而稀硝酸不能氧化一氧化氮。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
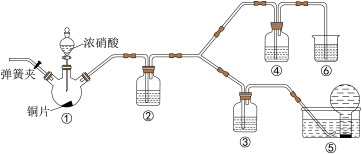
可选试剂:浓硝酸,稀硝酸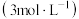 ,蒸馏水,浓硫酸,NaOH溶液。
,蒸馏水,浓硫酸,NaOH溶液。
已知:NaOH溶液不与一氧化氮反应,能与二氧化氮反应。

(1)做实验时应避免将有害气体排放到空气中,装置③④⑥中盛放的试剂依次是_______ 、_______ 、_______ 。
(2)装置①中所发生反应的化学方程式是_______ 。
(3)装置②的作用是_______ ,其中所发生反应的化学方程式是_______ 。
(4)该小组得出结论所依据的实验现象是_______ 。

可选试剂:浓硝酸,稀硝酸
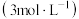 ,蒸馏水,浓硫酸,NaOH溶液。
,蒸馏水,浓硫酸,NaOH溶液。已知:NaOH溶液不与一氧化氮反应,能与二氧化氮反应。

(1)做实验时应避免将有害气体排放到空气中,装置③④⑥中盛放的试剂依次是
(2)装置①中所发生反应的化学方程式是
(3)装置②的作用是
(4)该小组得出结论所依据的实验现象是
您最近一年使用:0次