23-24高一上·全国·假期作业
解题方法
1 . 已知氨可以与灼热的氧化铜反应生成氮气和金属铜,用下面示意图中的装置可以实现该反应。
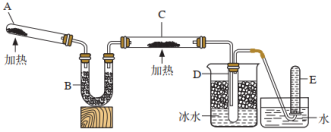
A中装有的NH4Cl和Ca(OH)2混合物在加热条件下,可以发生反应生成CaCl2、NH3和H2O。
试回答下列问题:
(1)B中加入的物质是碱石灰(CaO和NaOH的混合物),其作用是____ 。
(2)实验时在C中观察到的现象是____ ,发生反应的化学方程式是_____ 。
(3)实验时在D中观察到的现象是____ ,收集到的物质是____ 。

A中装有的NH4Cl和Ca(OH)2混合物在加热条件下,可以发生反应生成CaCl2、NH3和H2O。
试回答下列问题:
(1)B中加入的物质是碱石灰(CaO和NaOH的混合物),其作用是
(2)实验时在C中观察到的现象是
(3)实验时在D中观察到的现象是
您最近半年使用:0次
2 . 氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

(1)写出合成塔和氧化炉中发生反应的化学方程式____ ,并指出其中的氧化剂和还原剂__ 。
(2)请思考A是什么物质_______ ,以及向吸收塔中通入A的作用_________ 。
(3)工业生产中为了盛装大量浓硝酸,可选择_______ 作为罐体材料。
a.铜 b.铂 c.铝 d.镁
(4)为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的 溶液等吸收尾气,后者使用
溶液等吸收尾气,后者使用 或其他物质将氮氧化物还原为
或其他物质将氮氧化物还原为 。请以尾气中的
。请以尾气中的 处理为例,写出相关反应的化学方程式
处理为例,写出相关反应的化学方程式___ ,并查阅资料,了解还有哪些尾气处理方法______ 。

(1)写出合成塔和氧化炉中发生反应的化学方程式
(2)请思考A是什么物质
(3)工业生产中为了盛装大量浓硝酸,可选择
a.铜 b.铂 c.铝 d.镁
(4)为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的
 溶液等吸收尾气,后者使用
溶液等吸收尾气,后者使用 或其他物质将氮氧化物还原为
或其他物质将氮氧化物还原为 。请以尾气中的
。请以尾气中的 处理为例,写出相关反应的化学方程式
处理为例,写出相关反应的化学方程式
您最近半年使用:0次
2021-12-02更新
|
1344次组卷
|
2卷引用:人教2019版必修第二册第五章 化工生产中的重要非金属元素复习与提高
3 . 请设计尽可能多的实验方案,在实验室中制备
____________ 。

您最近半年使用:0次
2021-12-01更新
|
502次组卷
|
2卷引用:人教2019版必修第一册第三章 铁 金属材料复习与提高
11-12高二上·北京·单元测试
4 . 化合物SOCl2是一种液态化合物,沸点为77℃,在盛有10mL的锥形瓶中小心滴加8~10滴SOCl2,可观察到剧烈水解反应,液面有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色.轻轻振荡锥形瓶,等白雾消失后,往溶液中滴加AgNO3溶液,有不溶于HNO3的白色凝乳状沉淀析出.
(1)根据上述实验,写出SOCL2和水反应的化学方程式_______________________________ .
(2)AlCl3溶液蒸干灼烧得不到无水AlCl3,而用SOCl2与AlCl3·H2O 混合共热,可得到无水AlCl3,其原因是___________________________________________________________________________ .
(1)根据上述实验,写出SOCL2和水反应的化学方程式
(2)AlCl3溶液蒸干灼烧得不到无水AlCl3,而用SOCl2与AlCl3·H2O 混合共热,可得到无水AlCl3,其原因是
您最近半年使用:0次



