1 .  的转化是资源利用和环境保护的重要研究课题。
的转化是资源利用和环境保护的重要研究课题。
(1)通过电化学循环法可将 转化为
转化为 和
和 (如图所示)。其中氧化过程发生如下两步反应:
(如图所示)。其中氧化过程发生如下两步反应: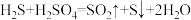 、
、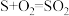 。
。
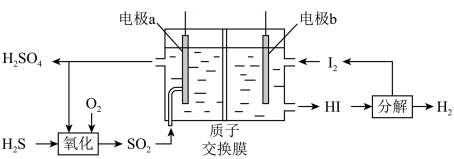
①电极a上发生反应的电极反应式为_______ 。
②理论上1mol 参加反应可产生
参加反应可产生 的物质的量为
的物质的量为_______ 。
(2) 可用作脱除
可用作脱除 气体的脱硫剂。以赤铁矿渣(主要成分为
气体的脱硫剂。以赤铁矿渣(主要成分为 、
、 和少量
和少量 )为原料制备
)为原料制备 晶体,已知
晶体,已知 易溶于水难溶于乙醇,请补充完整相应的实验方案:取一定量的赤铁矿渣,
易溶于水难溶于乙醇,请补充完整相应的实验方案:取一定量的赤铁矿渣,_______ ,向滤液中加乙醇,在恒温水浴槽中冷却结晶,过滤,用丙酮洗涤,干燥。(已知该实验中pH=3.5时, 沉淀完全;pH=4.1时,
沉淀完全;pH=4.1时, 开始沉淀。实验中必须使用的试剂:1.0
开始沉淀。实验中必须使用的试剂:1.0
 、1.0
、1.0 NaOH、铁粉。)
NaOH、铁粉。)
 的转化是资源利用和环境保护的重要研究课题。
的转化是资源利用和环境保护的重要研究课题。(1)通过电化学循环法可将
 转化为
转化为 和
和 (如图所示)。其中氧化过程发生如下两步反应:
(如图所示)。其中氧化过程发生如下两步反应: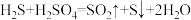 、
、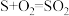 。
。
①电极a上发生反应的电极反应式为
②理论上1mol
 参加反应可产生
参加反应可产生 的物质的量为
的物质的量为(2)
 可用作脱除
可用作脱除 气体的脱硫剂。以赤铁矿渣(主要成分为
气体的脱硫剂。以赤铁矿渣(主要成分为 、
、 和少量
和少量 )为原料制备
)为原料制备 晶体,已知
晶体,已知 易溶于水难溶于乙醇,请补充完整相应的实验方案:取一定量的赤铁矿渣,
易溶于水难溶于乙醇,请补充完整相应的实验方案:取一定量的赤铁矿渣, 沉淀完全;pH=4.1时,
沉淀完全;pH=4.1时, 开始沉淀。实验中必须使用的试剂:1.0
开始沉淀。实验中必须使用的试剂:1.0
 、1.0
、1.0 NaOH、铁粉。)
NaOH、铁粉。)
您最近一年使用:0次
2 . 有机化合物A常用于配制香水、精油,为测定A的结构,某化学兴趣小组进行如下实验。回答下列问题:
(1)13.6g有机物A置于氧气流中充分燃烧,生成17.92L (标准状况)和7.2g
(标准状况)和7.2g ,通过质谱仪测得A的相对分子质量为136,则A的分子式为
,通过质谱仪测得A的相对分子质量为136,则A的分子式为_______ 。有机物A的红外光谱如图所示,则A可能的结构简式为_______ 、_______ 。
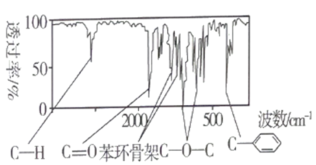
(2)请设计简单实验,确定A的结构简式_______ 。(可选用的试剂:银氨溶液,氢氧化钠溶液,稀硫酸,限选一种试剂)
(3)探究制备A的最佳反应条件:
①该小组成员通过核磁共振仪测定A的核磁共振氢谱如图所示。在实验室中,利用有机酸B和醇C,通过酯化反应制备A的化学方程式为_______ 。反应结束后,可用_______ (填序号)洗涤粗产品A。
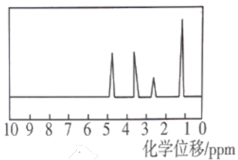
A.稀硫酸 B.饱和碳酸钠溶液 C.乙醇 D.水
②该小组通过监测混合物中有机酸B的含量,探究制备A的最佳反应温度。已知:A、B、C的熔沸点如表-1所示,有机酸B的含量如图3。该反应的最佳温度为_______ (填序号)。温度超过106℃后,B的含量逐渐增大的原因为_______ 。
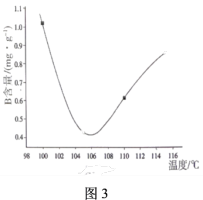
A.100℃ B.106℃ C.116℃
(1)13.6g有机物A置于氧气流中充分燃烧,生成17.92L
 (标准状况)和7.2g
(标准状况)和7.2g ,通过质谱仪测得A的相对分子质量为136,则A的分子式为
,通过质谱仪测得A的相对分子质量为136,则A的分子式为
(2)请设计简单实验,确定A的结构简式
(3)探究制备A的最佳反应条件:
①该小组成员通过核磁共振仪测定A的核磁共振氢谱如图所示。在实验室中,利用有机酸B和醇C,通过酯化反应制备A的化学方程式为

A.稀硫酸 B.饱和碳酸钠溶液 C.乙醇 D.水
②该小组通过监测混合物中有机酸B的含量,探究制备A的最佳反应温度。已知:A、B、C的熔沸点如表-1所示,有机酸B的含量如图3。该反应的最佳温度为
| 物质 | 熔点 | 沸点 |
| A | -12.3 | 199.6 |
| B | 122.4 | 249 |
| C | - 97 | 64.3 |

A.100℃ B.106℃ C.116℃
您最近一年使用:0次
3 . 化学工业为疫情防控提供了强有力的物质支撑。次氯酸溶液是常用的消毒剂,可利用Cl2O与水反应得到。根据该原理,某化学兴趣小组利用如下装置制备一定浓度的次氯酸溶液。已知:常温常压下,Cl2O为棕黄色气体,沸点为3.8℃,42℃以上会分解为Cl2和O2。实验时,将氯气和空气(不参与反应)按体积比为1:3混合通入含水8%的碳酸钠糊状物中,请回答下列问题:
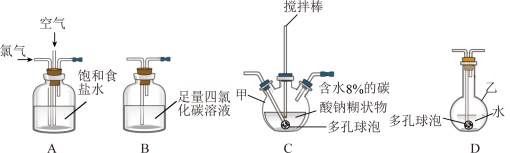
(1)实验室一般通过MnO2与浓盐酸加热制备氯气,发生反应的离子方程式为_______ 。
(2)装置C中的仪器甲的名称为_______ ,仪器甲中发生反应的化学方程式为_______ ,为了提高 的产率,需控制反应在合适的温度,可采取的操作为
的产率,需控制反应在合适的温度,可采取的操作为_______ 。
(3)装置 的作用为
的作用为_______ ,有同学建议将装置 中的仪器乙换为棕色瓶,原因是
中的仪器乙换为棕色瓶,原因是_______ 。
(4)测定装置D中得到的次氯酸的物质的量浓度。量取 装置D中得到的次氯酸溶液,并稀释至
装置D中得到的次氯酸溶液,并稀释至 ,再从中取出
,再从中取出 至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (滴定反应为
(滴定反应为 )。
)。
①次氯酸与KI溶液反应时氧化剂与还原剂的物质的量之比为_______ 。
②达到滴定终点的现象为_______ 。
③装置D中得到的次氯酸的物质的量浓度为_______ mol/L。
④若滴定开始前滴定管尖嘴有气泡,滴定结束后气泡消失,则测定的次氯酸的物质的量浓度将_______ (填“偏低”、“偏高”或“无影响”)。

(1)实验室一般通过MnO2与浓盐酸加热制备氯气,发生反应的离子方程式为
(2)装置C中的仪器甲的名称为
 的产率,需控制反应在合适的温度,可采取的操作为
的产率,需控制反应在合适的温度,可采取的操作为(3)装置
 的作用为
的作用为 中的仪器乙换为棕色瓶,原因是
中的仪器乙换为棕色瓶,原因是(4)测定装置D中得到的次氯酸的物质的量浓度。量取
 装置D中得到的次氯酸溶液,并稀释至
装置D中得到的次氯酸溶液,并稀释至 ,再从中取出
,再从中取出 至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (滴定反应为
(滴定反应为 )。
)。①次氯酸与KI溶液反应时氧化剂与还原剂的物质的量之比为
②达到滴定终点的现象为
③装置D中得到的次氯酸的物质的量浓度为
④若滴定开始前滴定管尖嘴有气泡,滴定结束后气泡消失,则测定的次氯酸的物质的量浓度将
您最近一年使用:0次
4 . 以工厂烟气中的 为原料制备脱氯剂
为原料制备脱氯剂 。
。
(1) 制备。边搅拌边向
制备。边搅拌边向 溶液中通入
溶液中通入 。
。
① 溶液中通入
溶液中通入 得到
得到 ,其离子方程式为
,其离子方程式为_______ 。
② 溶液中
溶液中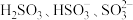 随
随 的分布下图所示。确定何时停止通
的分布下图所示。确定何时停止通 的操作为
的操作为_______ 。

(2) 制备。请补充完整由S和
制备。请补充完整由S和 溶液制备
溶液制备 的实验方案:向过量硫磺粉中加入
的实验方案:向过量硫磺粉中加入 溶液,加热充分反应,
溶液,加热充分反应,_______ ,低温干燥得产品。[实验中必须使用的试剂:无水乙醇]
(3)废水中 的测定。取出一定量废水于锥形瓶中,加入足量硫酸酸化的
的测定。取出一定量废水于锥形瓶中,加入足量硫酸酸化的 溶液,充分反应后加入2~3滴淀粉溶液,然后用
溶液,充分反应后加入2~3滴淀粉溶液,然后用 标准溶液滴定。已知:
标准溶液滴定。已知: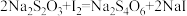 。
。

①滴定达到终点时的实验现象是_______ 。
②若滴定过程中滴定管中的液面如图所示,则a=_______  。
。
 为原料制备脱氯剂
为原料制备脱氯剂 。
。(1)
 制备。边搅拌边向
制备。边搅拌边向 溶液中通入
溶液中通入 。
。①
 溶液中通入
溶液中通入 得到
得到 ,其离子方程式为
,其离子方程式为②
 溶液中
溶液中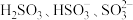 随
随 的分布下图所示。确定何时停止通
的分布下图所示。确定何时停止通 的操作为
的操作为
(2)
 制备。请补充完整由S和
制备。请补充完整由S和 溶液制备
溶液制备 的实验方案:向过量硫磺粉中加入
的实验方案:向过量硫磺粉中加入 溶液,加热充分反应,
溶液,加热充分反应,(3)废水中
 的测定。取出一定量废水于锥形瓶中,加入足量硫酸酸化的
的测定。取出一定量废水于锥形瓶中,加入足量硫酸酸化的 溶液,充分反应后加入2~3滴淀粉溶液,然后用
溶液,充分反应后加入2~3滴淀粉溶液,然后用 标准溶液滴定。已知:
标准溶液滴定。已知: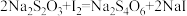 。
。
①滴定达到终点时的实验现象是
②若滴定过程中滴定管中的液面如图所示,则a=
 。
。
您最近一年使用:0次
解题方法
5 . 二氧化氯(ClO2)是一种高效的灭菌消毒剂,受热或浓度过大时易发生分解甚至爆炸。工业上常将ClO2制备成NaClO2固体以便运输和贮存,流程如下:
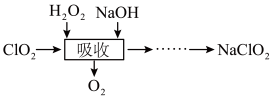
(1)“吸收”过程中发生反应的离子方程式是_______ 。
(2)“吸收”过程,温度控制在25℃的目的是_______ (填字母)。
a.保持适当的反应速率 b.促进H2O2分解 c.防止温度过高引起爆炸
(3)NaClO2的溶解度曲线如图所示,由NaClO2溶液得到无水NaClO2的操作如下:

①减压,55℃蒸发结晶;
②_______ ;
③38℃~60℃热水洗涤;
④低于60℃干燥。

(1)“吸收”过程中发生反应的离子方程式是
(2)“吸收”过程,温度控制在25℃的目的是
a.保持适当的反应速率 b.促进H2O2分解 c.防止温度过高引起爆炸
(3)NaClO2的溶解度曲线如图所示,由NaClO2溶液得到无水NaClO2的操作如下:

①减压,55℃蒸发结晶;
②
③38℃~60℃热水洗涤;
④低于60℃干燥。
您最近一年使用:0次
6 . 脱硝技术主要用于脱除燃煤烟气中的NO。
I.配合物生物脱硝法
以Fe(II)EDTA2-为吸收剂结合微生物进行脱硝的原理如图所示:

已知:NO 、NO
、NO 会使微生物总量下降。
会使微生物总量下降。
(1)若烟气中参与反应的n(NO):n(O2)=1:1,碳源为C6H12O6,写出过程中脱硝总反应的化学方程式_______ 。
(2)该原理中将“化学吸收”与“生物还原”分开在不同容器中进行的原因是_______ 。
Ⅱ.ClO2氧化脱硝法
电解NaClO3制备ClO2的装置如图所示。

(3)写出该电解过程中总反应的化学方程式_______ 。
(4)ClO2氧化脱硝过程发生的反应是:5NO+3ClO2+4H2O=5HNO3+3HCl。已知:①ClO2与水能产生•OH,•OH更易与NO反应;②ClO2受热易分解,反应为2ClO2=Cl2+2O2。当烟气流速、烟气中NO浓度及n(ClO2)/n(NO)一定时,温度对NO脱除效率的影响如图所示。温度升高,脱硝率变化不大的原因可能是_______ 。

(5)烟气中混有的SO2能与ClO2反应。
①写出SO2与溶液中ClO2反应的离子方程式_______ 。
②其他条件一定时,SO2浓度的增加对脱硝率影响不大,其原因可能是_______ 。
I.配合物生物脱硝法
以Fe(II)EDTA2-为吸收剂结合微生物进行脱硝的原理如图所示:

已知:NO
 、NO
、NO 会使微生物总量下降。
会使微生物总量下降。(1)若烟气中参与反应的n(NO):n(O2)=1:1,碳源为C6H12O6,写出过程中脱硝总反应的化学方程式
(2)该原理中将“化学吸收”与“生物还原”分开在不同容器中进行的原因是
Ⅱ.ClO2氧化脱硝法
电解NaClO3制备ClO2的装置如图所示。

(3)写出该电解过程中总反应的化学方程式
(4)ClO2氧化脱硝过程发生的反应是:5NO+3ClO2+4H2O=5HNO3+3HCl。已知:①ClO2与水能产生•OH,•OH更易与NO反应;②ClO2受热易分解,反应为2ClO2=Cl2+2O2。当烟气流速、烟气中NO浓度及n(ClO2)/n(NO)一定时,温度对NO脱除效率的影响如图所示。温度升高,脱硝率变化不大的原因可能是

(5)烟气中混有的SO2能与ClO2反应。
①写出SO2与溶液中ClO2反应的离子方程式
②其他条件一定时,SO2浓度的增加对脱硝率影响不大,其原因可能是
您最近一年使用:0次
解题方法
7 . 硫酸是最重要的化工产品之一,常用于物质的制备、催化等领域。
(1)工业上用硫酸制备硫酸铜。
方案I:将铜与浓硫酸共热,反应生成硫酸铜。
方案II:向铜与稀硫酸的混合物中持续通入氧气并加热,反应原理: 。
。
①方案I反应的化学方程式为___________ 。
②在实验室中,将浓硫酸稀释为稀硫酸的操作方法为___________ 。
③比较以上两种制备方案,哪一种方案更好,理由是___________ 。
(2)浓硫酸常用作实验室制取乙酸乙酯的催化剂。制取乙酸乙酯的化学方程式为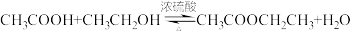 ,乙酸中所含官能团的名称为
,乙酸中所含官能团的名称为_______ 。
(1)工业上用硫酸制备硫酸铜。
方案I:将铜与浓硫酸共热,反应生成硫酸铜。
方案II:向铜与稀硫酸的混合物中持续通入氧气并加热,反应原理:
 。
。①方案I反应的化学方程式为
②在实验室中,将浓硫酸稀释为稀硫酸的操作方法为
③比较以上两种制备方案,哪一种方案更好,理由是
(2)浓硫酸常用作实验室制取乙酸乙酯的催化剂。制取乙酸乙酯的化学方程式为
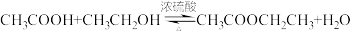 ,乙酸中所含官能团的名称为
,乙酸中所含官能团的名称为
您最近一年使用:0次



