名校
解题方法
1 . 利用如图所示装置不能完成对应实验的是( )
A.图甲可以用来制备Fe(OH)3胶体 |
B.图乙可以用来证明酸性强弱顺序:H2SO4>H2CO3>H2SiO3 |
C.图丙可以通过点燃肥皂泡来检验是否有氢气气体生成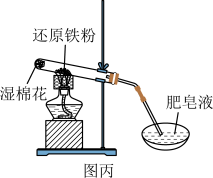 |
D.图丁可以用陶瓷坩埚加热融化NaOH固体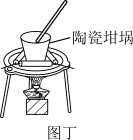 |
您最近一年使用:0次
2020-04-03更新
|
156次组卷
|
2卷引用:百校联盟2019-2020学年高一上学期第四次月考化学试题 化学
名校
解题方法
2 . 在化学研究中,往往可以通过观察现象认识物质变化的情况。请分析以下一组有现象变化的化学反应。
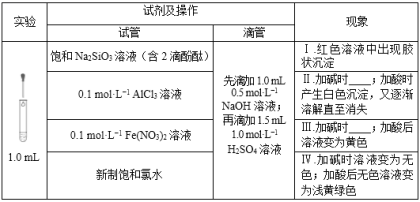
(1)用离子方程式解释现象Ⅰ中出现胶状沉淀的原因:_____________ 。
(2)Ⅱ中加碱时出现的现象是_______________ ,此现象说明溶液中发生反应的离子方程式是____________________________________ 。
(3)Ⅲ中加碱时出现的现象是_____________________________________ 。
(4)用离子方程式解释Ⅳ中加碱时出现的现象:____________________________________ 。
(5)滴加试剂顺序的变化,会影响溶液中的现象和发生的反应,请继续分析以下实验。
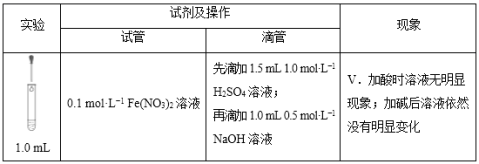
① 探究加酸时Fe(NO3)2溶液中是否发生了反应:
向1.0mL 0.1mol/LFe(NO3)2溶液中______________ ,溶液立即变红,说明溶液中含Fe3+,证明加酸时溶液中发生了反应。
② 推测溶液中产生Fe3+的可能原因有两种:
a.酸性条件下,0.1mol/LFe(NO3)2溶液中的Fe2+被NO3-氧化;
b.______________________ (用离子方程式表示)。

(1)用离子方程式解释现象Ⅰ中出现胶状沉淀的原因:
(2)Ⅱ中加碱时出现的现象是
(3)Ⅲ中加碱时出现的现象是
(4)用离子方程式解释Ⅳ中加碱时出现的现象:
(5)滴加试剂顺序的变化,会影响溶液中的现象和发生的反应,请继续分析以下实验。

① 探究加酸时Fe(NO3)2溶液中是否发生了反应:
向1.0mL 0.1mol/LFe(NO3)2溶液中
② 推测溶液中产生Fe3+的可能原因有两种:
a.酸性条件下,0.1mol/LFe(NO3)2溶液中的Fe2+被NO3-氧化;
b.
您最近一年使用:0次
解题方法
3 . 氮化镁(Mg3N2)在工业上应用广泛,通常条件下为黄绿色粉末,极易与水反应,常用作接触媒。
I.氮化镁的制备下面是甲、乙两位学生提出的制备氮化镁的实验方案示意图(实验前系统内的空气已排除。图中箭头表示气体的流向)。
甲.
乙.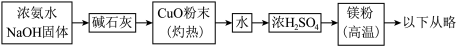
(1)Mg3N2的电子式为___________ ,甲同学的实验方案不能顺利制得氮化镁,原因为________ (用化学方程式表示)。
(2)乙同学方案中NaOH固体的作用为_____________________________________________ 。
(3)丙同学利用空气中含有大量N2的事实,用以下装置设计了另外一种制备氮化镁的方案(夹持装置略去):
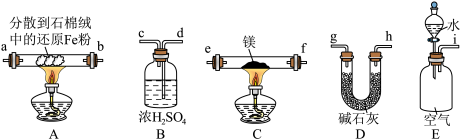
①按气流由左到右的方向,上述装置合理的连接顺序为____________ (填接口字母);
②装置B的作用为___________ ,装置D的作用为__________________________ 。
Ⅱ.定性分析产物
Ⅲ.定量测定氮化镁纯度
i.称取4.0 g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1.00 mol/L盐酸中,充分反应后,将所得溶液稀释到200.00mL;
ii.取20.00 mL稀释后的溶液,用0.2 mol/L NaOH标准溶液滴定过量的盐酸,达到终点时消耗标准溶液25.00 mL。
(6)产物中氮化镁的质量分数为_______________ 。
I.氮化镁的制备下面是甲、乙两位学生提出的制备氮化镁的实验方案示意图(实验前系统内的空气已排除。图中箭头表示气体的流向)。
甲.

乙.

(1)Mg3N2的电子式为
(2)乙同学方案中NaOH固体的作用为
(3)丙同学利用空气中含有大量N2的事实,用以下装置设计了另外一种制备氮化镁的方案(夹持装置略去):

①按气流由左到右的方向,上述装置合理的连接顺序为
②装置B的作用为
Ⅱ.定性分析产物
| 操作步明 | 实验现象 | 解释原因 |
| 取少量产品于试管中,加适量蒸馏水 | 试管底部有固体不溶物,有刺激性气味的气体产生 | (4)反应的化学方程式为 |
| . | ||
| 弃去上层清液,加入足量稀盐酸 | 观察到固体全部溶解,且有气泡冒出 | (5)气泡冒出的原因为 |
i.称取4.0 g反应后的固体,加入足量水,将生成的气体全部蒸出并通入100.00mL 1.00 mol/L盐酸中,充分反应后,将所得溶液稀释到200.00mL;
ii.取20.00 mL稀释后的溶液,用0.2 mol/L NaOH标准溶液滴定过量的盐酸,达到终点时消耗标准溶液25.00 mL。
(6)产物中氮化镁的质量分数为
您最近一年使用:0次
名校
解题方法
4 . 某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2 gCuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是_______________ (填实验序号),步骤①、③中研磨固体所用仪器的名称是___________________ ;
(2)步骤③中洗涤沉淀的操作是______________________________________________
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
用图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:

回答下列问题:
(3)上述实验中的“待测数据”指_____________ ;
(4)若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,__________________________________________ ;
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a、_______________________________ ,b、_____________________________ 。
(一)制取氧化铜
①称取2 gCuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是
(2)步骤③中洗涤沉淀的操作是
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
用图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:

| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2 g | 无其他物质 | |
| ⑤ | 1.2 g | CuO 0.5 g | |
| ⑥ | 1.2 g | MnO2 0.5 g |
(3)上述实验中的“待测数据”指
(4)若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a、
您最近一年使用:0次
2017-10-16更新
|
67次组卷
|
2卷引用:辽宁省葫芦岛市第一中学2017-2018学年高一上学期第一次月考化学试题
名校
解题方法
5 . 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:_______ 。
A. Na2SO3溶液与HNO3 B. Na2SO3固体与浓硫酸
C. 硫化氢在空气中燃烧 D. 高温煅烧硫铁矿
(2)装置C的作用是______________________________ 。
(3)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、________ 、自然干燥,在这一系列操作中没有用到的仪器有________ (填序号)。
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯 E.玻璃棒 F.坩埚
(4)①写出SO2与FeCl3溶液反应的离子方程式:______________________________ ;
②请设计实验方案检验反应后A中Fe2+生成______________________________ ;
③本实验中能表明SO2的还原性比I-的还原性强的现象是__________________ ,其反应的离子方程式为___________________________________________ 。

A. Na2SO3溶液与HNO3 B. Na2SO3固体与浓硫酸
C. 硫化氢在空气中燃烧 D. 高温煅烧硫铁矿
(2)装置C的作用是
(3)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯 E.玻璃棒 F.坩埚
(4)①写出SO2与FeCl3溶液反应的离子方程式:
②请设计实验方案检验反应后A中Fe2+生成
③本实验中能表明SO2的还原性比I-的还原性强的现象是
您最近一年使用:0次
2017-08-28更新
|
145次组卷
|
2卷引用:甘肃省武威市第六中学2018届高三第一次阶段性过关考试化学试题
6 . 某学生用下图所示的装置测定镁的相对原子质量:

(1)①实验前必须对装置进行气密性检查,具体操作是:__________________ ;
(2)如果量气管的最大测量体积为50mL(假设条件为标准状况),则取金属镁条(设纯度为100%)的质量不超过______ g;(精确到0.001)
(3)实验结束,在读取数据前必须:a冷却,使温度恢复到原来状态;b_________________ ;
(4)该学生实验时称取镁条0.051g(已除去氧化膜),实验结果收集到气体48.00mL(已换算到标准状况,其他实验操作均正确),根据实验测定,镁的相对原子质量为_________ ;产生误差的原因可能是__________ (写出一点)。

(1)①实验前必须对装置进行气密性检查,具体操作是:
(2)如果量气管的最大测量体积为50mL(假设条件为标准状况),则取金属镁条(设纯度为100%)的质量不超过
(3)实验结束,在读取数据前必须:a冷却,使温度恢复到原来状态;b
(4)该学生实验时称取镁条0.051g(已除去氧化膜),实验结果收集到气体48.00mL(已换算到标准状况,其他实验操作均正确),根据实验测定,镁的相对原子质量为
您最近一年使用:0次



