名校
1 . 海洋是巨大的资源宝库,可以从海洋中获取多种化工原料。
I.海带提碘___________ (填仪器名称)中,用酒精灯充分加热灰化。
(2)设计实验证明“浸泡”已经进行完全:___________ 需要用到的实验药品有:淀粉溶液、硫酸酸化的 溶液,写出具体实验操作和现象)。
溶液,写出具体实验操作和现象)。
(3)“氧化”步骤发生反应的离子方程式为___________ 。
II.海水的综合利用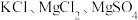 和
和 等。
等。
(4)操作1的名称为___________ 。
(5)操作2为粗盐精制的过程,为除去粗盐中的 和
和 ,加入下列试剂的顺序为
,加入下列试剂的顺序为___________ (填序号)。
① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④稀盐酸
溶液 ④稀盐酸
(6)试剂1最好选用___________ (填字母);电解无水氯化镁的化学方程式为___________ 。
A. B.
B. C.
C. D.
D.
(7)将吹出后的含 空气按一定速率通入吸收塔,用
空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。
①流程中可用热空气吹出溴的原因为___________ 。
②“吸收塔”内发生反应的离子方程式为___________ 。
I.海带提碘
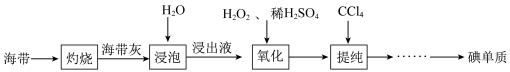
(2)设计实验证明“浸泡”已经进行完全:
 溶液,写出具体实验操作和现象)。
溶液,写出具体实验操作和现象)。(3)“氧化”步骤发生反应的离子方程式为
II.海水的综合利用
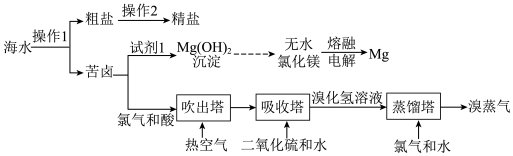
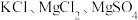 和
和 等。
等。(4)操作1的名称为
(5)操作2为粗盐精制的过程,为除去粗盐中的
 和
和 ,加入下列试剂的顺序为
,加入下列试剂的顺序为①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④稀盐酸
溶液 ④稀盐酸(6)试剂1最好选用
A.
 B.
B. C.
C. D.
D.
(7)将吹出后的含
 空气按一定速率通入吸收塔,用
空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。①流程中可用热空气吹出溴的原因为
②“吸收塔”内发生反应的离子方程式为
您最近一年使用:0次
解题方法
2 . 工业上可用海水、石英砂 、焦炭、氮气等原料制备高纯硅和氮化硅,一种工艺流程如下:
、焦炭、氮气等原料制备高纯硅和氮化硅,一种工艺流程如下:
①向粗盐水中加入过量 溶液,目的是
溶液,目的是___________ 。沉淀完全后加入过量___________ ,目的是除去 ,再加入过量
,再加入过量 溶液,反应的离子方程式为
溶液,反应的离子方程式为___________ 。过滤,向滤液中加适量的盐酸,即得精盐水。
②向粗盐水中加入 溶液,证明沉淀完全的操作是
溶液,证明沉淀完全的操作是___________ 。
(2) 的分子式为
的分子式为___________ ,反应①~④中,属于置换反应的有___________ 。
(3)石英砂反应前需要粉碎,目的是___________ ,反应①的化学方程式为___________ 。
(4)反应④中氧化剂与还原剂的物质的量之比是___________ 。
 、焦炭、氮气等原料制备高纯硅和氮化硅,一种工艺流程如下:
、焦炭、氮气等原料制备高纯硅和氮化硅,一种工艺流程如下: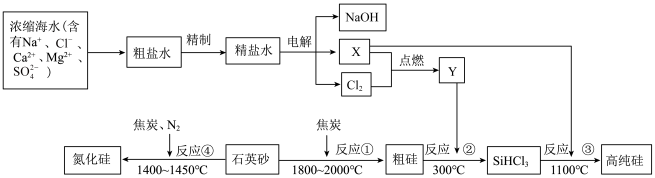
①向粗盐水中加入过量
 溶液,目的是
溶液,目的是 ,再加入过量
,再加入过量 溶液,反应的离子方程式为
溶液,反应的离子方程式为②向粗盐水中加入
 溶液,证明沉淀完全的操作是
溶液,证明沉淀完全的操作是(2)
 的分子式为
的分子式为(3)石英砂反应前需要粉碎,目的是
(4)反应④中氧化剂与还原剂的物质的量之比是
您最近一年使用:0次
3 . 下列关于粗盐提纯的说法中正确的是
| A.溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解 |
| B.滤去不溶性杂质后,将滤液移至蒸发皿内加热浓缩 |
| C.当蒸发到剩余少量液体时停止加热,利用余热将液体蒸干 |
| D.将制得的晶体转移到新制过滤器中用大量水洗涤 |
您最近一年使用:0次
名校
4 . 南海是一个巨大的资源宝库,海水开发利用的部分过程如图所示,下列说法错误的是
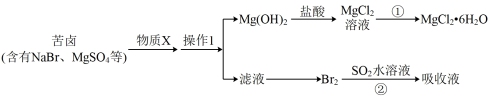
| A.物质X常选用CaO |
B.第①步中为了得到干燥的 固体,应采用高温烘干 固体,应采用高温烘干 |
| C.操作1中玻璃棒的作用是引流 |
D.第②步中反应的离子方程式为: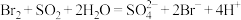 |
您最近一年使用:0次
名校
5 . NaCl是一种化工原料,可以制备多种物质,如下图所示,下列说法错误的是
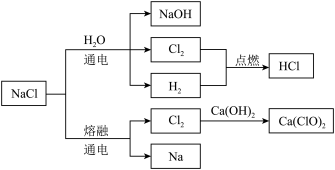
| A.工业上电解饱和食盐水被称为氯碱工业 |
B.工业上电解熔融的氯化钠可制得金属钠,阴极的电极反应式为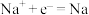 |
C.工业上将氯气通入冷的澄清石灰水中制备漂白粉,其有效成分为 |
D.纯净的 能在氯气中安静地燃烧,发出苍白色火焰,工业上用此原理制备盐酸 能在氯气中安静地燃烧,发出苍白色火焰,工业上用此原理制备盐酸 |
您最近一年使用:0次
解题方法
6 . 化学服务生活。下列有关说法正确的是
| A.利用冰箱存储食物可减缓食物变质的速率 |
| B.以氧化铝、氧化钇等氧化物为成分的透明陶瓷,是金属材料 |
| C.信息传输系统使用的光导纤维,主要成分是Si |
| D.蒸馏海水,可制得食盐、蒸馏水以及镁、溴、碘等单质 |
您最近一年使用:0次
名校
解题方法
7 . 海洋中有丰富的资源,下图为海水资源利用的部分过程。下列有关说法正确的是
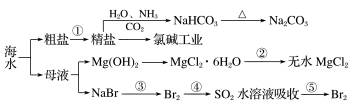
A.在第①步中除去粗盐中的 、 、 、 、 等杂质,加入药品的顺序为NaCO3溶液→NaOH溶液→ 等杂质,加入药品的顺序为NaCO3溶液→NaOH溶液→ 溶液→过滤后加盐酸 溶液→过滤后加盐酸 |
| B.步骤③通入氯气后,再通热空气将溴单质吹出,利用了溴密度较小的性质 |
| C.工业上通过电解熔融MgO制取金属镁 |
D.反应④的离子方程式为: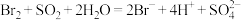 |
您最近一年使用:0次
名校
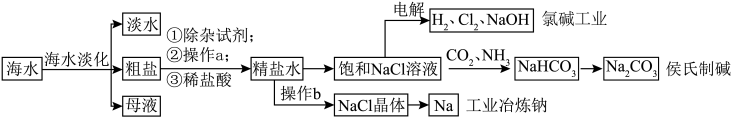
8 . 海水中蕴含着丰富的化学物质,从海水中获得的NaCl除了可供食用,还是一种重要的化工原料,部分应用方向如下图所示。
(1)海水淡化的方法主要有___________ (写一种即可)。
(2)粗盐的主要成分为NaCl,还含有少量的Ca2+、Mg2+和SO 。将粗盐溶于水后,依次加入足量的除杂试剂为___________(填字母)。1
。将粗盐溶于水后,依次加入足量的除杂试剂为___________(填字母)。1
(3)在实验室完成操作a和操作b,都需要用到的玻璃仪器是___________ ,工业冶炼钠的化学方程式为___________ 。
(4)通过氯碱工业制备3.36LCl2(标准状况下),理论上需要转移的电子数为___________ 。
(5)侯氏制碱第一步中通入CO2和NH3的顺序为___________ (选填“先通CO2”、“先通NH3”或“同时通入”)。
(6)下列有关说法不正确的是___________(填字母)。
(1)海水淡化的方法主要有
(2)粗盐的主要成分为NaCl,还含有少量的Ca2+、Mg2+和SO
 。将粗盐溶于水后,依次加入足量的除杂试剂为___________(填字母)。1
。将粗盐溶于水后,依次加入足量的除杂试剂为___________(填字母)。1| A.NaOH溶液、Na2CO3溶液、BaCl2溶液 |
| B.Na2CO3溶液、KOH溶液BaCl2溶液 |
| C.BaCl2溶液、Na2CO3溶液、NaOH溶液 |
| D.KOH溶液、BaCl2溶液、Na2CO3溶液 |
(3)在实验室完成操作a和操作b,都需要用到的玻璃仪器是
(4)通过氯碱工业制备3.36LCl2(标准状况下),理论上需要转移的电子数为
(5)侯氏制碱第一步中通入CO2和NH3的顺序为
(6)下列有关说法不正确的是___________(填字母)。
| A.在水中的溶解度NaHCO3大于NaCl |
| B.母液(苦卤)可以用于提炼获得工业溴和镁 |
| C.上述应用方向所涉及的反应均为氧化还原反应 |
| D.氯碱工业制得的Cl2和H2必须分开收集、分开保存 |
您最近一年使用:0次
2024-07-10更新
|
32次组卷
|
3卷引用:贵州省铜仁市2023-2024年高一下学期化学期末考试试卷
9 . NaCl被称为“化学工业之母”。下列说法不正确的是
| A.“制钠”:电解熔融的NaCl可制备金属Na |
B.“氯碱工业”:电解饱和食盐水可获得 、NaOH和 、NaOH和 |
C.“侯氏制碱”:将 、 、 通入饱和食盐水中,析出碳酸钠晶体 通入饱和食盐水中,析出碳酸钠晶体 |
| D.“海水晒盐”过程主要发生物理变化 |
您最近一年使用:0次
2023-05-16更新
|
173次组卷
|
2卷引用:江苏省徐州市铜山区2022-2023学年高一下学期期中化学(合格考)试题
23-24高一下·全国·课后作业
名校
10 . 海洋中有丰富的资源,下图为海水资源利用的部分过程。下列有关说法正确的是
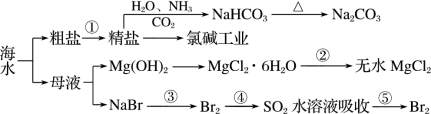
A.在第①步中除去粗盐中的 、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.操作④的目的是对溴进行富集 |
| C.工业上通过电解饱和 MgCl2溶液制取金属镁 |
D.反应④的离子方程式为:Br2+SO2+2H2O=2HBr+2H++SO |
您最近一年使用:0次
2024-02-25更新
|
370次组卷
|
4卷引用:8.1自然资源的开发利用课后作业提高篇
(已下线)8.1自然资源的开发利用课后作业提高篇湖南省长沙市弘益高级中学2022-2023学年高一下学期期末考试化学试题(已下线)8.1.1 金属矿物、海水资源的开发利用陕西省咸阳市武功县普集高级中学2023-2024学年高一下学期6月月考化学试题



