解题方法
1 . 海洋资源的利用具有非常广阔的研究价值。
Ⅰ.利用空气吹出法从海水(弱碱性)中提取溴的流程如图。
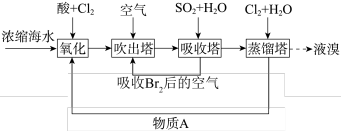
已知:溴单质的沸点为 。
。
(1)溴元素在元素周期表中的位置是___________ 。
(2)“氧化”中发生反应的离子方程式为___________ 。
(3)“蒸馏塔”中温度应控制在___________ (填字母序号)。
A.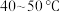 B.
B.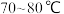 C.
C. 以上
以上
(4)物质A___________ (填化学式)可以循环利用,降低成本。
(5)探究“氧化”的适宜条件。下图为不同条件下海水中被氧化的 的百分含量。
的百分含量。
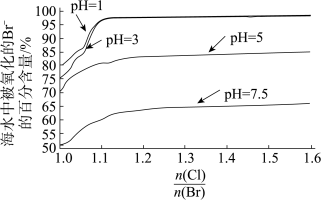
注: 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。
①“氧化”的适宜条件为___________ 。
②若海水中溴的浓度为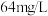 ,经该方法处理
,经该方法处理 海水后最终得到
海水后最终得到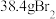 ,则溴的总提取率为
,则溴的总提取率为___________ 。
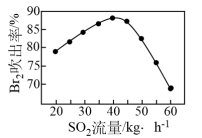
③吹出塔中, 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示。由图可知,
流量的关系如图所示。由图可知, 流量过大,
流量过大, 吹出率反而下降,原因是
吹出率反而下降,原因是___________ 。
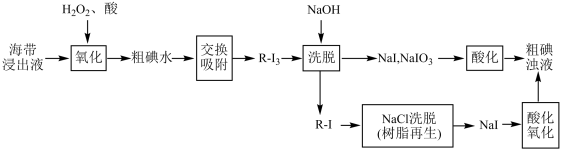
Ⅱ.离子交换法从海带中提取碘是一种较为先进的制碘工艺。使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程如下:
已知:① ;
;
②强碱性阴离子树脂(用 表示,
表示, 可被其它更易被吸附的阴离子替代)对多磺离子(
可被其它更易被吸附的阴离子替代)对多磺离子( )有很强的交换吸附能力;
)有很强的交换吸附能力;
③“交换吸附”发生的反应为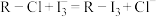 。
。
回答下列问题:
(6)下列各步反应中,不属于氧化还原反应的有___________(填字母序号)。
(7)“氧化”时发生的反应有①___________ ;②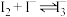 。
。
Ⅰ.利用空气吹出法从海水(弱碱性)中提取溴的流程如图。

已知:溴单质的沸点为
 。
。(1)溴元素在元素周期表中的位置是
(2)“氧化”中发生反应的离子方程式为
(3)“蒸馏塔”中温度应控制在
A.
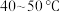 B.
B.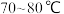 C.
C. 以上
以上(4)物质A
(5)探究“氧化”的适宜条件。下图为不同条件下海水中被氧化的
 的百分含量。
的百分含量。
注:
 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。①“氧化”的适宜条件为
②若海水中溴的浓度为
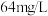 ,经该方法处理
,经该方法处理 海水后最终得到
海水后最终得到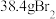 ,则溴的总提取率为
,则溴的总提取率为③吹出塔中,
 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示。由图可知,
流量的关系如图所示。由图可知, 流量过大,
流量过大, 吹出率反而下降,原因是
吹出率反而下降,原因是
Ⅱ.离子交换法从海带中提取碘是一种较为先进的制碘工艺。使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程如下:

已知:①
 ;
;②强碱性阴离子树脂(用
 表示,
表示, 可被其它更易被吸附的阴离子替代)对多磺离子(
可被其它更易被吸附的阴离子替代)对多磺离子( )有很强的交换吸附能力;
)有很强的交换吸附能力;③“交换吸附”发生的反应为
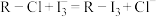 。
。回答下列问题:
(6)下列各步反应中,不属于氧化还原反应的有___________(填字母序号)。
| A.交换吸附 | B.洗脱 | C.酸化氧化 | D. 洗脱 洗脱 |
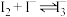 。
。
您最近半年使用:0次
2 . 海洋资源的利用具有非常广阔的前景。
I.利用空气吹出法从海水(弱碱性)中提取溴的流程如图。

已知:溴单质的沸点为58.5℃。
(1)溴元素在元素周期表中的位置是_______ 。
(2)“吸收塔”中发生反应的离子方程式为_______ 。
(3)“蒸馏塔”中温度应控制在_______ (填序号)。
A.40~50℃ B.70~80℃ C.100℃以上
(4)物质A_______ (填化学式)可以循环利用,降低成本。
(5)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的Br-的百分含量如图:

注: 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。
①“氧化”的适宜条件为_______ 。
②已知:海水中溴的浓度是64 mg/L ,经该方法处理后1m3海水最终得到 38.4g Br2,则溴的总提取率为_______ 。
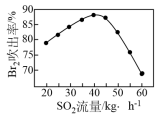
③吸收后的空气进行循环利用。吹出时,Br2 吹出率与吸收塔中SO2流量的关系如图所示。SO2 流量过大,Br2 吹出率反而下降的原因是:___________ 。
Ⅱ.离子交换法从海带中提取碘是一种较为先进的制碘工艺。如图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。

已知:①I2 + I- I
I ;
;
②强碱性阴离子树脂(用R-Cl表示,Cl-可被其它更易被吸附的阴离子替代)对多碘离子(I )有很强的交换吸附能力;
)有很强的交换吸附能力;
③步骤“交换吸附”发生的反应:R-Cl+I =R-I3+Cl-。
=R-I3+Cl-。
试回答下列问题:
(6)下列各步反应中,属于氧化还原反应的有:_______(填序号)
(7)酸性条件下,原料被H2O2氧化时发生的反应有:①_______ ;②I2+I- I
I 。
。
(8)实验室模拟步骤“酸化氧化”,一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则添加氧化剂与NaI的质量比应不少于_______ 。
I.利用空气吹出法从海水(弱碱性)中提取溴的流程如图。

已知:溴单质的沸点为58.5℃。
(1)溴元素在元素周期表中的位置是
(2)“吸收塔”中发生反应的离子方程式为
(3)“蒸馏塔”中温度应控制在
A.40~50℃ B.70~80℃ C.100℃以上
(4)物质A
(5)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的Br-的百分含量如图:

注:
 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。①“氧化”的适宜条件为
②已知:海水中溴的浓度是64 mg/L ,经该方法处理后1m3海水最终得到 38.4g Br2,则溴的总提取率为
③吸收后的空气进行循环利用。吹出时,Br2 吹出率与吸收塔中SO2流量的关系如图所示。SO2 流量过大,Br2 吹出率反而下降的原因是:

Ⅱ.离子交换法从海带中提取碘是一种较为先进的制碘工艺。如图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。

已知:①I2 + I-
 I
I ;
;②强碱性阴离子树脂(用R-Cl表示,Cl-可被其它更易被吸附的阴离子替代)对多碘离子(I
 )有很强的交换吸附能力;
)有很强的交换吸附能力;③步骤“交换吸附”发生的反应:R-Cl+I
 =R-I3+Cl-。
=R-I3+Cl-。试回答下列问题:
(6)下列各步反应中,属于氧化还原反应的有:_______(填序号)
| A.交换吸附 | B.洗脱 | C.酸化氧化 | D.NaCl洗脱 |
 I
I 。
。(8)实验室模拟步骤“酸化氧化”,一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则添加氧化剂与NaI的质量比应不少于
您最近半年使用:0次



