1 . 海水开发利用的部分过程如图所示,下列有关说法错误的是
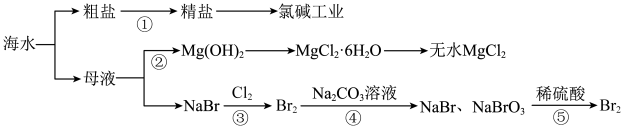

| A.由粗盐制取精盐,需除去其中的不溶性杂质与可溶性杂质 |
| B.步骤②在工业生产中常加入火碱作Mg2+的沉淀剂,以降低生产成本 |
| C.第④步反应的化学方程式为3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑ |
| D.第⑤步反应中理论上生成1molBr2时,转移电子数为5NA |
您最近一年使用:0次
2023高三·全国·专题练习
2 . 海水开发利用的部分过程如图所示。下列说法错误的是
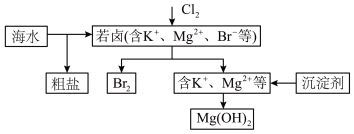

| A.向苦卤中通入Cl2是为了提取溴 |
| B.粗盐可依次加入沉淀剂BaCl2、NaOH、Na2CO3溶液提纯 |
| C.工业生产中常选用NaOH作为沉淀剂之一 |
| D.富集溴元素可以用水蒸气吹出单质溴,再用Na2SO3将其还原吸收 |
您最近一年使用:0次
名校
3 . 工业上制备下列物质的生产流程合理的是
A.工业制硫酸:硫铁矿 SO2 SO2 SO3 SO3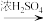 H2SO4 H2SO4 |
B.由NaCl制漂白粉:饱和食盐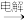 Cl2 Cl2 漂白粉 漂白粉 |
C.从海水中提取镁:海水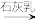  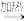 MgO MgO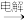 Mg Mg |
D.工业合成硝酸:N2 NO NO NO2 NO2 HNO3 HNO3 |
您最近一年使用:0次
4 . 海洋资源丰富,从海水中获取镁和溴的流程示意图如下:

| A.从经济角度,试剂X最适合的是氢氧化钠 |
B.直接将 溶液加热蒸干得 溶液加热蒸干得 |
C.可用 或 或 代替 代替 吸收含溴的空气 吸收含溴的空气 |
| D.虚线框内流程的主要目的是减少环境污染 |
您最近一年使用:0次
2023-12-31更新
|
45次组卷
|
2卷引用:2024届四川省德阳市高三上学期第一次诊断性考试 化学试题
5 . 海洋中的化学资源具有巨大的开发潜力,海水的综合利用示意图如下,下列有关说法正确的是
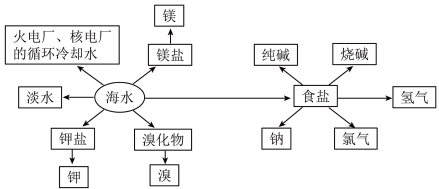
A.向 的食盐水中先通入NH3,再通入CO2即可析出小苏打进而制备纯碱 的食盐水中先通入NH3,再通入CO2即可析出小苏打进而制备纯碱 |
| B.海水提取溴采用先吹出再吸收的目的是提高溴的浓度 |
| C.制镁过程中可直接蒸发MgCl2溶液制备无水MgCl2 |
| D.火电厂利用物质燃烧产生的热能直接转化为电能来实现火力发电 |
您最近一年使用:0次
2023-12-31更新
|
158次组卷
|
3卷引用:浙江省北斗星盟2024届高三上学期12月联考-化学试题
浙江省北斗星盟2024届高三上学期12月联考-化学试题 河南省濮阳市油田第一中学2023-2024学年高三上学期第五次考试理科综合试题-高中化学(已下线)压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
6 . 已知MgO、MgCl2的熔点分别为2800 ℃、604 ℃,将MgO、MgCl2加热熔融后通电电解,都可得到金属镁。海水中含有MgCl2,工业上从海水中提取镁正确的方法是
A.海水 Mg(OH)2 Mg(OH)2 Mg Mg |
B.海水 MgCl2溶液→MgCl2(熔融) MgCl2溶液→MgCl2(熔融) Mg Mg |
C.海水 Mg(OH)2 Mg(OH)2 MgO MgO Mg Mg |
D.海水 Mg(OH)2 Mg(OH)2 MgCl2溶液→MgCl2(熔融) MgCl2溶液→MgCl2(熔融) Mg Mg |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
7 . 海洋是非常巨大的资源宝库,下列有关海洋资源开发利用的说法,不正确的有
| A.海洋约占地球表面积的71%,水储量达1.3×109亿吨,人类不存在缺水问题 |
| B.海水资源的利用包括水资源的利用和化学资源的利用,二者可以综合进行 |
| C.海水中除H2O外,还含有Cl、Na、K、Mg、Ca、Br、F等多种元素的化学资源 |
| D.从海水中获取食盐的过程属于物理变化 |
| E.从海水中可以得到NaCl,电解熔融NaCl可制备金属Na |
| F.海水蒸发制粗盐的过程中只发生了化学变化 |
| G.海水中含有钾元素,只需经过物理变化就可以得到钾单质 |
| H.从海水中提取溴单质的过程一定涉及氧化还原反应 |
| I.从海水中可以得到MgCl2,电解MgCl2溶液可制备Mg和Cl2 |
您最近一年使用:0次
2023高三·全国·专题练习
8 . 海水中有取之不尽的化学资源,从海水中可提取多种化工原料。下图是某工厂对海水资源的综合利用的示意图。

试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO 等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:
等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:
①粗盐溶液中加入过量的Na2CO3溶液:_______ 。
②滤液中加入盐酸至溶液呈中性:_______ 。
(2)母液中含有K+、Na+、Mg2+等阳离子,从以上流程可以看出,对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是_______ ;石灰乳是生石灰与水作用形成的化合物,生产生石灰的主要原料是_______ ;若加入石灰乳后所制取的产品中还混杂着熟石灰,那么将熟石灰从该产品中除去的方法是_______ 。
②电解无水氯化镁的化学方程式是_______ 。
③电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气的冷却剂的是_______ (填序号)。
A.H2 B.CO2 C.O2 D.水蒸气
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新的母液中加入一种常见的气态氧化剂,又制取了重要的化工原料溴单质。
①生成溴单质的化学反应的离子方程式是_______ ;生产中将溴单质从化合物中分离出来的方法是_______ ,这种方法的成功应用是基于溴单质具有_______ 性。
②从多种经营、综合开发、打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目是_______ 。

试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO
 等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:
等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中依次加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出下列操作中发生的化学反应的离子方程式:①粗盐溶液中加入过量的Na2CO3溶液:
②滤液中加入盐酸至溶液呈中性:
(2)母液中含有K+、Na+、Mg2+等阳离子,从以上流程可以看出,对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是
②电解无水氯化镁的化学方程式是
③电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气的冷却剂的是
A.H2 B.CO2 C.O2 D.水蒸气
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新的母液中加入一种常见的气态氧化剂,又制取了重要的化工原料溴单质。
①生成溴单质的化学反应的离子方程式是
②从多种经营、综合开发、打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目是
您最近一年使用:0次
9 . 如图是某化工厂对海水资源综合利用的示意图。根据以上信息,判断下列相关分析不正确的是
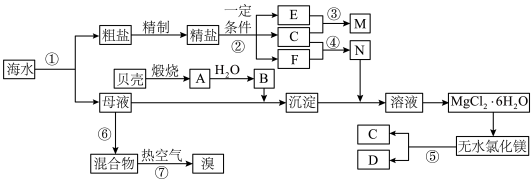

| A.上述提取Mg的流程中,没有涉及的反应类型是置换反应 |
| B.因氮气的化学性质相对稳定,冷却电解无水氯化镁所得的镁蒸气时,可选择氦气 |
| C.反应⑥所用的气态氧化剂可从本厂生产烧碱处循环利用或从本厂生产镁单质处循环利用 |
| D.从母液中提取Mg和Br2的先后顺序:先提取Mg,后提取Br2 |
您最近一年使用:0次
10 . 第三周期元素的单质及其化合物具有重要用途。如在熔融状态下,可用金属钠制备金属钾; 可制备多种镁产品;铝—空气电池具有较高的比能量,在碱性电解液中总反应为
可制备多种镁产品;铝—空气电池具有较高的比能量,在碱性电解液中总反应为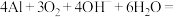
 。高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷(
。高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷( ),再经氢气还原得到高纯硅。硫有多种单质,如斜方硫(燃烧热为297 kJ⋅mol-1)、单斜硫等。
),再经氢气还原得到高纯硅。硫有多种单质,如斜方硫(燃烧热为297 kJ⋅mol-1)、单斜硫等。 可除去废水中
可除去废水中 等重金属离子,
等重金属离子, 水溶液在空气中会缓慢氧化生成S而变浑浊。下列物质的性质与用途具有对应关系的是
水溶液在空气中会缓慢氧化生成S而变浑浊。下列物质的性质与用途具有对应关系的是
 可制备多种镁产品;铝—空气电池具有较高的比能量,在碱性电解液中总反应为
可制备多种镁产品;铝—空气电池具有较高的比能量,在碱性电解液中总反应为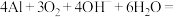
 。高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷(
。高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷( ),再经氢气还原得到高纯硅。硫有多种单质,如斜方硫(燃烧热为297 kJ⋅mol-1)、单斜硫等。
),再经氢气还原得到高纯硅。硫有多种单质,如斜方硫(燃烧热为297 kJ⋅mol-1)、单斜硫等。 可除去废水中
可除去废水中 等重金属离子,
等重金属离子, 水溶液在空气中会缓慢氧化生成S而变浑浊。下列物质的性质与用途具有对应关系的是
水溶液在空气中会缓慢氧化生成S而变浑浊。下列物质的性质与用途具有对应关系的是A.熔融 能电解,可用作冶炼镁的原料 能电解,可用作冶炼镁的原料 |
B. 具有还原性,可除去废水中的 具有还原性,可除去废水中的 |
| C.钠的密度比钾大,可用于冶炼金属钾 |
| D.晶体硅熔点高、硬度大,可用作通讯设备的芯片 |
您最近一年使用:0次



