2011高三上·江苏·专题练习
名校
1 . 镁及其合金是一种用途很广的金属材料,海水中镁的含量为1.10 mg·L-1,目前世界上60%的镁是从海水中提取的。主要步骤如下:

(1)为了使MgSO4完全转化为Mg(OH)2,可以加入过量试剂①,试剂①最好选用__________ 。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
________________________________________________________________ 。
(3)试剂②可以选用________ ,其反应的离子方程式为______________________ 。
(4)无水MgCl2在熔融状态下,通电后会产生Cl2和Mg,写出该反应的化学方程式______________________________________________ 。
(5)若假设海水中镁元素全部存在于MgSO4中,则海水中MgSO4的含量为____ mg·L-1,若某工厂每天生产1.00 t镁,则每天需要海水的体积为________ L。

(1)为了使MgSO4完全转化为Mg(OH)2,可以加入过量试剂①,试剂①最好选用
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
(3)试剂②可以选用
(4)无水MgCl2在熔融状态下,通电后会产生Cl2和Mg,写出该反应的化学方程式
(5)若假设海水中镁元素全部存在于MgSO4中,则海水中MgSO4的含量为
您最近一年使用:0次
2011·黑龙江·三模
2 . A、G、J均为非金属单质,工业上利用反应①来冶炼与A同主族元素G单质的粗产品。K为无色液体,D是一种常见金属,溶于某无氧酸中得到H溶液,该无氧酸的阴离子在同主族元素形成的简单阴离子中还原性最强(除放射性元素)。其物质间转化关系如下图:(部分反应物和生成物略去)

(1)写出下列物质的化学式B______ , F_______ , H______ 。A和G的最简单气态氢化物中,较稳定的物质是_______ (填化学式),写出反应①的化学方程式________________________ 。
(2)反应②是工业上冶炼金属D的方法之一,然而目前世界上60%的D单质是从海水中提取的。以下是海水中提炼金属D的简易流程图(结合工业生产实际,在括号内填写需要加入物质的化学式,方框内填写生成物质的化学式)

①__________ ②_____________ ③_______________
(3)海带中含有H的阴离子,常用过氧化氢、稀硫酸和淀粉来检验其阴离子,其主要反应的离子方程式为___________________________________________ 。
(4)写出G→J的化学方程式________________________________________ ,某同学利用了某技巧首先配平了G和J的系数,下列关系符合此技巧且正确的是_________
A.反应①:F:G=1:1 B.反应②:A:D=1:1
C.反应③:A:J=2:1 D.反应④:E:B =1:1

(1)写出下列物质的化学式B
(2)反应②是工业上冶炼金属D的方法之一,然而目前世界上60%的D单质是从海水中提取的。以下是海水中提炼金属D的简易流程图(结合工业生产实际,在括号内填写需要加入物质的化学式,方框内填写生成物质的化学式)

①
(3)海带中含有H的阴离子,常用过氧化氢、稀硫酸和淀粉来检验其阴离子,其主要反应的离子方程式为
(4)写出G→J的化学方程式
A.反应①:F:G=1:1 B.反应②:A:D=1:1
C.反应③:A:J=2:1 D.反应④:E:B =1:1
您最近一年使用:0次
解题方法
3 . 海水是巨大的资源宝库。下图是人类从海水资源获取某些重要化工原料的流程示意图。
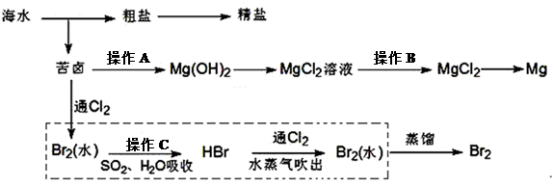
回答下列问题:
(1)操作B是_________________ (填实验具体操作名称)。原因是________ (用离子方程式表示)。
(2)操作A需加入下列试剂中的一种,最合适的是______ (选填编号)。
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳 d.碳酸钠溶液
(3)上图中虚线框内流程的主要作用是_________________ ;
(4)上图中虚线框内流程也可用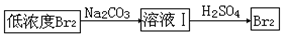 替代,请将Br2与Na2CO3反应的化学方程式补充完整并配平
替代,请将Br2与Na2CO3反应的化学方程式补充完整并配平
___ Br2 + ___ Na2CO3 = NaBrO3 + ___ _________ + ___ CO2
(5)写出将MgCl2转化为Mg时获得的副产品的一种用途(用方程式表示)____________ 。

回答下列问题:
(1)操作B是
(2)操作A需加入下列试剂中的一种,最合适的是
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳 d.碳酸钠溶液
(3)上图中虚线框内流程的主要作用是
(4)上图中虚线框内流程也可用
 替代,请将Br2与Na2CO3反应的化学方程式补充完整并配平
替代,请将Br2与Na2CO3反应的化学方程式补充完整并配平(5)写出将MgCl2转化为Mg时获得的副产品的一种用途(用方程式表示)
您最近一年使用:0次
2011·辽宁·一模
4 . 沿海地区有着丰富的海水资源,海水占地球总储水量的97.4﹪,海水是人类宝贵的自然资源,若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海水资源,从海水中可以提取多种化工原料,下图是某工厂对海水资源综合利用的示意图:
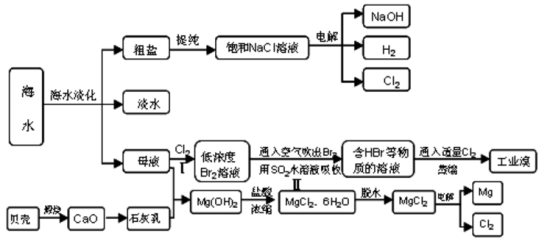
⑴请列举海水淡化的两种方法____________________ 、_____________________ 。
⑵使用离子交换树脂与水中的离子进行交换也是常用的水处理技术。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式_____________ .
⑶步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是:____________ .
步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式
_________________________________________________________
⑷在制取无水氯化镁时需要在干燥的HCl气流中加热MgCl2 6H2O的原因
6H2O的原因
_____________________________________________________________________ .
⑸电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是______
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
⑹苦卤(海水蒸发结晶分离出食盐后的母液)中含有较多的NaCl、MgCl2、KCl、MgSO4等物质.用沉淀法测定苦卤中MgCl2的含量(g/L),测定过程中应获取的数据有
___________________________________________________ .

⑴请列举海水淡化的两种方法
⑵使用离子交换树脂与水中的离子进行交换也是常用的水处理技术。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式
⑶步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是:
步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式
⑷在制取无水氯化镁时需要在干燥的HCl气流中加热MgCl2
 6H2O的原因
6H2O的原因⑸电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
⑹苦卤(海水蒸发结晶分离出食盐后的母液)中含有较多的NaCl、MgCl2、KCl、MgSO4等物质.用沉淀法测定苦卤中MgCl2的含量(g/L),测定过程中应获取的数据有
您最近一年使用:0次
2011·广东揭阳·一模
5 . 某研究性学习小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产提取镁,主要过程如下:
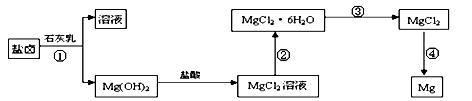
回答下列问题:
(1)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2 ,除去少量Ca(OH)2的方法是先将沉淀加入到盛有________ 饱和溶液的烧杯中,充分搅拌后经______ 、______ (填操作方法)可得纯净的Mg(OH)2。写出有关反应的离子方程式__________ 。
(2)右图是该研究性学习小组设计进行过程③的实验装置图。其中装置A的作用是_______ 。
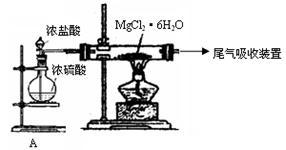
若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是________________ 。
(3)写出过程④中发生反应的化学方程式_______________ 。

回答下列问题:
(1)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2 ,除去少量Ca(OH)2的方法是先将沉淀加入到盛有
(2)右图是该研究性学习小组设计进行过程③的实验装置图。其中装置A的作用是

若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是
(3)写出过程④中发生反应的化学方程式
您最近一年使用:0次
6 . 目前下列工艺过程没有直接使用离子交换技术的是
| A.硬水的软化 | B.电解饱和食盐水制造NaOH |
| C.电渗析淡化海水 | D.海水中提取金属Mg |
您最近一年使用:0次
2016-12-09更新
|
943次组卷
|
3卷引用:2007年普通高等学校招生全国统一考试(海南卷)化学试题
真题
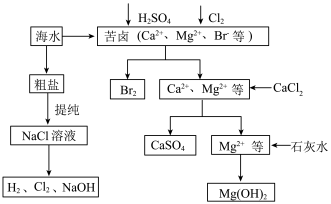
7 . 工业上对海水资源综合开发利用的部分工艺流程如下图所示。
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜均允许通过的分子或离子是_______ 。电解槽中的阳极材料为_________________ 。
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备_______ ?原因是____________________________ 。
(3)膜在四氧化碳中的溶解度比在水中大得多,四氧化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氧化碳,原因是______________________________________ 。
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜均允许通过的分子或离子是
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备
(3)膜在四氧化碳中的溶解度比在水中大得多,四氧化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氧化碳,原因是
您最近一年使用:0次
2010·江西·三模
解题方法
8 . 海水中有丰富的化学资源,从海水中可提取多种化工原料,下图是海水综合利用——合成氨——纯碱的联合生产工艺流程:
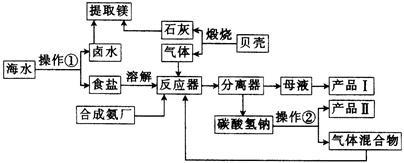
(1)写出反应器中发生反应的化学方程式:__________ 。
(2)分离器中进行的操作名称是____ ,图中操作①是__________ 。
(3)产品Ⅱ是______ (填化学式)。
(4)写出合成氨厂里用天然气和水蒸气在催化剂和高温下反应制备原料气H2的化学方程式:_________ 。
(5)设计用卤水和石灰及其他必要试剂提取镁的过程:_______________ (用化学方程式表示)。

(1)写出反应器中发生反应的化学方程式:
(2)分离器中进行的操作名称是
(3)产品Ⅱ是
(4)写出合成氨厂里用天然气和水蒸气在催化剂和高温下反应制备原料气H2的化学方程式:
(5)设计用卤水和石灰及其他必要试剂提取镁的过程:
您最近一年使用:0次
2010·福建泉州·一模
9 . 化学与科技、社会、生活有着密切的联系,下列说法不正确的是
| A.橡胶、塑料和光导纤维都是有机高分子化合物 |
| B.废电池要集中处理,防止其中的重金属盐对土壤和水源造成污染 |
| C.从海水提取金属镁的过程中涉及氧化还原反应 |
| D.利用太阳能、风能和氢能替代化石能源能改善空气质量 |
您最近一年使用:0次
10 . O、Si、Al是地壳中含量最多的三种元素,Na、Mg、Cl是海水中的重要元素。下列说法正确的是
| A.电解Al2O3和SiO2(少量)的混合物,可以制得较纯净的Al,且有氧气生成 |
| B.从海水中制备Na、Mg、Al、Cl四种元素单质的反应都是氧化还原反应 |
| C.普通玻璃、水泥成分中都含有O、Si、Al三种元素 |
| D.加热蒸干NaCl、MgCl2溶液时可以得到晶体NaCl、MgCl2 |
您最近一年使用:0次



