10. Ⅰ.(1)298K时,0.5molC
2H
4(g)完全燃烧生成二氧化碳和液态水,放出705.5kJ的热量。请写出该反应的热化学方程式
________。
(2)Na
2SO
3具有还原性,其水溶液可以吸收Cl
2(g),减少环境污染。
已知反应: Na
2SO
3(aq)+Cl
2(g)+H
2O(l)=Na
2SO
4(aq)+2HCl(aq)
ΔH
1=akJ·mol
−1Cl
2(g)+H
2O(l)=HCl(aq)+HClO(aq)
ΔH
2=bkJ·mol
−1试写出Na
2SO
3(aq)与HClO(aq)反应的热化学方程式:
________。
Ⅱ.红矾钠(Na
2Cr
2O
7·2H
2O)是重要的化工原料,工业上用铬铁矿(主要成分是FeO·Cr
2O
3)制备红矾钠的过程中会发生如下反应:4FeO(s)+4Cr
2O
3(s)+8Na
2CO
3(s)+7O
2(g)

8Na
2CrO
4(s)+2Fe
2O
3(s)+8CO
2(g)
ΔH<0
(1)请写出上述反应的化学平衡常数表达式:K=
_________。
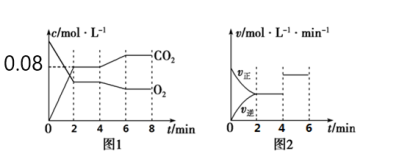
(2)如图1所示,在0~2min内CO
2的平均反应速率为
_______。
(3)图1、图2表示上述反应在2min时达到平衡、在4min时因改变某个条件而发生变化的曲线。由图1判断,反应进行至4min时,曲线发生变化的原因是
______(用文字表达);由图2判断,4min到6min的曲线变化的原因可能是
____(填写序号)。
a.升高温度
b.加催化剂
c.通入O
2 d.缩小容器体积
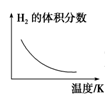
(4)工业上可用上述反应中的副产物CO
2来生产甲醇:CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g)。已知该反应能自发进行,则下列图象正确的是
______。
A.

B.

C.

D.