氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)“维生素C可以将食物中的 转化为
转化为 ”,说明维生素C具有
”,说明维生素C具有_____ (填“氧化性”或“还原性”)。
(2) 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下:
_____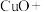 _____
_____
 _____
_____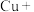 _____
_____ _____
_____ _____
_____
①配平上述氧化还原反应_____ 。
②该反应中,氧化剂是_____ (填化学式),被氧化的元素是_____ (填元素名称)。
(3)二氧化氯是一种高效消毒剂。工业上制备 的反应为
的反应为
①该反应中的还原产物是_____ (写化学式),反应中每生成1个 分子,转移电子的数目为
分子,转移电子的数目为_____ 。
②用双线桥标出反应中电子转移的方向和数目_____ 。
③ 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是_____ (填序号)
A. B.
B. C.KI D.
C.KI D.
(4)双氧水是公认的绿色氧化剂。已知氧化性强弱顺序为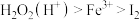 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为_____ 。
(1)“维生素C可以将食物中的
 转化为
转化为 ”,说明维生素C具有
”,说明维生素C具有(2)
 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下:_____
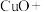 _____
_____
 _____
_____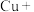 _____
_____ _____
_____ _____
_____
①配平上述氧化还原反应
②该反应中,氧化剂是
(3)二氧化氯是一种高效消毒剂。工业上制备
 的反应为
的反应为
①该反应中的还原产物是
 分子,转移电子的数目为
分子,转移电子的数目为②用双线桥标出反应中电子转移的方向和数目
③
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是A.
 B.
B. C.KI D.
C.KI D.
(4)双氧水是公认的绿色氧化剂。已知氧化性强弱顺序为
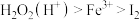 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
更新时间:2023-07-05 09:47:22
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】肼(N2H4)和亚硝酸钠在化工生产及航天工业中具有十分广泛的应用,下图是以液氨为原料生产肼和亚硝酸钠的工艺流程(肼能与水混溶,形成稳定的N2H4•H2O):
回答下列问题:
(1)NaNO2中N的化合价为_______ 。
(2)写出在NaClO溶液中通入NH3得到成品液1的化学反应方程式:______________ 。
(3)由成品液2得到成品固体混合物需经过的操作步骤为________________ 。
(4)亚硝酸钠在一定条件下能与无水肼反应生成一种钠氮化合物和水,生成的钠氮化合物中钠的质量分数为35.38%。则反应中氧化剂与还原剂的物质的量之比为_____ ;该反应中的氧化产物是___________________ 。
(5)已知所得成品固体混合物中含有2种钠盐,若要获得NaNO2产品,则需要除去的物质为_______ (填化学式);使用Pb进行处理时,杂质能转变为NaNO2,而Pb转化成PbO,则这一处理过程发生反应的化学方程式为___________ ;已知,NaNO2在邻苯二甲酸二丁酯中溶解度远大于在水中的溶解度,而另一钠盐则不具有该性质,若用有机溶剂邻苯二甲酸二丁酯处理成品固体混合物水溶液时,NaNO2 与另一钠盐通过_____ (填操作名称)被分离。

回答下列问题:
(1)NaNO2中N的化合价为
(2)写出在NaClO溶液中通入NH3得到成品液1的化学反应方程式:
(3)由成品液2得到成品固体混合物需经过的操作步骤为
(4)亚硝酸钠在一定条件下能与无水肼反应生成一种钠氮化合物和水,生成的钠氮化合物中钠的质量分数为35.38%。则反应中氧化剂与还原剂的物质的量之比为
(5)已知所得成品固体混合物中含有2种钠盐,若要获得NaNO2产品,则需要除去的物质为
您最近一年使用:0次
【推荐2】回答下列问题
(1)铁合金的硬度比各成分硬度___________ 。(填“大”,“小”或“不变”)
(2)向50mL沸水中加入5~6滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用___________ 来证明得到的分散系是氢氧化铁胶体。
(3)NaHCO3固体溶于水的电离方程式为___________ 。
(4)已知:Ⅰ. ;Ⅱ.
;Ⅱ. 。可推知
。可推知 、
、 、
、 氧化性由强到弱为
氧化性由强到弱为___________ 。
(5)Al2O3是碱性氧化物吗?___________ (填“是”或“不是”)。
(6)饮用水中的NO 对人类健康产生危害,为了降低饮用水中NO
对人类健康产生危害,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为: 10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2H2O
还原为N2,其化学方程式为: 10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2H2O
请回答下列问题:
①在化学方程式上用单线桥标出该反应中电子转移的方向和数目:___________ 。
②上述反应中若生成标准状况下3.36LN2,则转移的电子数目为:___________ 。
(1)铁合金的硬度比各成分硬度
(2)向50mL沸水中加入5~6滴饱和
 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用(3)NaHCO3固体溶于水的电离方程式为
(4)已知:Ⅰ.
 ;Ⅱ.
;Ⅱ. 。可推知
。可推知 、
、 、
、 氧化性由强到弱为
氧化性由强到弱为(5)Al2O3是碱性氧化物吗?
(6)饮用水中的NO
 对人类健康产生危害,为了降低饮用水中NO
对人类健康产生危害,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,其化学方程式为: 10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2H2O
还原为N2,其化学方程式为: 10Al + 6NaNO3 + 4NaOH = 10NaAlO2 + 3N2↑ + 2H2O请回答下列问题:
①在化学方程式上用单线桥标出该反应中电子转移的方向和数目:
②上述反应中若生成标准状况下3.36LN2,则转移的电子数目为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有下列物质:①氢氧化钡固体 ②KHSO4 ③HNO3 ④稀硫酸 ⑤二氧化碳气体 ⑥铜 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩CuSO4·5H2O晶体。请用序号填空:
(1)上述状态下可导电的是_________ 。
(2)属于电解质的是_________ 。
(3)属于非电解质的是_________ 。
(4)②在水溶液中的电离方程式为_________ ①与②在溶液中反应使溶液呈中性的离子方程式为_________ 。
(5)写出物质①和④在水中反应的离子反应方程式:_________ 。
(6)③与⑥可以发生如下反应,请配平方程:_________ 。
_________Cu+_________HNO3(浓)=_________Cu(NO3)2+_________NO2↑+_________H2O
回答下列问题:
I.还原剂是_________ 还原产物是_________
II.当有2molHNO3参加反应时,被氧化的物质的质量为_________ g。
III.用双线桥表示该反应电子转移的方向和数目_________ 。
(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)②在水溶液中的电离方程式为
(5)写出物质①和④在水中反应的离子反应方程式:
(6)③与⑥可以发生如下反应,请配平方程:
_________Cu+_________HNO3(浓)=_________Cu(NO3)2+_________NO2↑+_________H2O
回答下列问题:
I.还原剂是
II.当有2molHNO3参加反应时,被氧化的物质的质量为
III.用双线桥表示该反应电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】选择性催化还原法(SCR)是指在一定温度和催化剂下,适当通入空气,以氨为还原剂,将氮氧化物转化为无毒气体。_____ 。
2.此法仅限于低硫煤烟气脱硝,中高硫煤产生的高浓度二氧化硫会影响脱硝速率,可能的原因是_____ 。

2.此法仅限于低硫煤烟气脱硝,中高硫煤产生的高浓度二氧化硫会影响脱硝速率,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】依据物质类别和元素价态,可以对物质的性质进行解释和预测。
Ⅰ.有两种含氧物质: 、
、
(1)其中氧元素的化合价分别为_______ 价_______ 价
(2)从氧化剂和还原剂的角度,分析反应中的 作用。请完成下表内容。
作用。请完成下表内容。
(3)由 、
、 的名称可推知
的名称可推知 的名称为
的名称为_______ 。
(4)写出 与
与 反应的化学方程式
反应的化学方程式_______ , 与
与 一样,也可以做供氧剂。
一样,也可以做供氧剂。
Ⅱ.亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒。
而中毒。
(5)误食 后可服用维生素C解毒。下列分析正确的是_______(填序号)。
后可服用维生素C解毒。下列分析正确的是_______(填序号)。
(6)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过150毫克,以此计算,300克15%的亚硝酸钠溶液至少可用于生产火腿肠_______ 千克。
(7)亚硝酸钠在320℃时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目_______ 。

Ⅰ.有两种含氧物质:
 、
、
(1)其中氧元素的化合价分别为
(2)从氧化剂和还原剂的角度,分析反应中的
 作用。请完成下表内容。
作用。请完成下表内容。| 序号 | 化学反应方程式 | 作用 |
| ① |  | |
| ② |  作氧化剂 作氧化剂 | |
| ③ | 是氧化还原反应,但 既不作氧化剂,又不作还原剂 既不作氧化剂,又不作还原剂 | |
| ④ |  既作氧化剂,又作还原剂 既作氧化剂,又作还原剂 |
 、
、 的名称可推知
的名称可推知 的名称为
的名称为(4)写出
 与
与 反应的化学方程式
反应的化学方程式 与
与 一样,也可以做供氧剂。
一样,也可以做供氧剂。Ⅱ.亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒。
而中毒。(5)误食
 后可服用维生素C解毒。下列分析正确的是_______(填序号)。
后可服用维生素C解毒。下列分析正确的是_______(填序号)。A. 被还原 被还原 | B.维生素C被还原,表现出还原性 |
C.还原性:维生素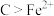 | D. 是还原剂 是还原剂 |
(7)亚硝酸钠在320℃时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。请填写并配平该反应的化学方程式,并用双线桥法标出此反应的电子得失和数目

您最近一年使用:0次
【推荐3】氧化剂和还原剂在生产生活中应用非常广泛。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝石(KNO3)、木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是_______ ,还原剂是_______ ,氧化产物是_______ ,还原产物是_______ 。
(2)水是生命之源,在常温常压下为无色无味液体,作为一种化学物质,水也会参与很多化学反应,如:
①2Na+2H2O=2NaOH+H2↑
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2H2O=2H2↑+O2↑
以上反应中,H2O只作氧化剂的是_______ ;H2O只作还原剂的是_______ ;H2O既作氧化剂,又作还原剂的是_______ ;H2O既不作氧化剂,又不作还原剂的是_______ 。
(3)高锰酸钾和浓盐酸可以发生如下反应制备氯气(Cl2):2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①已知KMnO4和MnCl2皆属于可溶盐,写出该反应的离子方程式_______ ;
②抄写化学方程式,用单线桥法标出电子转移的方向和数目_______ ;
③其中,氧化剂和还原剂的个数比为_______ 。
④在酸性溶液中,氧化性:KMnO4_______ Cl2(填大于或小于)。
(4)次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2的化学方程式:_______ 。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝石(KNO3)、木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是
(2)水是生命之源,在常温常压下为无色无味液体,作为一种化学物质,水也会参与很多化学反应,如:
①2Na+2H2O=2NaOH+H2↑
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2H2O=2H2↑+O2↑
以上反应中,H2O只作氧化剂的是
(3)高锰酸钾和浓盐酸可以发生如下反应制备氯气(Cl2):2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①已知KMnO4和MnCl2皆属于可溶盐,写出该反应的离子方程式
②抄写化学方程式,用单线桥法标出电子转移的方向和数目
③其中,氧化剂和还原剂的个数比为
④在酸性溶液中,氧化性:KMnO4
(4)次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2的化学方程式:
您最近一年使用:0次
【推荐1】NaNO2有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。
(1)下列说法正确的是__________ 。
A.解毒剂美蓝应该具有氧化性 B.中毒时亚硝酸盐发生氧化反应
C.解毒时高铁血红蛋白被还原 D.中毒过程中血红蛋白显氧化性
(2)已知NaNO2 能发生如下反应:NaNO2 + HI → NO + I2 + NaI + H2O,从上述反应推知__________ 。
A.氧化性:I2>NaNO2 B.氧化性:NaNO2>HI
C.还原性:HI>NO D.还原性:I2>HI
当有0.75mol HI被氧化时,在标准状况下产生气体的体积是_______ L。
(3)根据上述反应可用试纸和生活中常见的物质进行实验,鉴别NaNO2和NaCl ,现供选用的物质有①白酒、②碘化钾淀粉试纸、③淀粉、④白糖、⑤食醋,进行本实验时,可以选用的物质至少有___________ (填序号)。
(4)某工厂的废液中含有2%~5%的NaNO2直接排放会造成污染,下列试剂中①NaCl、②NH4Cl、③HNO3、④浓H2SO4,能使NaNO2转化为N2的是_________ (填序号)。
(1)下列说法正确的是
A.解毒剂美蓝应该具有氧化性 B.中毒时亚硝酸盐发生氧化反应
C.解毒时高铁血红蛋白被还原 D.中毒过程中血红蛋白显氧化性
(2)已知NaNO2 能发生如下反应:NaNO2 + HI → NO + I2 + NaI + H2O,从上述反应推知
A.氧化性:I2>NaNO2 B.氧化性:NaNO2>HI
C.还原性:HI>NO D.还原性:I2>HI
当有0.75mol HI被氧化时,在标准状况下产生气体的体积是
(3)根据上述反应可用试纸和生活中常见的物质进行实验,鉴别NaNO2和NaCl ,现供选用的物质有①白酒、②碘化钾淀粉试纸、③淀粉、④白糖、⑤食醋,进行本实验时,可以选用的物质至少有
(4)某工厂的废液中含有2%~5%的NaNO2直接排放会造成污染,下列试剂中①NaCl、②NH4Cl、③HNO3、④浓H2SO4,能使NaNO2转化为N2的是
您最近一年使用:0次
【推荐2】已知反应:
ⅰ.
ⅱ.
ⅲ.
(1)反应ⅰ中,做氧化剂的是___________ ,氯元素的化合价___________ (填“升高”或“降低”)。在该反应中,若消耗了1mol ,生成
,生成
___________ mol,转移电子的物质的量为___________ mol。
(2)依据ⅰ、ⅱ、ⅲ判断,物质氧化性由强到弱的顺序是___________ 。
ⅰ.

ⅱ.

ⅲ.

(1)反应ⅰ中,做氧化剂的是
 ,生成
,生成
(2)依据ⅰ、ⅱ、ⅲ判断,物质氧化性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)按如图所示操作,充分反应后:

①Ⅰ中铁丝上观察到的现象是______________________ ;
②Ⅱ中发生反应的离子方程式为_______________________ ;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_____________ 。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热。
①写出制备氢氧化铁胶体的化学方程式____________________ .
②向氢氧化铁胶体中逐滴滴入过量盐酸,出现的实验现象为:___________________________

①Ⅰ中铁丝上观察到的现象是
②Ⅱ中发生反应的离子方程式为
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热。
①写出制备氢氧化铁胶体的化学方程式
②向氢氧化铁胶体中逐滴滴入过量盐酸,出现的实验现象为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知反应:①
②
③
④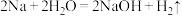
⑤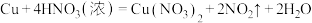
(1)上述反应中,属于置换反应的是___________ (填序号,下同);同一元素之间发生氧化还原的是___________ 。
(2)反应②中氧化剂是___________ (填化学式,下同);反应③中氧化产物是___________ 。
(3)在反应④中,每生成1个 分子时,转移的电子数为
分子时,转移的电子数为___________ 。
(4)在反应⑤中,氧化剂与还原剂的质量之比为___________ (填最简整数比)。

②

③

④
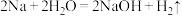
⑤
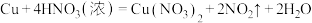
(1)上述反应中,属于置换反应的是
(2)反应②中氧化剂是
(3)在反应④中,每生成1个
 分子时,转移的电子数为
分子时,转移的电子数为(4)在反应⑤中,氧化剂与还原剂的质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列六种物质:
①液态HCl② 溶液③KOH固体④
溶液③KOH固体④ ⑤熔融
⑤熔融 ⑥
⑥ 胶体⑦
胶体⑦ ,请回答下列问题。
,请回答下列问题。
(1)上述物质中,属于电解质的是_______ ;(填写物质的序号,下同);属于非电解质的是_______ ;在题中状态下既是电解质又能导电的是_______ ;写出 的电离方程式:
的电离方程式:_______ 。
(2)②与少量 溶液反应的离子方程式为:
溶液反应的离子方程式为:_______ 。
(3)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备 气体的反应原理如下:
气体的反应原理如下:
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______NaCl
_______NaCl
配平上述方程式,并标出电子转移的方向和数目(单线桥)_______ 。
(4)该反应中,被还原的元素是_______ ;转移1mol电子时,生成气体的物质的量是_______ 。
①液态HCl②
 溶液③KOH固体④
溶液③KOH固体④ ⑤熔融
⑤熔融 ⑥
⑥ 胶体⑦
胶体⑦ ,请回答下列问题。
,请回答下列问题。(1)上述物质中,属于电解质的是
 的电离方程式:
的电离方程式:(2)②与少量
 溶液反应的离子方程式为:
溶液反应的离子方程式为:(3)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备
 气体的反应原理如下:
气体的反应原理如下:_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______NaCl
_______NaCl配平上述方程式,并标出电子转移的方向和数目(单线桥)
(4)该反应中,被还原的元素是
您最近一年使用:0次



