(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目:
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
相似题推荐
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O
+14H+=6Fe3++2Cr3++7H2O回答下列问题:
(1)该反应中,还原剂是
(2)实验室需要配制500mL0.1mol·L-1FeSO4溶液。。
①需要用托盘天平称取FeSO4·7H2O的质量
②在保存FeSO4溶液时,需加入少量铁粉,其目的是
③配制FeSO4溶液时,需要一系列操作,请写出下列图示所表示的操作名称。

④下列操作会造成所配FeSO4溶液物质的量浓度偏低的是
A.容量瓶在使用前未干燥,底部有少量蒸馏水
B.用于溶解FeSO4·7H2O固体后的烧杯和玻璃棒未洗涤
C.定容时俯视容量瓶刻度线
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水补至刻度线
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(1)H3PO2是一元弱酸,写出其电离方程式:
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于对器皿实现化学镀银。
①H3PO2中,P元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化产物为H3PO4,则氧化剂与还原剂的物质的量之比为
③NaH2PO2为
II.现有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目
(2)Cl2、SO2和KMnO4的氧化性由强到弱的顺序为
【推荐1】在抗击新型冠状病毒疫情期间,酸性KMnO4、NaClO、H2O2等被广泛用于此次抗疫行动中。
(1)向浸泡铜片的稀硫酸中加入H2O2后,铜片溶解,该反应的离子方程式为
(2)取300mL 0.3mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量为
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
①简要说明K2FeO4作为水处理剂时所起的作用
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾,原因是
(4)NaClO是“84”消毒液的有效成分,含氯消毒剂中HClO的消毒效果远高于ClO-。
①“84”消毒液必须避光密封保存,目的是防止与空气中的CO2反应而变质,该反应的离子方程式为
②过量NaClO溶液可使酸性废水中NH4+完全转化为N2,该反应的离子方程式为

(1)氨气在“氧化炉”中所发生反应的化学方程式为
(2)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
②NaClO溶液氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为NO
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示: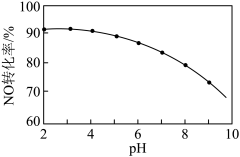
I.在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO
 ,其离子方程式:
,其离子方程式:II. NaClO溶液的初始pH越小,NO转化率越高。其原因是
(3)国家规定地下水中氮氧化物的排放标准不超过 400 mg∙L-1。氮氧化物可以用酸性硫酸亚铁溶液来吸收,反应原理为:NO+ Fe2+=Fe(NO)2+;NO2+ 3Fe2++ 2H+=2Fe3++ Fe(NO)2++ H2O。现测定某地下水脱硝过程中氮氧化物的排放量:收集500.00 mL排放的气体,缓慢通过250.00 mL 0.6240 mol∙L-1 酸性FeSO4溶液(过量),充分反应,量取吸收气体后的溶液25.00 mL置于锥形瓶中,用0.2000 mol∙L-1 酸性KMnO4溶液反应过量的Fe2+(还原产物为Mn2+),重复上述实验操作3次,平均消耗酸性KMnO4溶液的体积为15.00 mL。试通过计算分析地下水脱硝过程中氮氧化物的排放是否符合国家标准(写出计算过程)
(1)铝元素在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为食品污染源之一而加以控制.铝及其化合物在下列场合使用时必须严格加以控制的是
A.用明矾净水 B.制电线电缆 C.制包糖果用的铝箔
(2)
(3)盛装
 溶液的试剂瓶不能用玻璃塞的原因是
溶液的试剂瓶不能用玻璃塞的原因是(4)当人体缺铁时,往往需要吃补铁保健品,人体能够吸收的是
 ,但
,但 很容易被氧化.检验某固体补铁剂中铁元素是否被氧化的方法是
很容易被氧化.检验某固体补铁剂中铁元素是否被氧化的方法是(5)胃舒平[主要成分为
 ]是一种治疗胃酸过多的药物,写出胃舒平与胃酸反应的离子方程式
]是一种治疗胃酸过多的药物,写出胃舒平与胃酸反应的离子方程式(6)
 是一种有毒气体,如果泄漏会造成严重的环境污染.化工厂检验
是一种有毒气体,如果泄漏会造成严重的环境污染.化工厂检验 是否泄漏的反应方程式为
是否泄漏的反应方程式为 ,若反应中消耗
,若反应中消耗 ,则被氧化的
,则被氧化的 的体积为
的体积为(1)请用双线桥表明上述方程式中电子转移的方向和数目
(2)该反应中的浓HCl体现了
A.氧化性 B.还原性 C.既有氧化性又有还原性 D.酸性
(3)该反应中的氧化剂是
(4)若要制备标准状况下3.36L的Cl2,则参加反应的KMnO4固体质量为
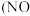 、
、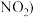 用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。
用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。(1)实验室可用加热亚硝酸钠与氯化铵的浓溶液制取氮气,写出该反应的化学方程式:
 酸性溶液中,可观察到溶液的颜色由
酸性溶液中,可观察到溶液的颜色由 (2)写出氮氧化物
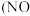 、
、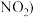 与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式:
与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式: 溶液吸收
溶液吸收 可生成
可生成 ,
, 和
和 溶液完全反应时转移电子
溶液完全反应时转移电子 ,则反应的离子方程式为
,则反应的离子方程式为 (3)从下列试剂中选用部分试剂鉴别亚硝酸钠、硝酸钠和氯化钠三种无色溶液,它们是
A.稀盐酸
 溶液
溶液  稀硝酸
稀硝酸  氢氧化钠溶液
氢氧化钠溶液(4)等物质的量浓度的亚硝酸钠、氯化钠、碳酸钠三种溶液中阴离子总浓度由大到小的顺序是
 填溶液中溶质的化学式
填溶液中溶质的化学式 。
。(5)工业品硝酸钠含少量杂质
 、
、 、NaCl、水不溶物
、NaCl、水不溶物 ,某同学欲测定工业品硝酸钠的纯度,进行了如下实验:
,某同学欲测定工业品硝酸钠的纯度,进行了如下实验: 称取
称取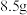 干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL
干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL  的A溶液
的A溶液 足量
足量 ,充分反应后过滤;
,充分反应后过滤; 向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液;
向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液; 取
取 所配溶液于锥形瓶中,加入少量B物质,再用
所配溶液于锥形瓶中,加入少量B物质,再用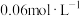 的
的 溶液滴定,用去
溶液滴定,用去 溶液
溶液 。
。(有关反应为:
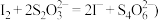
①A溶液中的溶质的化学式是
②B物质是
③若该同学操作正确,但结果造成测定结果略偏高,其原因可能是
 任写一点
任写一点



