(1)铁钉在氯气中被锈蚀为棕褐色物质FeCl3,而在盐酸中生成浅绿色的FeCl2溶液。在Cl2、Cl-、H+中,具有氧化性的是____________ ,其中氧化性最强的是____________ 。
(2)盐酸在不同的反应中可以分别表现出酸性、氧化性和还原性。现在有如下三个反应,请写出盐酸在三个反应中分别起何种作用:
①Zn+2HCl===ZnCl2+H2↑____________________ ;
②NaOH+HCl===NaCl+H2O__________________ ;
③2HCl H2↑+Cl2↑
H2↑+Cl2↑________________________ 。
(3)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成浅绿色溶液(FeCl2);向浓盐酸中滴加KMnO4溶液产生淡黄绿色气体(Cl2)。在Cl2、H+、 中,
中,__________________ 氧化性最强。
(4)高锰酸钾与氢溴酸溶液可以发生下列反应:2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O。其中还原剂是________________ 。若消耗15.8 g氧化剂,则被氧化的还原剂的质量是______________ g。HBr的作用是____________________ 。
(2)盐酸在不同的反应中可以分别表现出酸性、氧化性和还原性。现在有如下三个反应,请写出盐酸在三个反应中分别起何种作用:
①Zn+2HCl===ZnCl2+H2↑
②NaOH+HCl===NaCl+H2O
③2HCl
 H2↑+Cl2↑
H2↑+Cl2↑(3)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成浅绿色溶液(FeCl2);向浓盐酸中滴加KMnO4溶液产生淡黄绿色气体(Cl2)。在Cl2、H+、
 中,
中,(4)高锰酸钾与氢溴酸溶液可以发生下列反应:2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O。其中还原剂是
更新时间:2018-12-05 08:52:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】甘肃马家窑遗址(今临洮县)出土的青铜刀,是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,其化学式为Cu2(OH)2CO3,“铜绿”能跟酸反应生成铜盐、CO2和H2O。
(1)CO2属于_______ 氧化物。(填“酸性”或“碱性”)
(2)从物质分类标准看,“铜绿”属于哪类物质_______。(填选项)
(3)铜器表面有时会生成“铜绿”,这层“铜绿”可用化学方法除去,写出盐酸去除“铜绿”的化学方程式:_______ 。
(4)古代人们高温灼烧孔雀石[Cu(OH)2·CuCO3]和木炭的混合物得到一种紫红色的金属铜,其化学反应方程式为2CuO+C 2Cu+CO2↑,该反应属于_______。
2Cu+CO2↑,该反应属于_______。
(5)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:反应I:2Cu2S+3O2 2Cu2O +2SO2 ,反应II:Cu2S+2Cu2O
2Cu2O +2SO2 ,反应II:Cu2S+2Cu2O 6Cu+SO2↑
6Cu+SO2↑
请回答下列问题:
①反应I中,氧化产物是_______ ,用单线桥标出反应I中电子转移的方向和数目_______ ;
②反应 II 中,Cu2O的作用是_______ 。(填“氧化剂”“还原剂”或“氧化剂和还原剂”)
(1)CO2属于
(2)从物质分类标准看,“铜绿”属于哪类物质_______。(填选项)
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(4)古代人们高温灼烧孔雀石[Cu(OH)2·CuCO3]和木炭的混合物得到一种紫红色的金属铜,其化学反应方程式为2CuO+C
 2Cu+CO2↑,该反应属于_______。
2Cu+CO2↑,该反应属于_______。| A.化合反应 | B.复分解反应 | C.氧化还原反应 | D.离子反应 |
 2Cu2O +2SO2 ,反应II:Cu2S+2Cu2O
2Cu2O +2SO2 ,反应II:Cu2S+2Cu2O 6Cu+SO2↑
6Cu+SO2↑请回答下列问题:
①反应I中,氧化产物是
②反应 II 中,Cu2O的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】生活无处不化学,例如生活中常见消毒剂:臭氧、“84”消毒液、二氧化氯、高铁酸钠等。
(1)臭氧和氧气互为___________ (填“同位素”或“同素异形体”),它们在一定条件下可以相互转化,该变化过程属于___________ (填“氧化还原反应”或“非氧化还原反应”)。
(2)常温下,将氯气通入 溶液中,可以制得“84”消毒液,写出发生反应的离子方程式:
溶液中,可以制得“84”消毒液,写出发生反应的离子方程式:___________ ,该消毒液的有效成分是___________ (填化学式)。生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是___________ 。
(3) 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得: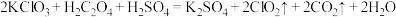 。产生
。产生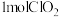 时,转移的电子的物质的量为
时,转移的电子的物质的量为___________ ;该反应中的氧化剂是___________ (填化学式)。
(4)高铁酸钠 是一种新型的净水剂。其净水过程中发生的化学反应主要为
是一种新型的净水剂。其净水过程中发生的化学反应主要为 ,证明有
,证明有 胶体生成的实验操作为
胶体生成的实验操作为___________ 。
(1)臭氧和氧气互为
(2)常温下,将氯气通入
 溶液中,可以制得“84”消毒液,写出发生反应的离子方程式:
溶液中,可以制得“84”消毒液,写出发生反应的离子方程式:(3)
 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得: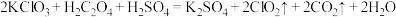 。产生
。产生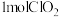 时,转移的电子的物质的量为
时,转移的电子的物质的量为(4)高铁酸钠
 是一种新型的净水剂。其净水过程中发生的化学反应主要为
是一种新型的净水剂。其净水过程中发生的化学反应主要为 ,证明有
,证明有 胶体生成的实验操作为
胶体生成的实验操作为
您最近一年使用:0次
【推荐3】氧化还原反应在生产、生活中有广泛的用途。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4═3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是_______ (填化学式,下同),还原剂是_______ ,氧化产物和还原产物的个数比是_______ 。
Ⅱ.工业废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+═6Fe3++2Cr3++7H2O。
+14H+═6Fe3++2Cr3++7H2O。
(2)在该反应中,被氧化的是_______ (填离子符号,下同),还原产物是_______ ,此反应可以推断物质还原性强弱顺序是__________ 。
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2 +____+5H2O。
+____+5H2O。
(3)请完成该化学方程式并配平_______ 。
(4)该反应中生成2个 转移的电子数为
转移的电子数为_______ 。
(5)氧化还原反应配平
①_______S+_______KOH═_______K2S+_______K2SO3+_______H2O
②_______Fe(OH)3+_______CH4+_______H+=_______Fe2++_______HCO +_______H2O
+_______H2O
①_______ 。
②_______ 。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4═3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是
Ⅱ.工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+═6Fe3++2Cr3++7H2O。
+14H+═6Fe3++2Cr3++7H2O。(2)在该反应中,被氧化的是
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2
 +____+5H2O。
+____+5H2O。(3)请完成该化学方程式并配平
(4)该反应中生成2个
 转移的电子数为
转移的电子数为(5)氧化还原反应配平
①_______S+_______KOH═_______K2S+_______K2SO3+_______H2O
②_______Fe(OH)3+_______CH4+_______H+=_______Fe2++_______HCO
 +_______H2O
+_______H2O①
②
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)现有下列状态的物质①干冰 ②NaCl晶体 ③氨水 ④冰醋酸 ⑤酒精水溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖,其中属于电解质的是_________ ,能导电的是______________ 。
(2)配平方程式__________ Cu+ HNO3(稀)= Cu(NO3)2+ NO↑ + H2O,在该反应中,硝酸表现的性质有_________________ ,还原剂与氧化剂的物质的量之比为:___________ 。
(3)根据下列三个反应,判断物质的氧化性由强到弱的顺序正确的是_________
①2Fe3++S2-= 2Fe2++S↓ ②2Fe2++C12 = 2Fe3++2C1- ③2MnO4-+10Cl-+16H+ = 2Mn2++5Cl2↑+8H2O
A.MnO4->Cl2>Fe3+ B.Fe3+>Cl2>S
C.S>Cl2>Fe3+ D.Fe3+>C12>MnO4-
(2)配平方程式
(3)根据下列三个反应,判断物质的氧化性由强到弱的顺序正确的是
①2Fe3++S2-= 2Fe2++S↓ ②2Fe2++C12 = 2Fe3++2C1- ③2MnO4-+10Cl-+16H+ = 2Mn2++5Cl2↑+8H2O
A.MnO4->Cl2>Fe3+ B.Fe3+>Cl2>S
C.S>Cl2>Fe3+ D.Fe3+>C12>MnO4-
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铁及其重要化合物的“价类二维图”如下图所示。
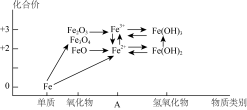
(1)该“价类二维图”中缺失的类别A应为_______ 。
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为_______。
(3)某实验小组在探究实验后,想要检验废液中是否存在Fe3+,该怎么做?_______ 。
(4)将足量铁粉投入溴化铁溶液中充分反应,写出该反应的化学方程式_______ 。
(5)在上述反应液中继续加入足量氯水,此时溶液中发生反应的离子方程式为_______ 。
(6)工业上曾经通过反应“3Fe+4NaOH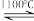 Fe3O4+2H2↑+4Na↑”生产金属钠,下列说法正确的是_______。
Fe3O4+2H2↑+4Na↑”生产金属钠,下列说法正确的是_______。

(1)该“价类二维图”中缺失的类别A应为
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为_______。
| A.干垃圾 | B.湿垃圾 | C.有毒有害垃圾 | D.可回收垃圾 |
(4)将足量铁粉投入溴化铁溶液中充分反应,写出该反应的化学方程式
(5)在上述反应液中继续加入足量氯水,此时溶液中发生反应的离子方程式为
(6)工业上曾经通过反应“3Fe+4NaOH
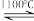 Fe3O4+2H2↑+4Na↑”生产金属钠,下列说法正确的是_______。
Fe3O4+2H2↑+4Na↑”生产金属钠,下列说法正确的是_______。| A.用磁铁可以将Fe与Fe3O4分离 | B.该反应条件下铁的氧化性比钠强 |
| C.每生成1 mol H2,转移的电子为4 mol | D.将生成的气体在空气中冷却可获得钠 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl H2O2+NaCl
H2O2+NaCl
B.Ag2O+H2O2 Ag+O2↑+H2O
Ag+O2↑+H2O
C.H2O2 H2O+O2↑
H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH K2CrO4+K2SO4+H2O
K2CrO4+K2SO4+H2O
H2O2仅体现氧化性的反应是___________ (填序号,下同),H2O2仅体现还原性的反应是___________ ,H2O2既体现氧化性又体现还原性的反应是___________ ,H2O2既不做氧化剂又不做还原剂的反应是___________ 。
(2)已知常温下在溶液中可发生如下两个反应:
Br2+2Fe2+=2Fe3++2Br-
2I-+2Fe3+=2Fe2++I2
由此可以确定Br2、I2、Fe3+的氧化性由强到弱的顺序是___________
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
①氧化剂是___________ ,还原剂是___________ 。
②氧化剂与还原剂的分子个数比为___________ 。
③当有68 g NH3参加反应时,被氧化的物质为___________ g,生成的还原产物为___________ g。
A.Na2O2+HCl
 H2O2+NaCl
H2O2+NaClB.Ag2O+H2O2
 Ag+O2↑+H2O
Ag+O2↑+H2OC.H2O2
 H2O+O2↑
H2O+O2↑D.H2O2+Cr2(SO4)3+KOH
 K2CrO4+K2SO4+H2O
K2CrO4+K2SO4+H2OH2O2仅体现氧化性的反应是
(2)已知常温下在溶液中可发生如下两个反应:
Br2+2Fe2+=2Fe3++2Br-
2I-+2Fe3+=2Fe2++I2
由此可以确定Br2、I2、Fe3+的氧化性由强到弱的顺序是
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
①氧化剂是
②氧化剂与还原剂的分子个数比为
③当有68 g NH3参加反应时,被氧化的物质为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.某溶液中只可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。
。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。
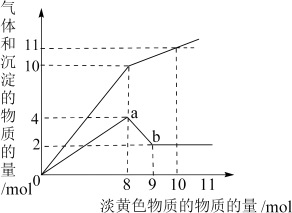
(1)该淡黄色物质做焰色反应实验显黄色。可知溶液中含有的离子是_______ ;所含离子的物质的量浓度之比为_______ ;所加的淡黄色固体是_______ 。
Ⅱ.湿法制备高铁酸钾 的反应体系中有六种粒子:
的反应体系中有六种粒子: 、
、 、
、 、
、 、
、 、
、 。
。
(2)写出并配平湿法制高铁酸钾反应的离子方程式:_______ 。
(3)每生成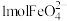 转移
转移_______  电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为
电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为_______  。
。
Ⅲ.已知在稀硫酸中, 和
和 能发生以下反应(均未配平):
能发生以下反应(均未配平):


(4)试比较在酸性条件下 、
、 、
、 、
、 氧化性的强弱:
氧化性的强弱:_______ 。
(5)以下离子方程式错误的是_______ (选填答案编号)。
a.
b.
c.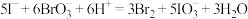
d.
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。
。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。
(1)该淡黄色物质做焰色反应实验显黄色。可知溶液中含有的离子是
Ⅱ.湿法制备高铁酸钾
 的反应体系中有六种粒子:
的反应体系中有六种粒子: 、
、 、
、 、
、 、
、 、
、 。
。(2)写出并配平湿法制高铁酸钾反应的离子方程式:
(3)每生成
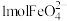 转移
转移 电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为
电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为 。
。Ⅲ.已知在稀硫酸中,
 和
和 能发生以下反应(均未配平):
能发生以下反应(均未配平):

(4)试比较在酸性条件下
 、
、 、
、 、
、 氧化性的强弱:
氧化性的强弱:(5)以下离子方程式错误的是
a.

b.

c.
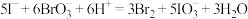
d.

您最近一年使用:0次
【推荐2】高锰酸钾是一种典型的强氧化剂,在生产、生活中有广泛应用。
(1)①请完成并配平下列化学方程式:___________ 。
_______KMnO4+______HCl(浓)=_______KCl+______MnCl2+______Cl2↑+__________
②HCl在上述反应中体现的性质有___________ 。
③氧化剂与还原剂的物质的量之比为___________ 。
④若标准状况下生成5.6L的气体,则转移电子的数目为___________ 。
(2)在用酸性KMnO4溶液处理Cu2S和CuS的混合物时,会发生如下反应: +Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平),下列关于该反应的说法错误的是___________(填序号)。
+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平),下列关于该反应的说法错误的是___________(填序号)。
(3)在稀硫酸中, 和H2O2也能发生氧化还原反应。
和H2O2也能发生氧化还原反应。
氧化反应:H2O2-2e-=2H++O2↑
还原反应: +5e-+8H+=Mn2++4H2O
+5e-+8H+=Mn2++4H2O
①若有0.2molH2O2参加此反应,转移的电子的物质的量为___________ mol,由上述反应可以得出物质氧化性强弱的结论是___________ 。
②已知:KMnO4+H2O2+H2SO4→K2SO4+MnSO4+O2↑+H2O(未配平),则被1molKMnO4氧化的H2O2的物质的量是___________ mol。
(1)①请完成并配平下列化学方程式:
_______KMnO4+______HCl(浓)=_______KCl+______MnCl2+______Cl2↑+__________
②HCl在上述反应中体现的性质有
③氧化剂与还原剂的物质的量之比为
④若标准状况下生成5.6L的气体,则转移电子的数目为
(2)在用酸性KMnO4溶液处理Cu2S和CuS的混合物时,会发生如下反应:
 +Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平),下列关于该反应的说法错误的是___________(填序号)。
+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平),下列关于该反应的说法错误的是___________(填序号)。| A.被氧化的元素是Cu和S |
| B.氧化剂与还原剂的物质的量之比为8∶5 |
| C.生成2.24L(标准状况下)SO2,转移电子的物质的量是0.8mol |
| D.还原性的强弱关系是Mn2+>Cu2S |
 和H2O2也能发生氧化还原反应。
和H2O2也能发生氧化还原反应。氧化反应:H2O2-2e-=2H++O2↑
还原反应:
 +5e-+8H+=Mn2++4H2O
+5e-+8H+=Mn2++4H2O①若有0.2molH2O2参加此反应,转移的电子的物质的量为
②已知:KMnO4+H2O2+H2SO4→K2SO4+MnSO4+O2↑+H2O(未配平),则被1molKMnO4氧化的H2O2的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。如图为氯元素的“价-类”二维图。
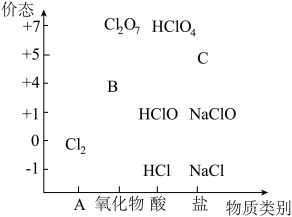
请回答下列问题:
(1)二维图中类别A是_______ ;B可以代替 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是_______ (填化学式,下同);C的焰色试验呈黄色,则C是_______ 。
(2)某同学利用①FeO、② 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与_______ (填序号)发生反应;从化合价角度看,盐酸中 具有
具有_______ 性,可能与(填序号)_______ 发生反应。
(3)实验室常用 固体和浓盐酸制取
固体和浓盐酸制取 ,可选用图中的
,可选用图中的_______ (填“A”或“B”)作为发生装置,反应的离子方程式为_______ 。

(4)若将84消毒液与双氧水混用给游泳池消毒,反应产生的 会促进藻类快速生长,使池水变绿,其反应原理为:
会促进藻类快速生长,使池水变绿,其反应原理为: 。
。
①该反应说明氧化性:NaClO_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②用单线桥法表示该反应电子转移的方向和数目:________ 。
(5)一定温度下, 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为_______ 。

请回答下列问题:
(1)二维图中类别A是
 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是(2)某同学利用①FeO、②
 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与 具有
具有(3)实验室常用
 固体和浓盐酸制取
固体和浓盐酸制取 ,可选用图中的
,可选用图中的
(4)若将84消毒液与双氧水混用给游泳池消毒,反应产生的
 会促进藻类快速生长,使池水变绿,其反应原理为:
会促进藻类快速生长,使池水变绿,其反应原理为: 。
。①该反应说明氧化性:NaClO
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②用单线桥法表示该反应电子转移的方向和数目:
(5)一定温度下,
 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】微型化学实验能有效减少污染,节约药品。下图中,某学生在衬有一张白纸的玻璃片上放置表面皿,在表面皿上的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,在表面皿中心处放置2小粒KMnO4晶体,并滴加一滴浓盐酸,立即将表面皿盖好。可见KMnO4晶体很快溶解,并产生气体

(1)①写出化学实验室中用MnO2制取Cl2的化学方程式______________________________ 。
②完成本实验中制取Cl2的化学方程式:
___________ KMnO4+__________ HCl(浓)——______ KCl+________ MnCl2+____ Cl2↑+______ _______
如该反应中消耗还原剂的物质的量为8mol,则电子转移数目为_________________ 。
(2)b处的实验现象为____________________________________________________ 。
c处的实验现象为____________________________________________________ 。
(3)d处反应的离子方程式为____________________ 、____________________ 。
(4)通过该实验能比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱,其氧化性由强到弱的顺序是_________________________________________ 。

(1)①写出化学实验室中用MnO2制取Cl2的化学方程式
②完成本实验中制取Cl2的化学方程式:
如该反应中消耗还原剂的物质的量为8mol,则电子转移数目为
(2)b处的实验现象为
c处的实验现象为
(3)d处反应的离子方程式为
(4)通过该实验能比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱,其氧化性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】根据信息回答以下与元素相关的问题。
I.汽车尾气中CO、NOx以及燃煤废气中的SO2都是大气污染物,对其治理具有重要意义。
(1)氧化-还原法消除NOx的转化:NO NO2
NO2 N2
N2
①反应I为NO+O3=NO2+O2,生成标准状况下11.2 L O2时,转移电子数目为___________ ;
②反应II中,当n(NO2):nCO(NH2)2=3:2时,氧化产物与还原产物的质量比为_________ ;
(2)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。装置II中酸性条件下,NO被Ce4+氧化的产物主要是 、
、 ,写出生成等物质的量的
,写出生成等物质的量的 和
和 时的离子方程式
时的离子方程式________ 。
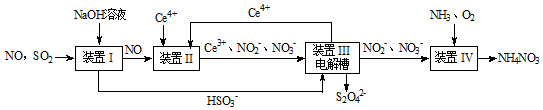
(3)已知进入装置IV的溶液中,NO2的浓度为a g/L,要使1m3该溶液中的 完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气
完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气______ L(用含a代数式表示,结果保留整数)。
II.镁、钙和锶(Sr)都属于碱土金属,具有相似的化学性质。
(1)锶比钙的金属性更强,它们的单质都能和水反应放出氢气,则锶与水反应的化学方程式为_______ 。颗粒状的单质锶与稀硫酸反应,反应现象不如钠和水反应剧烈,原因是_______ 。
(2)锶在一定条件下分别与N2、H2发生反应,生成Y、Z两种锶的固态化合物,Y、Z与水反应均可放出气体。0.01 mol Y溶于100 mL盐酸恰好完全反应,生成氯化物混合溶液,则盐酸的物质的量浓度为______ ,Z的电子式为_______ 。
I.汽车尾气中CO、NOx以及燃煤废气中的SO2都是大气污染物,对其治理具有重要意义。
(1)氧化-还原法消除NOx的转化:NO
 NO2
NO2 N2
N2①反应I为NO+O3=NO2+O2,生成标准状况下11.2 L O2时,转移电子数目为
②反应II中,当n(NO2):nCO(NH2)2=3:2时,氧化产物与还原产物的质量比为
(2)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。装置II中酸性条件下,NO被Ce4+氧化的产物主要是
 、
、 ,写出生成等物质的量的
,写出生成等物质的量的 和
和 时的离子方程式
时的离子方程式
(3)已知进入装置IV的溶液中,NO2的浓度为a g/L,要使1m3该溶液中的
 完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气
完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气II.镁、钙和锶(Sr)都属于碱土金属,具有相似的化学性质。
(1)锶比钙的金属性更强,它们的单质都能和水反应放出氢气,则锶与水反应的化学方程式为
(2)锶在一定条件下分别与N2、H2发生反应,生成Y、Z两种锶的固态化合物,Y、Z与水反应均可放出气体。0.01 mol Y溶于100 mL盐酸恰好完全反应,生成氯化物混合溶液,则盐酸的物质的量浓度为
您最近一年使用:0次



