21. 某科学小组制备硝基苯的实验装置如下,有关数据列如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g∙cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 不溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硫酸 | | 338 | 1.84 | 易溶于水 |
实验步骤如下:
取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制成混和酸,将混合酸小心地加入B中。把0.2mol(15.6g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,使溶液混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl
2颗粒,静置片刻,弃去CaCl
2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
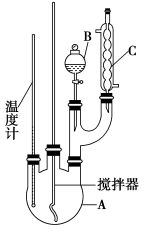
(1)图中B仪器的名称
___________,图中装置C的作用是
___________。
(2)制备硝基苯的化学方程式
___________。
(3)为了使反应在50~60℃下进行,常用的加热方式是
___________。反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是溶有的浓硝酸分解生成
___________,实验室常用氢氧化钠溶液除去该有色物质生成两种盐,涉及的离子方程式为
___________。
(4)将粗产品置于分液漏斗中加水,振荡后静置,产物应在
___________(填“上”或“下”)层,步骤中加入的无水CaCl
2的作用是
___________,若实验过程中省略该步操作,实验的产率
___________ (填“偏高”“偏低”或“不变”)。
(5)本实验所得到的硝基苯产率是
___________。(结果保留3位有效数字)