13. 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物的“价类二维图”。
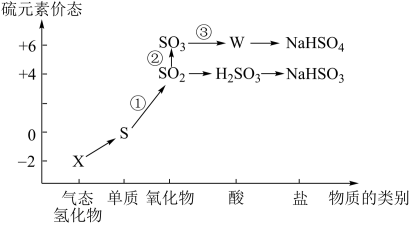
根据图示回答下列问题:
(1)X的化学式为
___________,将X与SO
2混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为
___________。
(2)过量的Fe粉与一定量W浓溶液混合加热反应,生成
___________(填化学式)气体。转化①可由S粉与热的W浓溶液反应实现,反应的化学方程式为
___________。
(3)欲制备Na
2S
2O
3,从氧化还原角度分析,下列合理的是
___________(选填字母)。
A.Na
2S+S B.Na
2SO
3+S C.Na
2SO
3+Na
2SO
4 D.SO
2+Na
2SO
3(4)工业制硫酸中,转化②是在
___________(填设备名称)进行的。进行转化③时,不用水而用98.3%的浓H
2SO
4吸收SO
3,原因是
___________。
(5)NaHSO
4溶液显强酸性,向NaHSO
4溶液中滴入Ba(OH)
2溶液,恰好使溶液呈中性,则发生反应的离子方程式为
___________。