17. 按照要求回答下列问题:
I.(1)已知:S
2Cl
2(l)+Cl
2(g)=2SCl
2(l) ΔH=-50.2 kJ·mol
-1。断裂1mol Cl—Cl键、1mol S—S键分别需要吸收243kJ、268kJ的能量,则断裂1mol S—Cl键需要吸收的能量为
______kJ。
(2)某容积不变的密闭容器中发生如下反应:2SO
2(g)+O
2(g)⇌2SO
3(g) △H=-197 kJ·mol
-1。
下列能说明反应达到平衡状态的是
_________。
a.体系压强保持不变
b.混合气体的密度保持不变
c.SO
3和O
2的体积比保持不变
d.每消耗1 mol SO
3的同时生成1 mol SO
2(3)如图所示,左侧石墨上通入

,右侧石墨上通入

,电解质溶液为

溶液。完成下列问题:

①负极反应式为
_______________________。
②放电时

向
_____(填“正”或“负”)极移动。
③当外电路通过电子的物质的量为
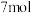
时,正极通入的

在标准状况下的体积为
_______(假设能量全部转化为电能)。
II.工业上硝酸的制备和自然界中硝酸的生成既有相同之处,又有区别。图中路线a、b、c是工业制备硝酸的主要途径,路线Ⅰ、Ⅱ、Ⅲ是雷电固氮过程中生成硝酸的途径。

(1)N
2在常温下性质很稳定,任意写出一种与此性质有关的用途:
_____。
(2)实验室制取NH
3的化学方程式为
_____。
(3)下列环境问题与氮的氧化物排放无关的是
_____。
a.酸雨
b.光化学烟雾
c.臭氧层空洞 d.白色污染
(4)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
_____(5)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H
2SO
4)=2.0 mol•L
-1,c(HNO
3)=1.0 mol•L
-1取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
___________L。