20. 某同学为验证元素周期表中元素性质的递变规律,设计了如下实验。
I.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
_____与盐酸反应最剧烈,
____与盐酸反应的速率最慢;
_____与盐酸反应产生的气体最多。
(2)向Na
2S溶液中通入氯气出现淡黄色浑浊,可证明C1的非金属性比S强,反应的离子方程式为:
_______________。
II.利用下图装置可验证同主族非金属性的变化规律。
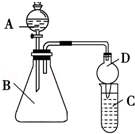
(3)仪器B的名称为
__________,干燥管D的作用为
___________。
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO
4(KMnO
4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到混合溶液
_____的现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用
_____溶液吸收尾气。
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO
3、C中加Na
2SiO
3溶液观察到C中溶液
______的现象,即可证明。但有的同学认为盐酸具有挥发性,应用
______溶液除去。