14. 二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(FeS
2,其中硫元素为-1价)在高温下和氧气反应制备SO
2:
4FeS
2+11O
2
8SO
2+2Fe
2O
3,该反应中被氧化的元素是
________(填元素符号)。当该反应转移2.75 mol电子时,生成的二氧化硫在标准状况下的体积为
________ L。
(2)实验室中用下列装置测定SO
2催化氧化为SO
3的转化率。(已知SO
3的熔点为16.8 ℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO
2的影响)
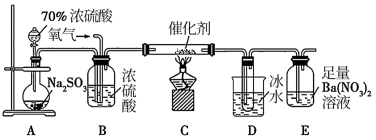
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作:
__________________。
②实验过程中,需要通入氧气。试写出一个用如下图所示装置制取氧气的化学方程式:
________________________________________________________________________。
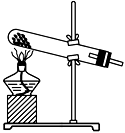
③当停止通入SO
2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
________________________________________________________________________。
④实验结束后,若装置D增加的质量为
m g,装置E中产生白色沉淀的质量为
n g,则此条件下二氧化硫的转化率是
________(用含字母的代数式表示,不用化简)。
(3)某学习小组设计用如图装置验证二氧化硫的化学性质。
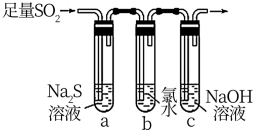
①能说明二氧化硫具有氧化性的实验现象为
___________________________________。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验。
方案Ⅰ:向第一份溶液中加入AgNO
3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液中加入BaCl
2溶液,产生白色沉淀
上述方案中合理的是
________(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为
________________________________________________________________。