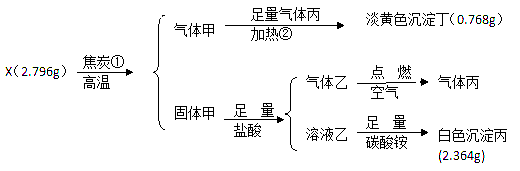
二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中硫元素为-1价)在高温下和氧气反应制备SO2:
4FeS2+11O2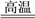 8SO2+2Fe2O3,该反应中被氧化的元素是
8SO2+2Fe2O3,该反应中被氧化的元素是________ (填元素符号)。当该反应转移2.75 mol电子时,生成的二氧化硫在标准状况下的体积为________ L。
(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率。(已知SO3的熔点为16.8 ℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响)
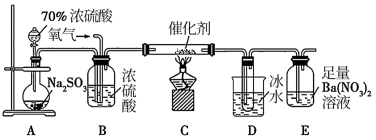
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作:__________________ 。
②实验过程中,需要通入氧气。试写出一个用如下图所示装置制取氧气的化学方程式:________________________________________________________________________ 。
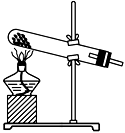
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是________________________________________________________________________ 。
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是________ (用含字母的代数式表示,不用化简)。
(3)某学习小组设计用如图装置验证二氧化硫的化学性质。
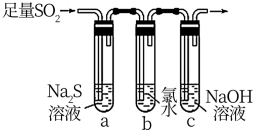
①能说明二氧化硫具有氧化性的实验现象为___________________________________ 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验。
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案中合理的是________ (填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为________________________________________________________________ 。
(1)工业上用黄铁矿(FeS2,其中硫元素为-1价)在高温下和氧气反应制备SO2:
4FeS2+11O2
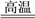 8SO2+2Fe2O3,该反应中被氧化的元素是
8SO2+2Fe2O3,该反应中被氧化的元素是(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率。(已知SO3的熔点为16.8 ℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作:
②实验过程中,需要通入氧气。试写出一个用如下图所示装置制取氧气的化学方程式:

③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是
(3)某学习小组设计用如图装置验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验。
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案中合理的是
15-16高一下·吉林松原·开学考试 查看更多[4]
(已下线)第五章 化工生产中的重要非金属元素(培优提升卷)-2020-2021学年高一化学必修第二册章末集训必刷卷(新教材人教版)2015-2016学年吉林松原油田高中高一下期初考试化学试卷四川省泸州市高级中学2016-2017学年高二3月月考化学试题四川省泸州高级中学2016-2017学年高一3月月考化学试题
更新时间:2017-07-08 10:54:52
|
相似题推荐
【推荐1】为验证氧化性Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。

已知:Na2SO3+H2SO4=SO2↑+Na2SO4+H2O
实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
Ⅶ.实验结束后,打开弹簧夹K1~K4,再通入一段时间N2,然后拆卸,洗涤,整理仪器。
(1)A中反应的化学方程式为_______ 。
(2)棉花中浸润的溶液是_______ 。
(3)步骤Ⅲ中溶液变黄的离子方程式是_______ ,能说明氧化性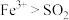 的离子方程式是
的离子方程式是_______ 。
(4)过程Ⅶ的目的是_______ 。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性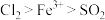 的是
的是_______ (填“甲”、“乙”、“丙”)。
(6)将B中的 溶液换成
溶液换成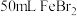 溶液并向其中通入
溶液并向其中通入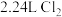 (标准状况下),若溶液中有
(标准状况下),若溶液中有 的
的 被氧化成单质
被氧化成单质 ,则原
,则原 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为_______ 。

已知:Na2SO3+H2SO4=SO2↑+Na2SO4+H2O
实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
Ⅶ.实验结束后,打开弹簧夹K1~K4,再通入一段时间N2,然后拆卸,洗涤,整理仪器。
(1)A中反应的化学方程式为
(2)棉花中浸润的溶液是
(3)步骤Ⅲ中溶液变黄的离子方程式是
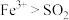 的离子方程式是
的离子方程式是(4)过程Ⅶ的目的是
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性
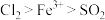 的是
的是| 过程Ⅳ B溶液中含有的离子 | 过程Ⅵ B溶液中含有的离子 | |
| 甲 | 既有 又有 又有 | 有 |
| 乙 | 有 无 无 | 有 |
| 丙 | 有 无 无 | 有 |
(6)将B中的
 溶液换成
溶液换成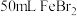 溶液并向其中通入
溶液并向其中通入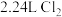 (标准状况下),若溶液中有
(标准状况下),若溶液中有 的
的 被氧化成单质
被氧化成单质 ,则原
,则原 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】实验题
实验室制取乙烯是用乙醇跟浓硫酸反应,常因温度过高而发生副反应生成炭黑、二氧化硫、二氧化碳和水蒸气。请用如图编号为①~⑥的实验装置,设计一个实验,以验证上述反应后的混合气体中含有二氧化硫、二氧化碳和水蒸气。

(1)用装置的编号表示其连接顺序(按气体产物从左到右的流向)(6)→( )→(3)→( )→( )→( )____
(2)装置⑤中的固体药品为____ ,用以验证的产物是____ 。
(3)装置④中的溶液是____ ,用以验证的产物是____ 。
(4)装置①中的品红溶液的作用_____ 。
(5)装置②中溴水的作用是____ 。写出②中可能发生的2个化学方程式____ 、____ 。
实验室制取乙烯是用乙醇跟浓硫酸反应,常因温度过高而发生副反应生成炭黑、二氧化硫、二氧化碳和水蒸气。请用如图编号为①~⑥的实验装置,设计一个实验,以验证上述反应后的混合气体中含有二氧化硫、二氧化碳和水蒸气。

(1)用装置的编号表示其连接顺序(按气体产物从左到右的流向)(6)→( )→(3)→( )→( )→( )
(2)装置⑤中的固体药品为
(3)装置④中的溶液是
(4)装置①中的品红溶液的作用
(5)装置②中溴水的作用是
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】由碳酸锰矿(主要成分MnCO3,还含有FeCO3、MnO2、Al2O3、SiO2等)中提取金属锰的一种流程如图:
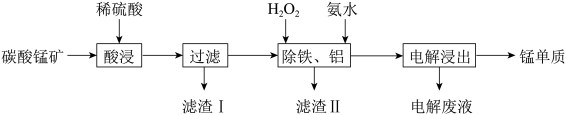
(1)“酸浸”过程中,提高锰元素浸出率的措施有:适当提高酸的浓度、________ (填一种)。
(2)滤渣I的主要成分是________ 。(填化学式)
(3)保持其他条件不变,在不同温度下对碳酸锰矿进行酸浸,锰元素的浸出率随时间变化如图所示,则酸浸的最佳温度和时间分别是________ ℃、________ min。

(4)已知“酸浸”后溶液中锰元素只以Mn2+形式存在,产物之一为CO2,且FeCO3、MnO2均为难溶物,则“酸浸”中发生氧化还原反应的离子方程式为________ 。
(5)结合提取过程中相关金属离子生成氢氧化物沉淀的pH,见下表,“除铁、铝”时加入氨水控制反应液pH的范围为_______ 。
(6)为了提高锰的提取率需要对滤渣Ⅱ进行洗涤,洗涤的方法是________ 。

(1)“酸浸”过程中,提高锰元素浸出率的措施有:适当提高酸的浓度、
(2)滤渣I的主要成分是
(3)保持其他条件不变,在不同温度下对碳酸锰矿进行酸浸,锰元素的浸出率随时间变化如图所示,则酸浸的最佳温度和时间分别是

(4)已知“酸浸”后溶液中锰元素只以Mn2+形式存在,产物之一为CO2,且FeCO3、MnO2均为难溶物,则“酸浸”中发生氧化还原反应的离子方程式为
(5)结合提取过程中相关金属离子生成氢氧化物沉淀的pH,见下表,“除铁、铝”时加入氨水控制反应液pH的范围为
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
| 开始沉淀的pH | 1.8 | 5.8 | 3.0 | 7.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.8 |
(6)为了提高锰的提取率需要对滤渣Ⅱ进行洗涤,洗涤的方法是
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】硫酸锰是一种重要的化工原料,在农业、电化学和建筑等领域均有广泛应用。工业上由软锰矿(主要成分为MnO2,含Fe、Al、Si等氧化物杂质)和闪锌矿(主要为成分为ZnS,含有Fe、Mn等硫化物杂质)为原料制备MnSO4,其工艺如下图所示:
②该工艺条件下,溶液中金属离子形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)“酸浸”后过滤洗涤滤渣1,通常要将洗涤液与滤液合并,其目的是___________ 。从“滤渣1”中可获得一种淡黄色非金属单质的副产品,其化学式为___________ 。
(2)“沉锌”时转化反应 的平衡常数K=
的平衡常数K=___________ ,用沉淀溶解平衡原理解释选择MnS“沉锌”的原因___________ 。
(3)若将“沉锌”与“氧化”两步操作交换,导致的结果为___________ 。
(4)利用MnCO3将溶液的pH应调节在________ 之间,”滤渣2”的成分为_________ 。
(5)工业上用电解MnSO4溶液制备Mn和MnO2,同时得到副产品 ,工作原理如下图所示,该电解池中的离子交换膜为
,工作原理如下图所示,该电解池中的离子交换膜为___________ (填“阳”或“阴”)离子交换膜,石墨电极发生的电极反应式为___________ 。
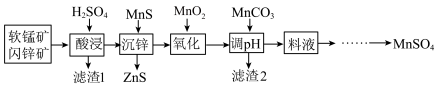
②该工艺条件下,溶液中金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.5 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.3 |
(1)“酸浸”后过滤洗涤滤渣1,通常要将洗涤液与滤液合并,其目的是
(2)“沉锌”时转化反应
 的平衡常数K=
的平衡常数K=(3)若将“沉锌”与“氧化”两步操作交换,导致的结果为
(4)利用MnCO3将溶液的pH应调节在
(5)工业上用电解MnSO4溶液制备Mn和MnO2,同时得到副产品
 ,工作原理如下图所示,该电解池中的离子交换膜为
,工作原理如下图所示,该电解池中的离子交换膜为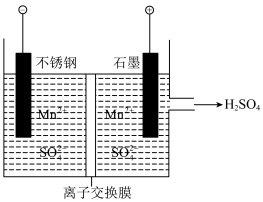
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】高铁酸盐( )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。已知:
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。已知:
ⅰ) 具有强氧化性,易被
具有强氧化性,易被 、
、 及空气中的还原性气体还原。
及空气中的还原性气体还原。
ⅱ) 在
在 或
或 催化作用下分解。
催化作用下分解。
ⅲ) 分解速率方程为
分解速率方程为 。
。
Ⅰ.Johnson提出由过-硫酸氢钾复合盐( )溶液,在冰盐水浴条件下,将
)溶液,在冰盐水浴条件下,将 氧化为
氧化为 ,装置如图所示:
,装置如图所示:
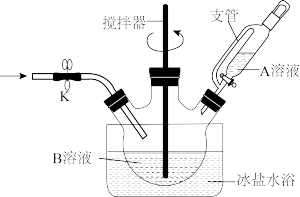
(1)A溶液为_______ (填“a”或“b”)。
a.过-硫酸氢钾复合盐溶液 b. 溶液
溶液
(2)过-硫酸结构简式为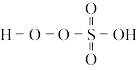 ,则
,则 中的S为+
中的S为+_______ 价。
(3)反应中需全程维持冰盐水浴,原因是_______ 。(任答一条即可)
Ⅱ.Poggendorf首次发现使用铁电极在浓NaOH溶液中,利用“电解法”合成高铁酸盐,原理为: 。
。
(4)电解过程中,电解槽中出现红色浑浊,用离子方程式和文字解释可能原因:_______ (任答一条即可)。
(5)采用如图“隔膜电解法”,可以解决电解过程中出现红色沉淀的问题。
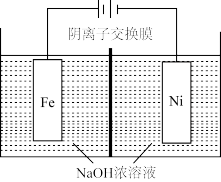
①阳极区加入某种电解质,能避免 被还原,宜加入
被还原,宜加入_______ (填序号,单选)。
a.NaCl b. c.
c. d.
d.
②当阴极区产生6.72L(标况下) 时,阳极区溶液的质量变化量为
时,阳极区溶液的质量变化量为_______ g。(不考虑 的迁移)
的迁移)
Ⅲ. 与水分子结合会发生质子化,并存在平衡
与水分子结合会发生质子化,并存在平衡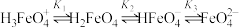 。常温下,0.1
。常温下,0.1 的高铁酸盐溶液中,含铁粒子的分布系数随pH的变化如图所示。
的高铁酸盐溶液中,含铁粒子的分布系数随pH的变化如图所示。
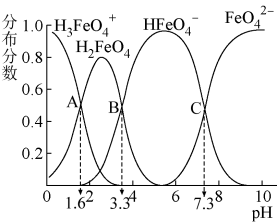
(6)溶液中水的电离程度:A点_______ C点(填“>”“<”或“=”)。
(7)当溶液pH=3时,
_______ :_______ 。
 )是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。已知:
)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。已知:ⅰ)
 具有强氧化性,易被
具有强氧化性,易被 、
、 及空气中的还原性气体还原。
及空气中的还原性气体还原。ⅱ)
 在
在 或
或 催化作用下分解。
催化作用下分解。ⅲ)
 分解速率方程为
分解速率方程为 。
。Ⅰ.Johnson提出由过-硫酸氢钾复合盐(
 )溶液,在冰盐水浴条件下,将
)溶液,在冰盐水浴条件下,将 氧化为
氧化为 ,装置如图所示:
,装置如图所示:
(1)A溶液为
a.过-硫酸氢钾复合盐溶液 b.
 溶液
溶液(2)过-硫酸结构简式为
 ,则
,则 中的S为+
中的S为+(3)反应中需全程维持冰盐水浴,原因是
Ⅱ.Poggendorf首次发现使用铁电极在浓NaOH溶液中,利用“电解法”合成高铁酸盐,原理为:
 。
。(4)电解过程中,电解槽中出现红色浑浊,用离子方程式和文字解释可能原因:
(5)采用如图“隔膜电解法”,可以解决电解过程中出现红色沉淀的问题。

①阳极区加入某种电解质,能避免
 被还原,宜加入
被还原,宜加入a.NaCl b.
 c.
c. d.
d.
②当阴极区产生6.72L(标况下)
 时,阳极区溶液的质量变化量为
时,阳极区溶液的质量变化量为 的迁移)
的迁移) Ⅲ.
 与水分子结合会发生质子化,并存在平衡
与水分子结合会发生质子化,并存在平衡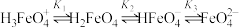 。常温下,0.1
。常温下,0.1 的高铁酸盐溶液中,含铁粒子的分布系数随pH的变化如图所示。
的高铁酸盐溶液中,含铁粒子的分布系数随pH的变化如图所示。
(6)溶液中水的电离程度:A点
(7)当溶液pH=3时,

您最近半年使用:0次