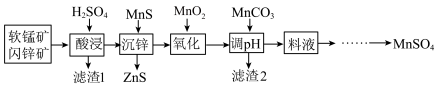
硫酸锰是一种重要的化工原料,在农业、电化学和建筑等领域均有广泛应用。工业上由软锰矿(主要成分为MnO2,含Fe、Al、Si等氧化物杂质)和闪锌矿(主要为成分为ZnS,含有Fe、Mn等硫化物杂质)为原料制备MnSO4,其工艺如下图所示:
②该工艺条件下,溶液中金属离子形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)“酸浸”后过滤洗涤滤渣1,通常要将洗涤液与滤液合并,其目的是___________ 。从“滤渣1”中可获得一种淡黄色非金属单质的副产品,其化学式为___________ 。
(2)“沉锌”时转化反应 的平衡常数K=
的平衡常数K=___________ ,用沉淀溶解平衡原理解释选择MnS“沉锌”的原因___________ 。
(3)若将“沉锌”与“氧化”两步操作交换,导致的结果为___________ 。
(4)利用MnCO3将溶液的pH应调节在________ 之间,”滤渣2”的成分为_________ 。
(5)工业上用电解MnSO4溶液制备Mn和MnO2,同时得到副产品 ,工作原理如下图所示,该电解池中的离子交换膜为
,工作原理如下图所示,该电解池中的离子交换膜为___________ (填“阳”或“阴”)离子交换膜,石墨电极发生的电极反应式为___________ 。
②该工艺条件下,溶液中金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.5 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.3 |
(1)“酸浸”后过滤洗涤滤渣1,通常要将洗涤液与滤液合并,其目的是
(2)“沉锌”时转化反应
 的平衡常数K=
的平衡常数K=(3)若将“沉锌”与“氧化”两步操作交换,导致的结果为
(4)利用MnCO3将溶液的pH应调节在
(5)工业上用电解MnSO4溶液制备Mn和MnO2,同时得到副产品
 ,工作原理如下图所示,该电解池中的离子交换膜为
,工作原理如下图所示,该电解池中的离子交换膜为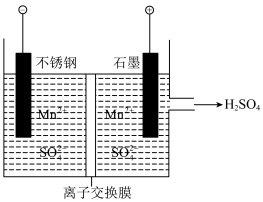
更新时间:2023-04-24 12:36:22
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】碳酸钴可用于伪装涂料的颜料、微量肥料,不溶于水、醇;硫酸镍主要用于电镀、镍电池、催化剂等。利用废镍电池的金属电极芯(主要成分为Co、Ni,还含有少量Fe、Al等)生产碳酸钴、硫酸镍晶体的工艺流程如图所示:
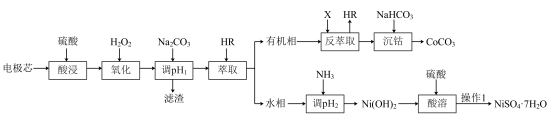
已知:部分金属阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
回答下列问题:
(1)写出“氧化”过程中发生反应的离子方程式为_______ 。
(2)滤渣的主要成分是_______ (填化学式); 的范围为
的范围为_______ 。
(3)在实验室中进行萃取的主要操作过程为加入萃取剂,_______ (填具体操作)。
(4)“沉钴”时发生反应的离子方程式为_______ 。
(5)当溶液中的金属阳离子浓度小于等于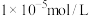 时金属阳离子沉淀完全,对应温度(常温)下
时金属阳离子沉淀完全,对应温度(常温)下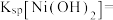
_______ 。
(6)操作I具体是指_______ 、洗涤、干燥。

已知:部分金属阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
| 沉淀物 |  |  |  |  |  |
| 开始沉淀pH | 2.2 | 7.4 | 6.8 | 4.0 | 7.0 |
| 完全沉淀pH | 3.2 | 8.9 | 8.4 | 5.2 | 9.1 |
(1)写出“氧化”过程中发生反应的离子方程式为
(2)滤渣的主要成分是
 的范围为
的范围为(3)在实验室中进行萃取的主要操作过程为加入萃取剂,
(4)“沉钴”时发生反应的离子方程式为
(5)当溶液中的金属阳离子浓度小于等于
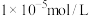 时金属阳离子沉淀完全,对应温度(常温)下
时金属阳离子沉淀完全,对应温度(常温)下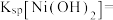
(6)操作I具体是指
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】硒(Se)和铜(Cu)在生产生活中有广泛的应用。氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如图所示:
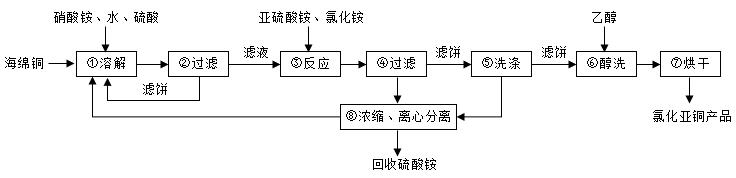
请回答下列问题:
(1)步骤①中主要成分发生的离子反应方程式是:___ 。
(2)写出步骤③中主要反应的离子方程式:___ 。
(3)步骤⑤包括用pH=2的溶液酸洗、水洗两步操作,酸洗采用的酸是___ (写酸的名称)。
(4)上述工艺中,步骤⑥和⑦的作用是___ 。
(5)Se为ⅥA族元素,用乙二胺四乙酸铜阴离子水溶液和硒代硫酸钠(Na2SeSO3)溶液反应可获得纳米硒化铜,硒代硫酸钠还可用于Se的精制,写出硒代硫酸钠(Na2SeSO3)与H2SO4溶液反应得到精硒的化学方程式:___ 。
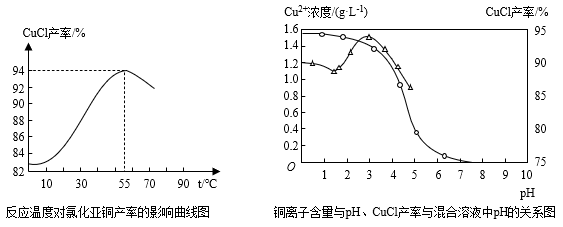
(6)氯化亚铜产率与温度、溶液pH关系如图所示。据图分析,流程化生产氯化亚铜的过程中,温度过低影响CuCl产率的原因是___ ;温度过高、pH过大也会影响CuCl产率的原因是___ 。
(7)用NaHS作污水处理的沉淀剂,可以处理工业废水中的Cu2+。已知:25℃时,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15,CuS的溶度积为Ksp(CuS)=6.3×10-36。反应Cu2+(aq)+HS-(aq) CuS(s)+H+(aq)的平衡常数K=
CuS(s)+H+(aq)的平衡常数K=___ (结果保留1位小数)。

请回答下列问题:
(1)步骤①中主要成分发生的离子反应方程式是:
(2)写出步骤③中主要反应的离子方程式:
(3)步骤⑤包括用pH=2的溶液酸洗、水洗两步操作,酸洗采用的酸是
(4)上述工艺中,步骤⑥和⑦的作用是
(5)Se为ⅥA族元素,用乙二胺四乙酸铜阴离子水溶液和硒代硫酸钠(Na2SeSO3)溶液反应可获得纳米硒化铜,硒代硫酸钠还可用于Se的精制,写出硒代硫酸钠(Na2SeSO3)与H2SO4溶液反应得到精硒的化学方程式:
(6)氯化亚铜产率与温度、溶液pH关系如图所示。据图分析,流程化生产氯化亚铜的过程中,温度过低影响CuCl产率的原因是

(7)用NaHS作污水处理的沉淀剂,可以处理工业废水中的Cu2+。已知:25℃时,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15,CuS的溶度积为Ksp(CuS)=6.3×10-36。反应Cu2+(aq)+HS-(aq)
 CuS(s)+H+(aq)的平衡常数K=
CuS(s)+H+(aq)的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】工业上常用水钴矿(主要成分为Co2O3,还含少量Fe2O3、Al2O3、MgO、CaO等杂质)制备钴的氧化物,其制备工艺流程如下(已知Na2SO3能还原Fe3+和Co3+):
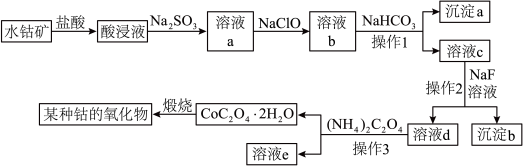
回答下列问题:
(1)在加入盐酸进行“酸浸”时,能提高“酸浸”速率的方法有______________ (任写2种)。
(2)“酸浸”后加入Na2SO3钴的存在形式为Co2+,产生Co2+反应的离子方程式为________
(3)溶液a中加入NaClO的作用是___________________________________
(4)沉淀a的成分是__________ (写化学式),操作2的名称是_______________
(5)溶液d中的金属离子只有Co2+和Na+两种,则溶液c中加入NaF溶液的作用是________
(6)在空气中缎烧CoC2O4生成钴的某种氧化物和CO2,测得充分煅烧后固体质量为12.05g,CO2的体积为6.72L(标准状况),则此反应的化学方程式为____________________________

回答下列问题:
(1)在加入盐酸进行“酸浸”时,能提高“酸浸”速率的方法有
(2)“酸浸”后加入Na2SO3钴的存在形式为Co2+,产生Co2+反应的离子方程式为
(3)溶液a中加入NaClO的作用是
(4)沉淀a的成分是
(5)溶液d中的金属离子只有Co2+和Na+两种,则溶液c中加入NaF溶液的作用是
(6)在空气中缎烧CoC2O4生成钴的某种氧化物和CO2,测得充分煅烧后固体质量为12.05g,CO2的体积为6.72L(标准状况),则此反应的化学方程式为
您最近一年使用:0次
【推荐1】氮的化合物既是重要的工业原料,也是主要的大气污染来源,研究氮的化合物的反应具有重要意义。
(Ⅰ)消除氮氧化物有多种方法。
(1)NH3催化还原法:原理如图所示
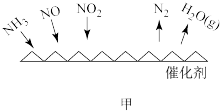
①若烟气中 c(NO2):c(NO)=1∶1,发生如图甲所示的脱氮反应时,反应过程中转移1.5mol电子时放出的热量为 113.8 kJ,则发生该脱氮反应的热化学方程式为___________ 。
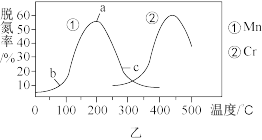
②图乙是在一定时间内,使用不同催化剂 Mn 和 Cr 在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应温度分别为_________ ;使用 Mn 作催化剂时,脱氮率 b~a 段呈现如图变化的可能原因是__________ 。
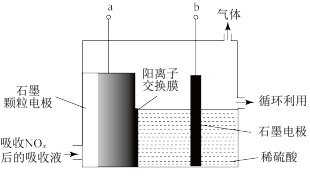
(2)直接电解吸收也是脱硝的一种方法。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如右下图所示。阳极的电极反应式为__________ 。
(Ⅱ)氨是重要的化工原料,工业合成氨有重要现实意义。
(1)在773K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。
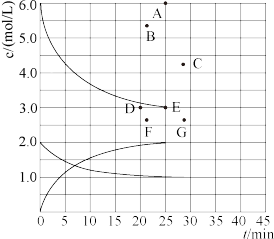
①下列能说明反应达到平衡状态的是____ (选填字母)。
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4.00mol N2和12.00mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为___ (选填字母)。
(2)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:2NO2(g)⇌N2O4(g) ∆H=-56.9kJ‧mol-1,测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
①计算0~20min时,v(N2O4)=____________ 。
②已知该反应v正(NO2)=k1‧c2(NO2),v逆(N2O4)=k2‧c(N2O4),其中k1、k2为速率常数,则373K时,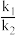 =
=_________ ;改变温度至T1时,k1=k2,则T1_______ 373K(填“>”“<”或“=”)。
(Ⅰ)消除氮氧化物有多种方法。
(1)NH3催化还原法:原理如图所示


①若烟气中 c(NO2):c(NO)=1∶1,发生如图甲所示的脱氮反应时,反应过程中转移1.5mol电子时放出的热量为 113.8 kJ,则发生该脱氮反应的热化学方程式为
②图乙是在一定时间内,使用不同催化剂 Mn 和 Cr 在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应温度分别为
(2)直接电解吸收也是脱硝的一种方法。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如右下图所示。阳极的电极反应式为

(Ⅱ)氨是重要的化工原料,工业合成氨有重要现实意义。
(1)在773K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。

①下列能说明反应达到平衡状态的是
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4.00mol N2和12.00mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为
(2)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:2NO2(g)⇌N2O4(g) ∆H=-56.9kJ‧mol-1,测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 |
| φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①计算0~20min时,v(N2O4)=
②已知该反应v正(NO2)=k1‧c2(NO2),v逆(N2O4)=k2‧c(N2O4),其中k1、k2为速率常数,则373K时,
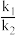 =
=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】NOx、SO2是大气的主要污染物。研究消除NOx、SO2的方法和机理一直是环境专家不断追求的目标。
I.南京大学某教授研究团队以CO同时还原NOx和SO2过程为研究对象,发现在一定温度下,平衡体系中发生的反应为:
①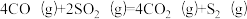
②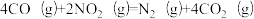
在该温度下,总压为4MPa条件下,以n(CO):n(SO2):n(NO2)=2:1:1通入,t1s后达到平衡,CO2的分压为aMPa,N2的分压为bMPa。
(1)当t1s达平衡时,以CO表示的反应速率为______________________ MPa/s。
(2)反应①在该温度下的Kp=_________________ (MPa)-1。(列出计算式即可,无需化简)
Ⅱ.东南大学化工团队在酸性的条件下,以电化学原理消除NOx、SO2,同时又变废为宝。
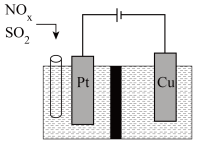
(3)写出NOx转化的电极反应方程式:________________ 。
(4)电解生成的硫酸,电离方程式可表示为: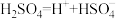 ,
, 。
。
①25°C时,Na2SO4溶液的pH________________ (填“>”“<”或“=”)7。
②0.100mol.L-1的稀硫酸中,c(H+)=0.109mol.L-1,求硫酸第二步电离的电离常数:________________ (写出计算过程,结果保留三位有效数字)。
I.南京大学某教授研究团队以CO同时还原NOx和SO2过程为研究对象,发现在一定温度下,平衡体系中发生的反应为:
①
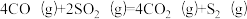
②
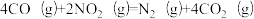
在该温度下,总压为4MPa条件下,以n(CO):n(SO2):n(NO2)=2:1:1通入,t1s后达到平衡,CO2的分压为aMPa,N2的分压为bMPa。
(1)当t1s达平衡时,以CO表示的反应速率为
(2)反应①在该温度下的Kp=
Ⅱ.东南大学化工团队在酸性的条件下,以电化学原理消除NOx、SO2,同时又变废为宝。

(3)写出NOx转化的电极反应方程式:
(4)电解生成的硫酸,电离方程式可表示为:
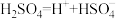 ,
, 。
。①25°C时,Na2SO4溶液的pH
②0.100mol.L-1的稀硫酸中,c(H+)=0.109mol.L-1,求硫酸第二步电离的电离常数:
您最近一年使用:0次
【推荐3】如今 的综合应用越来越成熟。
的综合应用越来越成熟。
(1) 可氧化
可氧化 脱氢转化为更有工业价值的
脱氢转化为更有工业价值的 。
。
查阅资料,计算 氧化
氧化 脱氢反应的反应热
脱氢反应的反应热
i.查阅______ 的燃烧热数据(填化学式)
ii.查阅水的汽化热:
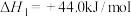
利用上述数据,得如下热化学方程式:
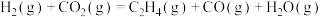
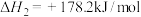
(2) 催化加氢制
催化加氢制 ,能助力“碳达峰”,发生的主要反应有:
,能助力“碳达峰”,发生的主要反应有:
反应Ⅰ

反应Ⅱ

反应Ⅲ

①反应Ⅱ自发进行的条件是______ (填“高温”“低温”或“任意温度”)。
②反应Ⅲ在热力学上趋势大于反应Ⅰ,其原因是______ 。
(3)在5MPa下, 和
和 按物质的量之比1:4进行投料,只发生上述(2)的反应Ⅰ和反应Ⅲ,平衡时
按物质的量之比1:4进行投料,只发生上述(2)的反应Ⅰ和反应Ⅲ,平衡时 和
和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。
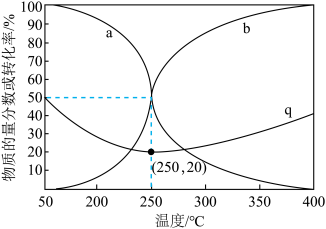
①图中 代表的物质是
代表的物质是______ 。
②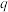 曲线在250℃之后随温度升高而增大的原因是
曲线在250℃之后随温度升高而增大的原因是____________ 。
③250°C时,反应Ⅰ的平衡常数 =
=______ 。
(4)已知25℃时,大气中的 溶于水存在以下过程:
溶于水存在以下过程:
①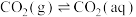

②

过程①的平衡常数 ,其中
,其中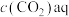 表示溶液中的
表示溶液中的 浓度,
浓度,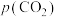 表示大气中
表示大气中 的分压(单位:kPa)。其他条件不变时,温度升高,
的分压(单位:kPa)。其他条件不变时,温度升高,
______ (填“增大”或“减小”);当大气压强为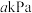 ,溶液中的
,溶液中的 时(忽略
时(忽略 和水的电离),大气中
和水的电离),大气中 的体积分数为
的体积分数为______ %(用含 ,
, 、
、 、
、 的字母表示)。
的字母表示)。
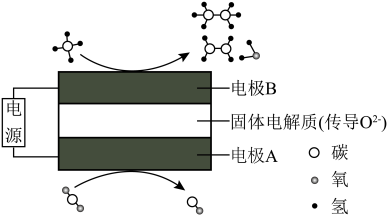
(5)科学家利用电化学装置实现两种分子 和
和 的耦合转化,其原理如图所示:当消耗
的耦合转化,其原理如图所示:当消耗 和
和 的物质的量之比为10:9时,对应的阳极的电极反应式为:
的物质的量之比为10:9时,对应的阳极的电极反应式为:______ 。
 的综合应用越来越成熟。
的综合应用越来越成熟。(1)
 可氧化
可氧化 脱氢转化为更有工业价值的
脱氢转化为更有工业价值的 。
。查阅资料,计算
 氧化
氧化 脱氢反应的反应热
脱氢反应的反应热i.查阅
ii.查阅水的汽化热:

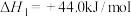
利用上述数据,得如下热化学方程式:
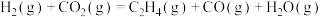
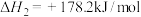
(2)
 催化加氢制
催化加氢制 ,能助力“碳达峰”,发生的主要反应有:
,能助力“碳达峰”,发生的主要反应有:反应Ⅰ


反应Ⅱ


反应Ⅲ


①反应Ⅱ自发进行的条件是
②反应Ⅲ在热力学上趋势大于反应Ⅰ,其原因是
(3)在5MPa下,
 和
和 按物质的量之比1:4进行投料,只发生上述(2)的反应Ⅰ和反应Ⅲ,平衡时
按物质的量之比1:4进行投料,只发生上述(2)的反应Ⅰ和反应Ⅲ,平衡时 和
和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。
①图中
 代表的物质是
代表的物质是②
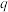 曲线在250℃之后随温度升高而增大的原因是
曲线在250℃之后随温度升高而增大的原因是③250°C时,反应Ⅰ的平衡常数
 =
=(4)已知25℃时,大气中的
 溶于水存在以下过程:
溶于水存在以下过程:①
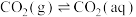

②


过程①的平衡常数
 ,其中
,其中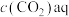 表示溶液中的
表示溶液中的 浓度,
浓度,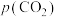 表示大气中
表示大气中 的分压(单位:kPa)。其他条件不变时,温度升高,
的分压(单位:kPa)。其他条件不变时,温度升高,
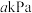 ,溶液中的
,溶液中的 时(忽略
时(忽略 和水的电离),大气中
和水的电离),大气中 的体积分数为
的体积分数为 ,
, 、
、 、
、 的字母表示)。
的字母表示)。(5)科学家利用电化学装置实现两种分子
 和
和 的耦合转化,其原理如图所示:当消耗
的耦合转化,其原理如图所示:当消耗 和
和 的物质的量之比为10:9时,对应的阳极的电极反应式为:
的物质的量之比为10:9时,对应的阳极的电极反应式为:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】绿矾常用于制造补血制剂、净水剂等。以废铁屑(主要含Fe,含少量Fe2O3、油脂等杂质)为原料制备绿矾(FeSO4∙7H2O)晶体并探究其性质。
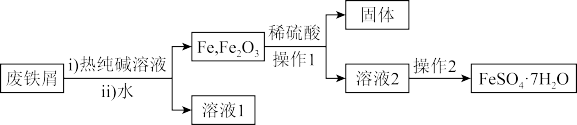
回答下列问题:
(1)铁粉与稀硫酸反应的离子方程式是______ 。操作1需要的玻璃仪器有玻璃棒、烧杯和_______ 。
(2)检验“溶液2”是否含 的试剂是___________(填字母)。
的试剂是___________(填字母)。
(3)操作2包括蒸发浓缩、___________ 、过滤、洗涤、干燥。
(4)实验室配制绿矾溶液时常加入少量铁粉,其作用是___________ (用离子方程式表示)。
(5)大多数文献认为“ 分解生成
分解生成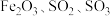 ”。某实验小组提出质疑,认为可能还有
”。某实验小组提出质疑,认为可能还有 生成。他们设计实验如图所示(加热仪器省略),分离
生成。他们设计实验如图所示(加热仪器省略),分离 并检验
并检验 。
。
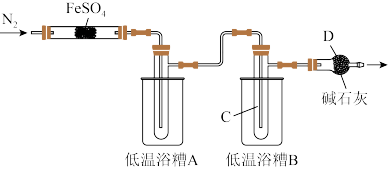
已知部分信息如下:
(I)几种物质的沸点如下表所示:
(II)几种盐浴温度如下:
①低温浴槽A宜选择盐浴___________ (填字母),C仪器收集的物质是___________ (填化学式)。
②若___________ (填实验操作和现象),则证明 分解有
分解有 生成。
生成。
(6)为了测定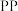 粉(
粉( 的俗名)的纯度,进行如下实验:
的俗名)的纯度,进行如下实验:
称取wgPP粉样品溶于蒸馏水配制成 溶液,准确量取
溶液,准确量取 配制的溶液于锥形瓶,加入适量的稀硫酸,用
配制的溶液于锥形瓶,加入适量的稀硫酸,用 溶液滴定至终点,恰好消耗
溶液滴定至终点,恰好消耗 溶液
溶液 。
。
①配平离子反应:___________ 。
_____ ______
______ _______
_______ _____
_____ ______
______ ______。
______。
②该PP粉的纯度为___________ %(用含w、c、V的代数式表示)。

回答下列问题:
(1)铁粉与稀硫酸反应的离子方程式是
(2)检验“溶液2”是否含
 的试剂是___________(填字母)。
的试剂是___________(填字母)。A. 溶液 溶液 | B. 溶液 溶液 |
C.酸性 溶液 溶液 | D.氯水和 溶液 溶液 |
(4)实验室配制绿矾溶液时常加入少量铁粉,其作用是
(5)大多数文献认为“
 分解生成
分解生成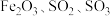 ”。某实验小组提出质疑,认为可能还有
”。某实验小组提出质疑,认为可能还有 生成。他们设计实验如图所示(加热仪器省略),分离
生成。他们设计实验如图所示(加热仪器省略),分离 并检验
并检验 。
。
已知部分信息如下:
(I)几种物质的沸点如下表所示:
| 物质 |  |  |  |
| 熔点/℃ | 16.8 |  | 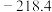 |
| 沸点/℃ | 44.8 | 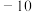 | 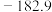 |
| 盐浴 | 浴温/℃ | 盐类及用量 | 碎冰用量 |
| a |  | 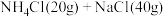 |  |
| b | 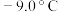 |  |  |
| c | 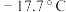 | 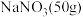 |  |
②若
 分解有
分解有 生成。
生成。(6)为了测定
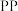 粉(
粉( 的俗名)的纯度,进行如下实验:
的俗名)的纯度,进行如下实验:称取wgPP粉样品溶于蒸馏水配制成
 溶液,准确量取
溶液,准确量取 配制的溶液于锥形瓶,加入适量的稀硫酸,用
配制的溶液于锥形瓶,加入适量的稀硫酸,用 溶液滴定至终点,恰好消耗
溶液滴定至终点,恰好消耗 溶液
溶液 。
。①配平离子反应:
_____
 ______
______ _______
_______ _____
_____ ______
______ ______。
______。②该PP粉的纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】已知NH4HCO3 NH3↑+CO2↑+H2O↑。为了将混有硫酸钠、碳酸氢铵的NaCl提纯,并制得纯净的NaCl溶液,某学生设计如下实验方案:
NH3↑+CO2↑+H2O↑。为了将混有硫酸钠、碳酸氢铵的NaCl提纯,并制得纯净的NaCl溶液,某学生设计如下实验方案:
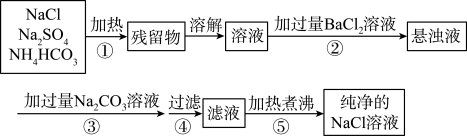
(1)操作④中所需的玻璃仪器有__________________ 。
(2)操作②为什么不用硝酸钡溶液,其理由是__________ 。
(3)进行操作②后,如何判断SO42-已除尽,方法是______
(4)操作③的目的是__________ ,其相应的化学方程式为:_____ ;为什么不先过滤,后加碳酸钠溶液,其理由是_______ 。
(5)说明此设计方案不严密之处及正确的方法____ .
 NH3↑+CO2↑+H2O↑。为了将混有硫酸钠、碳酸氢铵的NaCl提纯,并制得纯净的NaCl溶液,某学生设计如下实验方案:
NH3↑+CO2↑+H2O↑。为了将混有硫酸钠、碳酸氢铵的NaCl提纯,并制得纯净的NaCl溶液,某学生设计如下实验方案:
(1)操作④中所需的玻璃仪器有
(2)操作②为什么不用硝酸钡溶液,其理由是
(3)进行操作②后,如何判断SO42-已除尽,方法是
(4)操作③的目的是
(5)说明此设计方案不严密之处及正确的方法
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】某化学小组模拟工业生产原理:以废铁屑(含少量 、Mn、C等杂质)为原料生产配合物乙二胺四乙酸铁钠(EDTA铁钠盐),并测定所制取的样品中铁元素的含量。
、Mn、C等杂质)为原料生产配合物乙二胺四乙酸铁钠(EDTA铁钠盐),并测定所制取的样品中铁元素的含量。
已知:①乙二胺四乙酸铁钠,易溶于水和稀酸,微溶于乙醇;该螯合型配合物稳定性好
②氢氧化铁沉淀通常呈胶体状态,有较强的吸附性
Ⅰ.制备乙二胺四乙酸铁钠晶体
实验原理:
实验流程:
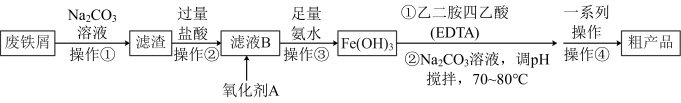
方案1:
(1)由 制乙二胺四乙酸铁钠可以选择
制乙二胺四乙酸铁钠可以选择_________ (填“酒精灯直接加热”或“水浴加热”)。
(2)氧化剂A可以选择 ,试写出该步反应的离子方程式
,试写出该步反应的离子方程式___________ 。
(3)下列说法正确的是___________ 。
A.为避免 沉淀中裹入过多杂质,可以采用一次性加入氨水
沉淀中裹入过多杂质,可以采用一次性加入氨水
B.该流程中两次用到 溶液,均可用
溶液,均可用 溶液代替
溶液代替
C.操作④洗涤时宜采用冷水洗涤
D.“一系列的操作”是指“蒸发浓缩,趁热过滤、洗涤、干燥”
E.乙二胺四乙酸铁钠溶液中滴入KSCN溶液不一定会显红色
方案2:用EDTA、 与
与 反应,制备乙二胺四乙酸铁钠,此法EDTA先被
反应,制备乙二胺四乙酸铁钠,此法EDTA先被 中和后再和
中和后再和 直接反应。两个方案都有不足之处,方案1的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗涤。
直接反应。两个方案都有不足之处,方案1的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗涤。
(4)为使沉淀颗粒增大,实验中往往可以采取___________ (填实验条件)。
(5)方案2的缺点:产品中含杂质多,纯度不好。方案2后剩余废液可用层柱法(利用筛网孔径与微粒孔径不同的一种分离方法)可得到反应的副产物___________ (填名称)。
Ⅱ.测定所制取样品中铁的含量(EDTA标准溶液滴定法)
取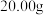 样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配成
样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配成 溶液,取出
溶液,取出 加入过量的
加入过量的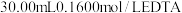 标准溶液并加热煮沸,充分反应后,再用
标准溶液并加热煮沸,充分反应后,再用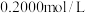 的
的 标准溶液滴定过量的EDTA至终点,消耗
标准溶液滴定过量的EDTA至终点,消耗 标准溶液体积为
标准溶液体积为 。
。
已知: 、
、 与EDTA反应的化学计量比均为
与EDTA反应的化学计量比均为 。
。
(6)实验室进行萃取操作时,需要打开分液漏斗活塞放气,正确的放气图示___________。
(7)计算铁元素的质量分数___________ 。
 、Mn、C等杂质)为原料生产配合物乙二胺四乙酸铁钠(EDTA铁钠盐),并测定所制取的样品中铁元素的含量。
、Mn、C等杂质)为原料生产配合物乙二胺四乙酸铁钠(EDTA铁钠盐),并测定所制取的样品中铁元素的含量。已知:①乙二胺四乙酸铁钠,易溶于水和稀酸,微溶于乙醇;该螯合型配合物稳定性好
②氢氧化铁沉淀通常呈胶体状态,有较强的吸附性
Ⅰ.制备乙二胺四乙酸铁钠晶体
实验原理:

实验流程:
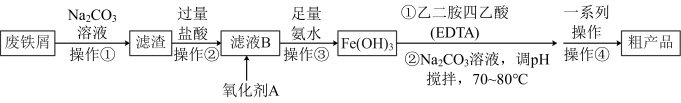
方案1:
(1)由
 制乙二胺四乙酸铁钠可以选择
制乙二胺四乙酸铁钠可以选择(2)氧化剂A可以选择
 ,试写出该步反应的离子方程式
,试写出该步反应的离子方程式(3)下列说法正确的是
A.为避免
 沉淀中裹入过多杂质,可以采用一次性加入氨水
沉淀中裹入过多杂质,可以采用一次性加入氨水B.该流程中两次用到
 溶液,均可用
溶液,均可用 溶液代替
溶液代替C.操作④洗涤时宜采用冷水洗涤
D.“一系列的操作”是指“蒸发浓缩,趁热过滤、洗涤、干燥”
E.乙二胺四乙酸铁钠溶液中滴入KSCN溶液不一定会显红色
方案2:用EDTA、
 与
与 反应,制备乙二胺四乙酸铁钠,此法EDTA先被
反应,制备乙二胺四乙酸铁钠,此法EDTA先被 中和后再和
中和后再和 直接反应。两个方案都有不足之处,方案1的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗涤。
直接反应。两个方案都有不足之处,方案1的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗涤。(4)为使沉淀颗粒增大,实验中往往可以采取
(5)方案2的缺点:产品中含杂质多,纯度不好。方案2后剩余废液可用层柱法(利用筛网孔径与微粒孔径不同的一种分离方法)可得到反应的副产物
Ⅱ.测定所制取样品中铁的含量(EDTA标准溶液滴定法)
取
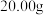 样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配成
样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配成 溶液,取出
溶液,取出 加入过量的
加入过量的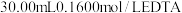 标准溶液并加热煮沸,充分反应后,再用
标准溶液并加热煮沸,充分反应后,再用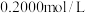 的
的 标准溶液滴定过量的EDTA至终点,消耗
标准溶液滴定过量的EDTA至终点,消耗 标准溶液体积为
标准溶液体积为 。
。已知:
 、
、 与EDTA反应的化学计量比均为
与EDTA反应的化学计量比均为 。
。(6)实验室进行萃取操作时,需要打开分液漏斗活塞放气,正确的放气图示___________。
A.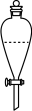 | B. | C.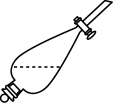 | D. |
(7)计算铁元素的质量分数
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】中美贸易战的矛盾激化,让我们看到了中国半导体产业存在的诸多不足,俗话说“亡羊补牢,为时未晚”,找出存在的不足,然后针对地去解决问题,才能让半导体产业链发展壮大起来。三氯化氧磷(POCl3)是一种重要的化工原料,常用作半导体掺杂剂及光导纤维原料。一研究小组在实验室模拟反应PCl3+SO2+Cl2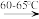 POCl3+SOCl2制备POCl3并测定产品含量。
POCl3+SOCl2制备POCl3并测定产品含量。
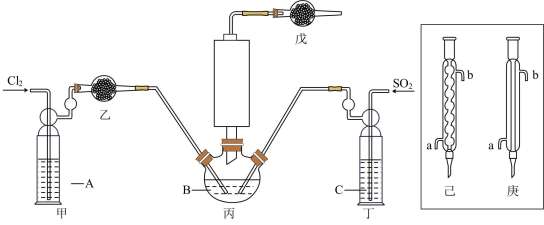
资料卡片:
(1)若选用Na2SO3固体与70%浓H2SO4制取SO2,反应的化学方程式是:_______ 。
(2)溶液A为饱和食盐水,乙装置中应该盛装的试剂为_______ (填“P2O5”或“碱石灰”或“浓H2SO4”或“无水硫酸铜”);反应装置图的虚框中未画出的仪器最好选择_______ (填“己”或“庚”)。
(3)甲、丁装置的作用除了用于气体的净化除杂外,还有_______ 。
(4)水浴加热三颈烧瓶,控制反应温度在60~65℃,其原因是_______ 。
(5)通过佛尔哈德法可测定经过提纯后的产品中POCl3的含量:准确称取1.600g样品在水解瓶中摇动至完全水解,将水解液配成100mL溶液,取10.00mL于锥形瓶中,加入0.2000mol·L-1的AgNO3溶液20.00mL(Ag++Cl-—AgCl↓),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖。加入NH4Fe(SO4)2作指示剂,用0.1000mol·L-1KSCN标准溶液滴定过量的AgNO3至终点(Ag++SCN-—AgSCN↓),做平行实验,平均消耗KSCN标准溶液10.00mL。
①达到滴定终点的现象是_______ 。
②POCl3的质量分数为_______ 。
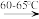 POCl3+SOCl2制备POCl3并测定产品含量。
POCl3+SOCl2制备POCl3并测定产品含量。
资料卡片:
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
| PCl3 | -93.6 | 76.1 | 137.5 | 遇水剧烈水解,易与O2反应 |
| POCl3 | 1.25 | 105.8 | 153.5 | 遇水剧烈水解,能溶于PCl3 |
| SOCl2 | -105 | 78.8 | 119 | 遇水剧烈水解,受热易分解 |
(2)溶液A为饱和食盐水,乙装置中应该盛装的试剂为
(3)甲、丁装置的作用除了用于气体的净化除杂外,还有
(4)水浴加热三颈烧瓶,控制反应温度在60~65℃,其原因是
(5)通过佛尔哈德法可测定经过提纯后的产品中POCl3的含量:准确称取1.600g样品在水解瓶中摇动至完全水解,将水解液配成100mL溶液,取10.00mL于锥形瓶中,加入0.2000mol·L-1的AgNO3溶液20.00mL(Ag++Cl-—AgCl↓),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖。加入NH4Fe(SO4)2作指示剂,用0.1000mol·L-1KSCN标准溶液滴定过量的AgNO3至终点(Ag++SCN-—AgSCN↓),做平行实验,平均消耗KSCN标准溶液10.00mL。
①达到滴定终点的现象是
②POCl3的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】稀土元素被称为“工业维生素”,包括钇、铈等元素,稀土元素能显著提升建造航母及舰载机的材料性能。
Ⅰ.工业上吸收SO2和NO,以获得Na2S2O4和NH4NO3产品的流程图如图(Ce为铈元素)。

(1)装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO 、NO
、NO 。请写出生成相等数目的NO
。请写出生成相等数目的NO 和NO
和NO 时的离子方程式
时的离子方程式________ 。
Ⅱ.含有稀土元素钇的氧化钇(Y2O3)被广泛应用于航空航天涂层材料。以富钇稀土矿(主要成分为Y2O3,含有少量的Fe2O3、CuO、SiO2等杂质)生产氧化钇的工艺流程如图,回答下列问题:
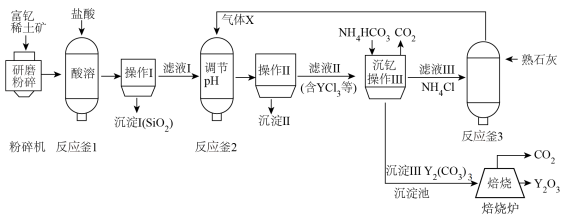
(2)在粉碎机中研磨粉碎的目的是________ 。
(3)流程中操作Ⅰ、Ⅱ、Ⅲ的名称是_______ ,“酸溶”过程中,Y2O3发生反应的离子方程式为_______ 。
(4)向反应釜2中通入气体X使溶液呈碱性,调节溶液的pH除去滤液1中杂质,沉淀Ⅱ的主要成分是________ (填化学式)。
(5)流程中可循环使用的物质为_______ (填名称)。
Ⅰ.工业上吸收SO2和NO,以获得Na2S2O4和NH4NO3产品的流程图如图(Ce为铈元素)。

(1)装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO
 、NO
、NO 。请写出生成相等数目的NO
。请写出生成相等数目的NO 和NO
和NO 时的离子方程式
时的离子方程式Ⅱ.含有稀土元素钇的氧化钇(Y2O3)被广泛应用于航空航天涂层材料。以富钇稀土矿(主要成分为Y2O3,含有少量的Fe2O3、CuO、SiO2等杂质)生产氧化钇的工艺流程如图,回答下列问题:

(2)在粉碎机中研磨粉碎的目的是
(3)流程中操作Ⅰ、Ⅱ、Ⅲ的名称是
(4)向反应釜2中通入气体X使溶液呈碱性,调节溶液的pH除去滤液1中杂质,沉淀Ⅱ的主要成分是
(5)流程中可循环使用的物质为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】亚硝酰硫酸(NOSO4H)是一种浅黄色或蓝紫色液体,遇水分解,溶于浓硫酸不分解,主要用于染料、医药领域的重氮化反应中取代亚硝酸钠。亚硝酰硫酸能有效降低硫酸使用量,增加反应的流动性,不产生无机盐,从而可以降低成本,提高产品质量,使染料成品色泽鲜艳、固色能力强,并减少污水。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。
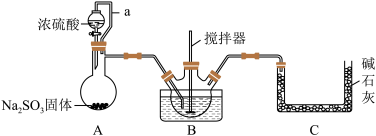
(1)简述检验装置A的气密性操作______ 。
(2)装置B中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20 ℃,故可将三颈烧瓶置于____ 中。
②开始时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是______ 。
③该实验装置存在导致NOSO4H产量降低的缺陷,请提出改进方案_____ 。
④利用装置A制备SO2 ,下列试剂最适宜的是______ 。
A.Na2SO3固体和20%硝酸 B.Na2SO3固体和20%硫酸
C.Na2SO3固体和70%硫酸 D.Na2SO3固体和98%硫酸
⑤已知亚硝酸不稳定,易分解,发生反应2HNO2=NO2↑+NO↑+H2O。请写出NOSO4H遇水分解时发生反应的化学方程式______ 。
(3)测定亚硝酰硫酸NOSO4H的纯度。
准确称取1.380 g产品放入250 mL的碘量瓶中,加入60.00 mL0.1000 mol·L-1KMnO4标准溶液和10 mL 25%的H2SO4溶液,然后摇匀(过程中无气体产生)。用0.2500 mol·L-1的草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00 mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4。
①简述该操作达到滴定终点时的现象______ 。
②亚硝酰硫酸的纯度为______ 。

(1)简述检验装置A的气密性操作
(2)装置B中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20 ℃,故可将三颈烧瓶置于
②开始时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是
③该实验装置存在导致NOSO4H产量降低的缺陷,请提出改进方案
④利用装置A制备SO2 ,下列试剂最适宜的是
A.Na2SO3固体和20%硝酸 B.Na2SO3固体和20%硫酸
C.Na2SO3固体和70%硫酸 D.Na2SO3固体和98%硫酸
⑤已知亚硝酸不稳定,易分解,发生反应2HNO2=NO2↑+NO↑+H2O。请写出NOSO4H遇水分解时发生反应的化学方程式
(3)测定亚硝酰硫酸NOSO4H的纯度。
准确称取1.380 g产品放入250 mL的碘量瓶中,加入60.00 mL0.1000 mol·L-1KMnO4标准溶液和10 mL 25%的H2SO4溶液,然后摇匀(过程中无气体产生)。用0.2500 mol·L-1的草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00 mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4。
①简述该操作达到滴定终点时的现象
②亚硝酰硫酸的纯度为
您最近一年使用:0次



