碳酸钴可用于伪装涂料的颜料、微量肥料,不溶于水、醇;硫酸镍主要用于电镀、镍电池、催化剂等。利用废镍电池的金属电极芯(主要成分为Co、Ni,还含有少量Fe、Al等)生产碳酸钴、硫酸镍晶体的工艺流程如图所示:
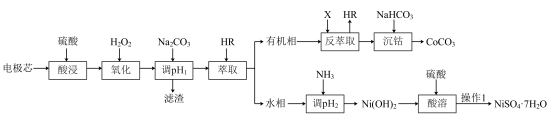
已知:部分金属阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
回答下列问题:
(1)写出“氧化”过程中发生反应的离子方程式为_______ 。
(2)滤渣的主要成分是_______ (填化学式); 的范围为
的范围为_______ 。
(3)在实验室中进行萃取的主要操作过程为加入萃取剂,_______ (填具体操作)。
(4)“沉钴”时发生反应的离子方程式为_______ 。
(5)当溶液中的金属阳离子浓度小于等于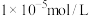 时金属阳离子沉淀完全,对应温度(常温)下
时金属阳离子沉淀完全,对应温度(常温)下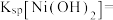
_______ 。
(6)操作I具体是指_______ 、洗涤、干燥。

已知:部分金属阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
| 沉淀物 |  |  |  |  |  |
| 开始沉淀pH | 2.2 | 7.4 | 6.8 | 4.0 | 7.0 |
| 完全沉淀pH | 3.2 | 8.9 | 8.4 | 5.2 | 9.1 |
(1)写出“氧化”过程中发生反应的离子方程式为
(2)滤渣的主要成分是
 的范围为
的范围为(3)在实验室中进行萃取的主要操作过程为加入萃取剂,
(4)“沉钴”时发生反应的离子方程式为
(5)当溶液中的金属阳离子浓度小于等于
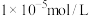 时金属阳离子沉淀完全,对应温度(常温)下
时金属阳离子沉淀完全,对应温度(常温)下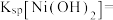
(6)操作I具体是指
更新时间:2023-08-02 16:18:59
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】锂离子电池在我们日常生活中随处可见,随之而来的是废旧电池的合理处理,否则会造成新的环境污染。从废旧锂离子电池正极材料(主要含LiCoO2、Al等)中回收Co并制取CoC2O4·2H2O的工艺流程如图所示:
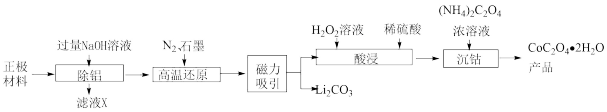
已知:①LiCoO2与NaOH溶液不反应;
②金属Co易被磁铁吸引,与稀硫酸反应生成大量氢气。
回答下列问题:
(1)“除铝”前需将废旧锂离子电池经过放电、破碎处理,其中破碎的目的是______ ,滤液X的主要溶质是______ (填化学式)。
(2)“高温还原”时,有CO生成,发生反应的化学方程式为______ ;“高温还原”时,通入N2的目的是______ 。
(3)从安全性角度考虑,“酸浸”时先加入过氧化氢溶液,再加入稀硫酸的原因是______ ,“酸浸”发生的总离子反应方程式为_______ 。
(4)“沉钴”时,检验钴离子已沉淀完全的方法是______ ,已知钴离子恰好完全沉淀(离子浓度等于10-5mol•L-1)时,c(C2O )=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=
)=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=______ 。

已知:①LiCoO2与NaOH溶液不反应;
②金属Co易被磁铁吸引,与稀硫酸反应生成大量氢气。
回答下列问题:
(1)“除铝”前需将废旧锂离子电池经过放电、破碎处理,其中破碎的目的是
(2)“高温还原”时,有CO生成,发生反应的化学方程式为
(3)从安全性角度考虑,“酸浸”时先加入过氧化氢溶液,再加入稀硫酸的原因是
(4)“沉钴”时,检验钴离子已沉淀完全的方法是
 )=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=
)=2.0×10-5mol•L-1,则该温度下Ksp(CoC2O4)=
您最近一年使用:0次
【推荐2】电化学原理被广泛应用于生产、生活的许多方面,利用电解法脱除煤中的含硫物质(主要是FeS2)的原理如图所示。
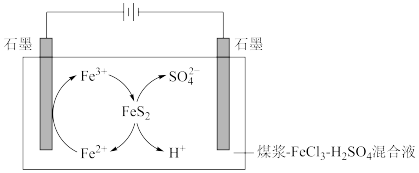
(1)阴极石墨棒上有无色气体产生,该气体是_______ 。
(2)阳极的电极反应式为_______ 。
(3)补全脱硫反应方程式:_______ 。
FeS2+_______+_______=SO +_______+_______
+_______+_______
(4)相同反应时间,FeCl3对脱硫率的影响如图所示。

①电解脱硫过程中,FeCl3的作用是催化剂,结合简单碰撞理论说明使用FeCl3能加快反应速率的原因_______ 。
②FeCl3的质量分数大于1.5%时,脱硫率随FeCl3浓度的增大而下降,解释原因_______ 。
(5)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率降低。电解效率η的定义: 。某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其它含硫物质,混合液中H2SO4浓度为0.01mol·L−1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(SO
。某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其它含硫物质,混合液中H2SO4浓度为0.01mol·L−1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(SO )=0.02mol·L−1,η(SO
)=0.02mol·L−1,η(SO )=
)=_______ (忽略电解前后溶液的体积变化)。
(6)综上,电解法脱硫的优点有_______ (写出两点)。

(1)阴极石墨棒上有无色气体产生,该气体是
(2)阳极的电极反应式为
(3)补全脱硫反应方程式:
FeS2+_______+_______=SO
 +_______+_______
+_______+_______(4)相同反应时间,FeCl3对脱硫率的影响如图所示。

①电解脱硫过程中,FeCl3的作用是催化剂,结合简单碰撞理论说明使用FeCl3能加快反应速率的原因
②FeCl3的质量分数大于1.5%时,脱硫率随FeCl3浓度的增大而下降,解释原因
(5)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率降低。电解效率η的定义:
 。某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其它含硫物质,混合液中H2SO4浓度为0.01mol·L−1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(SO
。某电压下电解100mL煤浆-FeCl3-H2SO4混合液,煤浆中除FeS2外不含其它含硫物质,混合液中H2SO4浓度为0.01mol·L−1,FeCl3的质量分数为1.5%。当阴极收集到224mL(标准状况)气体时(阴极无副反应发生),测得溶液中c(SO )=0.02mol·L−1,η(SO
)=0.02mol·L−1,η(SO )=
)=(6)综上,电解法脱硫的优点有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】一种从阳极泥(主要成分为Cu、Ag、Pt、 Se和
Se和 等)中回收Se和贵重金属的工艺流程如下图所示。回答下列问题:
等)中回收Se和贵重金属的工艺流程如下图所示。回答下列问题:

已知:该工艺中萃取与反萃取原理为:
(1)已知Ag为47号元素,Ag在元素周期表中的位置为_______ 。
(2)“焙烧”产生的 与
与 的混合烟气可用水吸收制得单质Se,该反应的化学方程式为
的混合烟气可用水吸收制得单质Se,该反应的化学方程式为_______ ;过滤所得粗硒可采用减压蒸馏的方法提纯单质硒,采用减压蒸馏的目的是_______ 。
(3)“酸浸氧化”中通入氧气的目的是_______ ;“反萃取剂”最好选用_______ (填化学式)。
(4)沉银时加入NaCl,可将 转化为AgCl,再用硫代硫酸盐溶液浸出银元素。已知:
转化为AgCl,再用硫代硫酸盐溶液浸出银元素。已知:
①

②

溶液中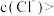
_______  时,可使所得浸出液中
时,可使所得浸出液中 。
。
(5)“滤液Ⅳ”中含有 和
和 ,则“还原”中发生反应的离子方程式为
,则“还原”中发生反应的离子方程式为_______ 。
(6)研究发现,硫代硫酸盐浸出金的过程是电化学催化腐蚀过程,催化机理模型如图所示:

图中表示金粒负极的电极反应式为_______ 。浸金过程中的催化剂是_______ (填化学式)。
 Se和
Se和 等)中回收Se和贵重金属的工艺流程如下图所示。回答下列问题:
等)中回收Se和贵重金属的工艺流程如下图所示。回答下列问题:
已知:该工艺中萃取与反萃取原理为:

(1)已知Ag为47号元素,Ag在元素周期表中的位置为
(2)“焙烧”产生的
 与
与 的混合烟气可用水吸收制得单质Se,该反应的化学方程式为
的混合烟气可用水吸收制得单质Se,该反应的化学方程式为(3)“酸浸氧化”中通入氧气的目的是
(4)沉银时加入NaCl,可将
 转化为AgCl,再用硫代硫酸盐溶液浸出银元素。已知:
转化为AgCl,再用硫代硫酸盐溶液浸出银元素。已知:①


②


溶液中
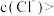
 时,可使所得浸出液中
时,可使所得浸出液中 。
。(5)“滤液Ⅳ”中含有
 和
和 ,则“还原”中发生反应的离子方程式为
,则“还原”中发生反应的离子方程式为(6)研究发现,硫代硫酸盐浸出金的过程是电化学催化腐蚀过程,催化机理模型如图所示:

图中表示金粒负极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】世界上铬单质及其化合物的生产呈现高速增长,故铬贫矿的利用至关重要。某铬贫矿的主要成分为Fe(CrO2)2,还含有Fe2O3、MgO、Al2O3,采用次氯酸钠法处理矿石并制备CrO3的工艺流程如下:

回答下列问题:
(1)已知经“氧化浸出”后,铁元素以Fe2O3形式存在,该过程中Fe(CrO2)2参与反应的化学方程式为_______ 。
(2)“滤渣”可能含有的物质有_______ (填化学式)。
(3)已知常温下Al(OH)3(s)+H₂O( l) [Al(OH)4]-(aq)+H+(aq) K=1×10-13.37;Al(OH)3( s)
[Al(OH)4]-(aq)+H+(aq) K=1×10-13.37;Al(OH)3( s)  Al3+(aq)+3OH-( aq) Ksp[Al(OH)3]=1×10-33。
Al3+(aq)+3OH-( aq) Ksp[Al(OH)3]=1×10-33。
经“沉铝”后所得溶液中[Al(OH)4]-的浓度为1×10-5.5mol·L-1此时溶液中的c(H+)=_______ mol·L-1, c(Al3+) =_______ mol·L-1。
(4)实验室将浓硫酸和Na2CrO7溶液“混合”时的具体实验操作为_______ 。
(5)以1.4kg铬贫矿为原料,按照此流程最终得到0.2kgCrO3,原料的利用率为80%,则该铬贫矿中Fe(CrO2)2的百分含量为_______ 。
(6)以节能环保为原则,以化合物M为原料,设计在此工艺流程中的循环利用方案:_______ (结合化学方程式用文字说明)。

回答下列问题:
(1)已知经“氧化浸出”后,铁元素以Fe2O3形式存在,该过程中Fe(CrO2)2参与反应的化学方程式为
(2)“滤渣”可能含有的物质有
(3)已知常温下Al(OH)3(s)+H₂O( l)
 [Al(OH)4]-(aq)+H+(aq) K=1×10-13.37;Al(OH)3( s)
[Al(OH)4]-(aq)+H+(aq) K=1×10-13.37;Al(OH)3( s)  Al3+(aq)+3OH-( aq) Ksp[Al(OH)3]=1×10-33。
Al3+(aq)+3OH-( aq) Ksp[Al(OH)3]=1×10-33。经“沉铝”后所得溶液中[Al(OH)4]-的浓度为1×10-5.5mol·L-1此时溶液中的c(H+)=
(4)实验室将浓硫酸和Na2CrO7溶液“混合”时的具体实验操作为
(5)以1.4kg铬贫矿为原料,按照此流程最终得到0.2kgCrO3,原料的利用率为80%,则该铬贫矿中Fe(CrO2)2的百分含量为
(6)以节能环保为原则,以化合物M为原料,设计在此工艺流程中的循环利用方案:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】以废镍催化剂(主要含 、
、 ,以及
,以及 、
、 、
、 杂质)为原料制备
杂质)为原料制备 的工艺流程如图所示:
的工艺流程如图所示:
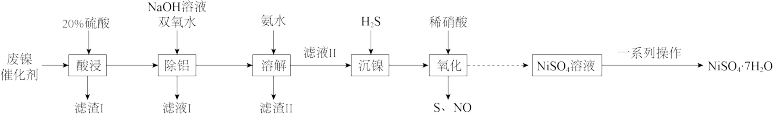
已知:双氧水不能氧化 ;
; 、
、 均难溶于水。
均难溶于水。
请回答下列问题:
(1)废镍催化剂在“酸浸”前还需要粉碎,粉碎的主要目的是_______ 。
(2)“除铝”步骤中铝元素发生反应的离子方程式是_______ 。
(3)已知滤液Ⅱ中存在 的解离平衡:
的解离平衡: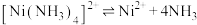 ,请根据平衡移动原理说明通入
,请根据平衡移动原理说明通入 能“沉镍”的原因:
能“沉镍”的原因:_______ 。
(4)“氧化”步骤中有用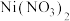 生成,则生成
生成,则生成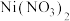 的反应中氧化剂与还原剂的物质的量之比为
的反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)室温下,已知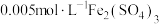 溶液中
溶液中 开始沉淀的
开始沉淀的 为2.3,则
为2.3,则 完全沉淀时
完全沉淀时 的
的 为
为_______ 。
 、
、 ,以及
,以及 、
、 、
、 杂质)为原料制备
杂质)为原料制备 的工艺流程如图所示:
的工艺流程如图所示:
已知:双氧水不能氧化
 ;
; 、
、 均难溶于水。
均难溶于水。请回答下列问题:
(1)废镍催化剂在“酸浸”前还需要粉碎,粉碎的主要目的是
(2)“除铝”步骤中铝元素发生反应的离子方程式是
(3)已知滤液Ⅱ中存在
 的解离平衡:
的解离平衡: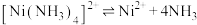 ,请根据平衡移动原理说明通入
,请根据平衡移动原理说明通入 能“沉镍”的原因:
能“沉镍”的原因:(4)“氧化”步骤中有用
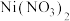 生成,则生成
生成,则生成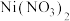 的反应中氧化剂与还原剂的物质的量之比为
的反应中氧化剂与还原剂的物质的量之比为(5)室温下,已知
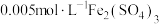 溶液中
溶液中 开始沉淀的
开始沉淀的 为2.3,则
为2.3,则 完全沉淀时
完全沉淀时 的
的 为
为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】工业上由黄铜矿(主要成分CuFeS2)制取 FeSO4·7H2O 和Cu的主要流程如下:

(1)检验酸浸过程中 Fe2+是否被氧化,应选择________ (填字母编号)。
A.KMnO4 溶液 B.K3[Fe(CN)6]溶液 C.KSCN 溶液
(2)酸浸过程中主要反应的化学方程式为__________ 。
(3)电解粗铜制精铜时,可采用NO2、O2和熔融NaNO3制作的燃料电池作电源,其原理如图,该电池在使用过程中石墨 I电极上生成氧化物Y,则其正极的电极反应为:____________ 。

(4)某同学向盛有 H2O2溶液的试管中加入几滴酸化的 FeSO4溶液,溶液变成棕黄色,发生反应的离子方程式为___________ 。一段时间后.溶液中有气泡出现,并放热,随后有红褐色沉淀生成;产生气泡的原因是_________ ,生成沉淀的原因是___________ (用平衡移动原理解释)。
(5)已知 25℃时, Ksp[Fe(OH)3]=4.0×10-38,此温度下,若实验室中配制 2.5 mol/L 100 mLFe2(SO4)3溶液,为使配制过程中不出现浑浊,则至少需要加10 mol/L的硫酸______ mL(忽略加入硫酸的体积)。

(1)检验酸浸过程中 Fe2+是否被氧化,应选择
A.KMnO4 溶液 B.K3[Fe(CN)6]溶液 C.KSCN 溶液
(2)酸浸过程中主要反应的化学方程式为
(3)电解粗铜制精铜时,可采用NO2、O2和熔融NaNO3制作的燃料电池作电源,其原理如图,该电池在使用过程中石墨 I电极上生成氧化物Y,则其正极的电极反应为:

(4)某同学向盛有 H2O2溶液的试管中加入几滴酸化的 FeSO4溶液,溶液变成棕黄色,发生反应的离子方程式为
(5)已知 25℃时, Ksp[Fe(OH)3]=4.0×10-38,此温度下,若实验室中配制 2.5 mol/L 100 mLFe2(SO4)3溶液,为使配制过程中不出现浑浊,则至少需要加10 mol/L的硫酸
您最近一年使用:0次



