广东省化州市2018届高三上学期第二次高考模拟考试理综化学试题
广东
高三
二模
2017-12-25
371次
整体难度:
适中
考查范围:
化学与STSE、有机化学基础、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、常见无机物及其应用
广东省化州市2018届高三上学期第二次高考模拟考试理综化学试题
广东
高三
二模
2017-12-25
371次
整体难度:
适中
考查范围:
化学与STSE、有机化学基础、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
单选题
|
容易(0.94)
1. 化学与生活、技术密不可分,下列有关说法错误的是
| A.天然气是高效清洁的化石燃料 | B.煤的干馏属于化学变化 |
| C.油脂可以制取肥皂 | D.我国使用最早的合金是生铁 |
【知识点】 化学科学对人类文明发展的意义解读 金属材料的性质及利用 化石能源 煤的干馏解读
您最近一年使用:0次
单选题
|
适中(0.65)
2. 某分子的球棍模型如下图所示,图中“棍”代表单键或双键或三键;不同颜色的球代表不同元素的原子。有关该分子的说法错误的是:
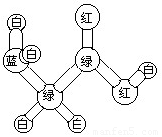

| A.不属于烃类 | B.能发生聚合反应 |
| C.不能与盐酸反应 | D.能与金属钠发生置换反应 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
3. 设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.在标准状况下,11.2 L NO 与11.2 LO2混合后所含原子数为NA |
| B.110 g Na2S2中含有的离子数为3NA |
| C.0.1mol·L-1Na2CO3溶液1L所含阴离子数目小于0.1NA |
| D.1mol Cl2溶于足量的水中,反应时断裂的Cl-Cl 键数目为NA |
您最近一年使用:0次
2017-12-20更新
|
248次组卷
|
2卷引用:广东省化州市2018届高三上学期第二次高考模拟考试理综化学试题
单选题
|
适中(0.65)
4. 厨房垃圾发酵液可通过电渗析法处理,同时得到乳酸的原理如图所示(图中HA表示乳酸分子,A-表示乳酸根离子)。下列说法正确的是
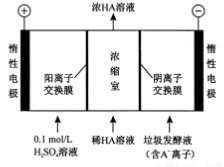

| A.通电后,阳极附近PH增大 | B.电子从负极经电解质溶液回到正极 |
| C.通电后,A-通过阴离子交换膜从阴极进入浓缩室 | D.当电路中通过2mol电子的电量时,会有11.2LO2生成 |
【知识点】 电解原理的应用 电解原理的理解及判断解读 电解原理的应用实验解读
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
5. 短周期元素W、X、Y、Z的原子序数依次增加。m、n、s是由这些元素组成的二元化合物。p和r分别是元素Z和X的单质,p通常为黄绿色气体。常温下0.01mol·L-1q的水溶液的pH为12。上述物质的转化关系如图所示。下列说法正确的是
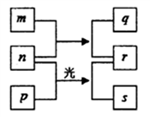

| A.离子半径的大小Z>Y>X | B.单质的还原性:Y>W |
| C.W在化合物中一定是+1价 | D.Z的氧化物的水化物为强酸 |
您最近一年使用:0次
单选题
|
较难(0.4)
6. 下列有关实验现象和解释或结论都正确的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2 N2O4的△H<0 N2O4的△H<0 |
| B | 淀粉水解后的溶液加入新制Cu(OH)2浊液,再加热 | 无砖红色沉淀 | 淀粉水解产物不含醛基 |
| C | 用铂丝蘸取少量溶液进行焰色反应 | 火焰呈黄色 | 该溶液是钠盐溶液 |
| D | 向盛有1mL0.l mol/L的AgNO3溶液中加入10滴0.1mol/L的NaCl溶液,振荡,再加入10滴0.1 nol/L的NaI溶液,再振荡, | 先生成白色沉淀,后产生黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-12-20更新
|
766次组卷
|
3卷引用:广东省化州市2018届高三上学期第二次高考模拟考试理综化学试题
广东省化州市2018届高三上学期第二次高考模拟考试理综化学试题2017-2018学年第一学期期末复习备考之精准复习模拟题高三化学(单科)(C卷)(已下线)第三单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)
单选题
|
适中(0.65)
7. 下图是一种染料敏化太阳能电池的示意图。电池的一个电极由有机光敏染料(S)涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:
TiO2/S→TiO2/S*(激发态)
TiO2/S*→TiO2/S*+e-
I3-+2e-→3I-
2TiO2/S++3I-→2TiO2/S+I3-
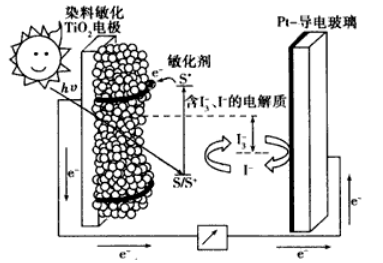
下列关于该电池叙述错误的是
TiO2/S→TiO2/S*(激发态)
TiO2/S*→TiO2/S*+e-
I3-+2e-→3I-
2TiO2/S++3I-→2TiO2/S+I3-

下列关于该电池叙述错误的是
| A.电池工作时,是将太阳能转化为电能 |
| B.电池工作时,I-离子在镀铂导电玻璃电极上放电 |
| C.电池中镀铂导电玻璃为正极 |
| D.电池的电解质溶液中I-和I3-的浓度不会减少 |
【知识点】 原电池原理的综合应用解读 新型电池解读
您最近一年使用:0次
2017-12-20更新
|
300次组卷
|
2卷引用:广东省化州市2018届高三上学期第二次高考模拟考试理综化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
解题方法
8. 草酸亚铁晶体(FeC2O4·2H2O)是一种黄色难溶于水的固体,受热易分解,是生产锂电池、涂料、着色剂以及感光材料的原材料。
Ⅰ、草酸亚铁晶体的制备:

(1)步骤①硫酸亚铁铵晶体加稀硫酸溶解的原因是___________________ 。
(2)步骤2倾析的作用是使固液分离,具体操作是静置后,将沉淀上部的溶液倾入另一容器,从而获得固体。倾析法与普通的过滤相比,明显的优点是____________________ 。
(3)硫酸亚铁铵俗称莫尔盐,在空气中比一般的亚铁盐稳定,较难被氧化,其水溶液的性质与组成它的简单盐的混合溶液没有区别。设计简单实验证明硫酸亚铁铵比硫酸亚铁更稳定______________________ 。
Ⅱ、测定草酸亚铁的纯度:
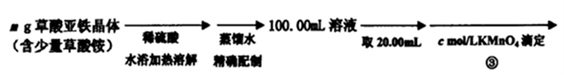

(4)在步骤③的溶液中除发生反应MnO4-+8H++5Fe2+=5Fe3++Mn2++4H2O 外,还有另一氧化还原反应,写出该反应的离子方程式__________________ ;用KmnO4标准溶液滴定至终点的现象是_____________________ 。
(5)步骤④加入适量锌粉的目的是________________ 。
(6)相同条件下,重复滴定三次,步骤③平均消耗KmnO4标准溶液V1mL,步骤⑤平均消耗V2mL,则mg固体样品的纯度计算式为______________ 。(用相关字母表示,不必化简)
Ⅰ、草酸亚铁晶体的制备:

(1)步骤①硫酸亚铁铵晶体加稀硫酸溶解的原因是
(2)步骤2倾析的作用是使固液分离,具体操作是静置后,将沉淀上部的溶液倾入另一容器,从而获得固体。倾析法与普通的过滤相比,明显的优点是
(3)硫酸亚铁铵俗称莫尔盐,在空气中比一般的亚铁盐稳定,较难被氧化,其水溶液的性质与组成它的简单盐的混合溶液没有区别。设计简单实验证明硫酸亚铁铵比硫酸亚铁更稳定
Ⅱ、测定草酸亚铁的纯度:


(4)在步骤③的溶液中除发生反应MnO4-+8H++5Fe2+=5Fe3++Mn2++4H2O 外,还有另一氧化还原反应,写出该反应的离子方程式
(5)步骤④加入适量锌粉的目的是
(6)相同条件下,重复滴定三次,步骤③平均消耗KmnO4标准溶液V1mL,步骤⑤平均消耗V2mL,则mg固体样品的纯度计算式为
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
解题方法
9. 用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备碱式碳酸铜的流程如下:
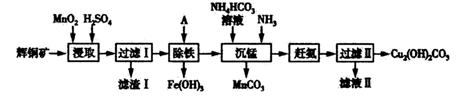
(1)辉铜矿中铜元素的价态为_________________ 。
(2)滤渣Ⅰ的成分除了不溶性矿渣外,还有S、__________ 、______________ ,写出“浸取”过程中生成S 的离子方程式_______________________ 。
(3)也可用FeCl3代替MnO2作浸取剂。若向FeCl3浸取液中加入CuCl2 ,能加快铜元素的浸取速率,该过程的反应原理可用化学方程式表示为:①Cu2S+2CuCl2=4CuCl+S;②____________ 。
(4)“沉锰”时发生的反应的离子方程式为____________________ 。
(5)滤液Ⅱ经结晶得到的盐主要是____________ (填化学式,下同),流程中可循环的物质是_________________ 。
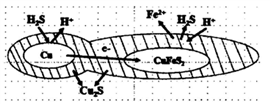
(6)辉铜矿可由黄铜矿(主要成分为CuFeS2)通过电化学反应转变而成,有关转化见下图,转化时负极的电极 反应式为___________________ 。

(1)辉铜矿中铜元素的价态为
(2)滤渣Ⅰ的成分除了不溶性矿渣外,还有S、
(3)也可用FeCl3代替MnO2作浸取剂。若向FeCl3浸取液中加入CuCl2 ,能加快铜元素的浸取速率,该过程的反应原理可用化学方程式表示为:①Cu2S+2CuCl2=4CuCl+S;②
(4)“沉锰”时发生的反应的离子方程式为
(5)滤液Ⅱ经结晶得到的盐主要是
(6)辉铜矿可由黄铜矿(主要成分为CuFeS2)通过电化学反应转变而成,有关转化见下图,转化时负极的电极 反应式为

您最近一年使用:0次
解答题-原理综合题
|
较难(0.4)
解题方法
10. 对机动车尾气中的N元素、C 元素进行处理,可以保护环境,减少污染。
(1)汽缸中生成 NO 的反应为:N2(g)+O2(g) 2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
反应Ⅰ:NO(g)+CO(g)+Rh(s) RhN(s)+CO2(g) △H=-8 kcal·mol-1
RhN(s)+CO2(g) △H=-8 kcal·mol-1
反应Ⅱ:RhN(s)+NO(g) Rh(s)+N2O △H =-76.4 kcal·mol -1
Rh(s)+N2O △H =-76.4 kcal·mol -1
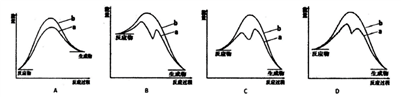
则由NO生成2 mol N2O的△H =_________ kcal·mol-1。若Ⅰ比Ⅱ的反应速率大,下列能正确表示反应2NO(g)+CO(g) N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应过程的能量变化图的是
N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应过程的能量变化图的是________________ 。
(2)相同温度下,两个体积均为1L的恒容密闭容器中,发生反应:
2NO(g)+2CO (g)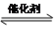 N2(g)+2CO2(g),有关物质的量如下表:
N2(g)+2CO2(g),有关物质的量如下表:
①容器Ⅰ中平衡后气体的压强为开始时的0.875 倍,则a =_________________ 。
②容器Ⅱ平衡时的气体压强为p,用平衡分压代替平衡浓度表示的平衡常数K为_________ 。(3) 汽车使用乙醇汽油并不能减少NOx的排放,某研究小组在实验室以耐高温试剂Ag-ZSW-5催化,测得NO转化为N2的转化率随温度变化情况如下图所示。
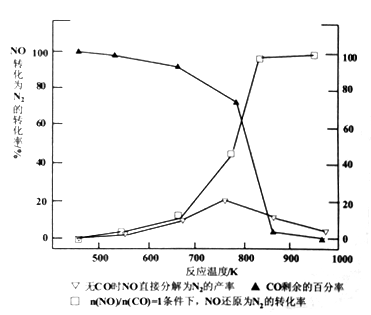
①在n(NO)/n(CO)=1条件下,最佳温度应控制在_____ 左右。
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为_______________ 。
③用平衡移动原理解释为什么加入CO后NO转化为N2的转化率增大?__________________ 。
(1)汽缸中生成 NO 的反应为:N2(g)+O2(g)
 2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):反应Ⅰ:NO(g)+CO(g)+Rh(s)
 RhN(s)+CO2(g) △H=-8 kcal·mol-1
RhN(s)+CO2(g) △H=-8 kcal·mol-1反应Ⅱ:RhN(s)+NO(g)
 Rh(s)+N2O △H =-76.4 kcal·mol -1
Rh(s)+N2O △H =-76.4 kcal·mol -1则由NO生成2 mol N2O的△H =
 N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应过程的能量变化图的是
N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应过程的能量变化图的是
(2)相同温度下,两个体积均为1L的恒容密闭容器中,发生反应:
2NO(g)+2CO (g)
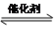 N2(g)+2CO2(g),有关物质的量如下表:
N2(g)+2CO2(g),有关物质的量如下表:| 容器 编号 | 起始物质的量/mol | 平衡物质的量/mol | |||
| NO | CO | N2 | CO2 | CO2 | |
| Ⅰ | 0.2 | 0.2 | 0 | 0 | a |
| Ⅱ | 0.3 | 0.3 | b | 0.1 | 0.2 |
①容器Ⅰ中平衡后气体的压强为开始时的0.875 倍,则a =
②容器Ⅱ平衡时的气体压强为p,用平衡分压代替平衡浓度表示的平衡常数K为

①在n(NO)/n(CO)=1条件下,最佳温度应控制在
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为
③用平衡移动原理解释为什么加入CO后NO转化为N2的转化率增大?
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
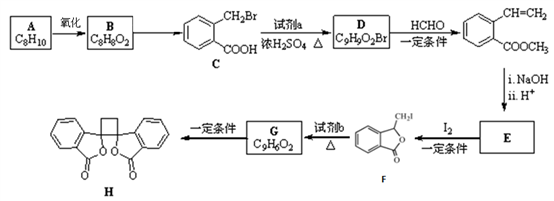
11. [化学一选修5:有机化学基础]具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:
已知:
ⅰ.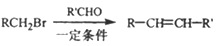
ⅱ.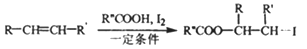
ⅲ.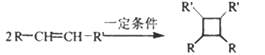
(以上R、R’、R”代表氢、或烃基等)
(1)A属于芳香烃,名称是______________ ,由B生成C的反应类型是________________ 。
(2)试剂a是_________________ ,HCHO的电子式是________________ 。
(3)E的结构简式是_________________ 。
(4)由F生成G的化学方程式是____________________ 。
(5)二取代芳香化合物W是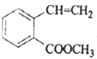 同分异构体,能使溴的四氯化碳溶液反应,能发生银镜反应,W共有
同分异构体,能使溴的四氯化碳溶液反应,能发生银镜反应,W共有____ 种(不含立体结构)。其中核磁共振氢谱为五组峰的结构简式为________ 。
(6)以乙醇为起始原料,结合已知信息选用必要的无机试剂合成 ,写出合成路线(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
,写出合成路线(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)__________________ 。

已知:
ⅰ.

ⅱ.

ⅲ.

(以上R、R’、R”代表氢、或烃基等)
(1)A属于芳香烃,名称是
(2)试剂a是
(3)E的结构简式是
(4)由F生成G的化学方程式是
(5)二取代芳香化合物W是
 同分异构体,能使溴的四氯化碳溶液反应,能发生银镜反应,W共有
同分异构体,能使溴的四氯化碳溶液反应,能发生银镜反应,W共有(6)以乙醇为起始原料,结合已知信息选用必要的无机试剂合成
 ,写出合成路线(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
,写出合成路线(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学与STSE、有机化学基础、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、常见无机物及其应用
试卷题型(共 11题)
题型
数量
单选题
7
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 化学科学对人类文明发展的意义 金属材料的性质及利用 化石能源 煤的干馏 | |
| 2 | 0.65 | 根据元素种类、原子个数、有机物类别确定分子式 氨基酸的两性 | |
| 3 | 0.65 | 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 盐类水解规律理解及应用 | |
| 4 | 0.65 | 电解原理的应用 电解原理的理解及判断 电解原理的应用实验 | |
| 5 | 0.4 | 元素周期律、元素周期表的推断 微粒半径大小的比较方法 根据物质性质进行元素种类推断 结合物质计算的元素周期律、元素周期表相关推断 | |
| 6 | 0.4 | 温度对化学平衡移动的影响 沉淀转化 淀粉水解及其产物检验相关实验 综合实验设计与评价 | |
| 7 | 0.65 | 原电池原理的综合应用 新型电池 | |
| 二、解答题 | |||
| 8 | 0.4 | 亚铁盐 酸碱中和滴定实质、原理 常见无机物的制备 探究物质组成或测量物质的含量 | 实验探究题 |
| 9 | 0.4 | 氧化还原反应方程式的配平 原电池电极反应式书写 常见无机物的制备 | 工业流程题 |
| 10 | 0.4 | 盖斯定律与热化学方程式 化学平衡的移动及其影响因素 化学平衡常数的有关计算 | 原理综合题 |
| 11 | 0.4 | 逆合成分析法 根据题给物质选择合适合成路线 有机合成综合考查 有机推断综合考查 | 有机推断题 |



