【全国百强校】江苏省泰州中学2018届高三第四次模拟理综化学试题
江苏
高三
模拟预测
2018-06-06
336次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、有机化学基础、化学实验基础、物质结构与性质、化学反应原理
【全国百强校】江苏省泰州中学2018届高三第四次模拟理综化学试题
江苏
高三
模拟预测
2018-06-06
336次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、有机化学基础、化学实验基础、物质结构与性质、化学反应原理
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
1. 党的十九大进一步强调加强生态文明建设,倡导绿水青山就是金山银山。下列做法不符合该理念的是
| A.燃煤发电 | B.植树造林 | C.普及新能源汽车 | D.节约用电 |
【知识点】 绿色化学与可持续发展解读 新能源的开发解读
您最近一年使用:0次
单选题
|
容易(0.94)
名校
2. 下列有关化学用语表示正确的是
| A.质子数为117,中子数为176的Ts原子:176117Ts |
B.Al3+的结构示意图: 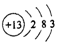 |
C.Na2O的电子式: 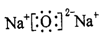 |
| D.磁性氧化铁的化学式:Fe2O3 |
您最近一年使用:0次
2018-05-29更新
|
458次组卷
|
3卷引用:【全国百强校】江苏省泰州中学2018届高三第四次模拟理综化学试题
单选题
|
容易(0.94)
名校
3. 下列有关物质性质与用途具有对应关系的是
| A.二氧化硫具有氧化性,可用于漂白纸浆 |
| B.葡萄糖具有还原性,可用于化学镀银 |
| C.氢氧化铝受热易分解,可用作胃酸中和剂 |
| D.生石灰能与水反应,可用来干燥氯气 |
【知识点】 二氧化硫 氢氧化铝的物理性质及用途解读 葡萄糖和果糖
您最近一年使用:0次
2018-05-29更新
|
555次组卷
|
2卷引用:【全国百强校】江苏省泰州中学2018届高三第四次模拟理综化学试题
单选题
|
较易(0.85)
名校
5. 短周期主族元素X、Y、Z、W的原子序数依次增大,其中X原子最外层电子数是内层电子数的两倍,元素Y的核电荷数等于W原子的最外层电子数,Z在空气中燃烧发出耀眼的白光。下列说法正确的是
| A.X和Y的氧化物都是可导致酸雨的污染物 |
| B.Z和W形成的化合物中既有离子键又有共价键 |
| C.最高价氧化物对应水化物的酸性由强到弱的顺序:W、Y、X |
| D.原子半径由大到小的顺序:r(X)>r(Y)>r(Z) |
您最近一年使用:0次
2018-05-29更新
|
529次组卷
|
4卷引用:【全国百强校】江苏省泰州中学2018届高三第四次模拟理综化学试题
【全国百强校】江苏省泰州中学2018届高三第四次模拟理综化学试题(已下线)2018年高考题及模拟题汇编 专题06 物质结构 元素周期律【全国百强校】山西省平遥中学2019届高三上学期11月质检化学试题甘肃省武威市第十八中学2019届高三上学期期末考试化学试题
单选题
|
较易(0.85)
名校
6. 下列指定反应的离子方程式正确的是
| A.用氨水吸收足量的SO2气体:2OH-+SO2=SO32-+H2O |
| B.NaClO将污水中的NH3氧化成N2: 3ClO-+2NH3=N2↑+3C1-+3H2O |
| C.酸性条件下,用H2O2将Fe2+转化为Fe3+:H2O2+Fe2++2H+=Fe3++2H2O |
| D.NH4Al(SO4)2溶液与过量NaOH溶液反应:A13++4OH-=AlO2-+2H2O |
【知识点】 离子方程式的正误判断解读
您最近一年使用:0次
2018-05-29更新
|
538次组卷
|
5卷引用:【全国百强校】江苏省泰州中学2018届高三第四次模拟理综化学试题
单选题
|
容易(0.94)
名校
7. 在给定条件下,下列选项所示的物质转化均能实现的是
A.S SO2 SO2 CaSO4 CaSO4 |
B.Si SiO2 SiO2 SiCl4 SiCl4 |
C.Fe Fe2O3 Fe2O3 Fe(OH)3 Fe(OH)3 |
D.Na NaOH(aq) NaOH(aq)  NaHCO3(aq) NaHCO3(aq) |
您最近一年使用:0次
2018-05-29更新
|
856次组卷
|
5卷引用:【全国百强校】江苏省泰州中学2018届高三第四次模拟理综化学试题
单选题
|
适中(0.65)
名校
8. 煤燃烧排放的烟气含有SO2和NOx,会污染大气。采用NaClO、Ca(C1O)2溶液作为吸收剂可同时对烟气进行税硫、脱硝,下列说法正确的是
①SO2(g)+2OH-(aq) SO32-(aq)+H2O(l) ΔH1=a KJ/mol
SO32-(aq)+H2O(l) ΔH1=a KJ/mol
②ClO-(aq)+SO32-(aq) SO42-(aq)+Cl-(aq) ΔH2=b KJ/mol
SO42-(aq)+Cl-(aq) ΔH2=b KJ/mol
③CaSO4(s) Ca2+(aq)+ SO42- (aq) ΔH3=c KJ/mol
Ca2+(aq)+ SO42- (aq) ΔH3=c KJ/mol
④SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq) CaSO4(s)+H2O(l)+Cl-(aq)ΔH4=dKJ/mol
CaSO4(s)+H2O(l)+Cl-(aq)ΔH4=dKJ/mol
①SO2(g)+2OH-(aq)
 SO32-(aq)+H2O(l) ΔH1=a KJ/mol
SO32-(aq)+H2O(l) ΔH1=a KJ/mol②ClO-(aq)+SO32-(aq)
 SO42-(aq)+Cl-(aq) ΔH2=b KJ/mol
SO42-(aq)+Cl-(aq) ΔH2=b KJ/mol③CaSO4(s)
 Ca2+(aq)+ SO42- (aq) ΔH3=c KJ/mol
Ca2+(aq)+ SO42- (aq) ΔH3=c KJ/mol④SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)
 CaSO4(s)+H2O(l)+Cl-(aq)ΔH4=dKJ/mol
CaSO4(s)+H2O(l)+Cl-(aq)ΔH4=dKJ/mol| A.随着吸收反应的进行,吸收剂溶液的pH逐渐减小 |
| B.反应①、②均为氧化还原反应 |
| C.反应Ca(OH)2(aq)+H2SO4(aq)=CaSO4(s)+2H2O(1)的ΔH=-ckJ/mol |
| D.d=a+b+c |
【知识点】 氧化还原反应基本概念 盖斯定律及其有关计算
您最近一年使用:0次
2018-05-29更新
|
721次组卷
|
6卷引用:【全国百强校】江苏省泰州中学2018届高三第四次模拟理综化学试题
单选题
|
较易(0.85)
名校
9. 常温下,下列各组离子在指定溶液中能大量共存的是
| A.无色透明的溶液中: NH4+、Fe3+、SO42-、OH- |
| B.c(NO3-)=1mol/L的溶液中:H+、Fe2+、SO42-、Cl- |
| C.能使甲基橙变红的溶液中: Na+、NH4+、SO42-、NO3- |
| D.c(H+)/c(OH-)=1×10l2的溶液中: Ca2+、Na+、SiO32-、HCO3- |
【知识点】 限定条件下的离子共存解读
您最近一年使用:0次
单选题
|
较易(0.85)
名校
10. 生物脱H2S的原理为:
反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4FeSO4+O2+2H2SO4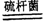 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,氧化速率随温度和pH变化如下图。下列说法正确的是

反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4FeSO4+O2+2H2SO4
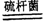 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,氧化速率随温度和pH变化如下图。下列说法正确的是

| A.该过程最终将H2S转化为Fe2(SO4)3 |
| B.H+是反应2的反应物,c(H+)越大反应速率越快 |
| C.反应1消耗11.2LH2S,转移的电子数目约为6.0×1023个 |
| D.反应温度过高,Fe2+氧化速率下降,其原因可能是硫感菌失去活性 |
【知识点】 氧化还原反应有关计算 化学反应原理综合考查解读
您最近一年使用:0次




