10. 直接排放SO
2、NO
2会危害环境。工业上常采用化学方法控制污染。
(1)下图是1mol CH
4完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化。

①CH
4完全燃烧的活化能是
_____________kJ/mol
②在催化剂作用下,CH
4可以还原SO
2生成单质S(g)、H
2O(g)和CO
2,写出该反应的热化学方程式
_____________________________;
(2)为减少SO
2排放,将含SO
2的烟气通过洗涤剂X,充分吸收后再向吸收后的溶液中加入稀硫酸,既可以回收

,同时又可得到化肥。X可以是
__________(填序号)。
a.Ca(OH)
2 b.K
2CO
3 c.Na
2SO
3 d.NH
3·H
2O
(3)对NO
2+SO
2
SO
3+NO
△H<0反应进行探究:在固定体积的密闭容器中,使用某种催化剂,改变原料气配比进行多组实验(各次实验的温度可能相同,也可能不同),测定NO
2的平衡转化率。实验结果如图所示:
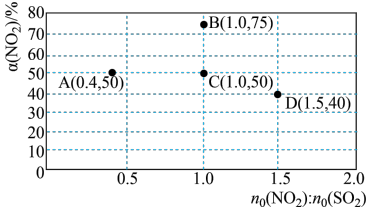
①能够加快该化学反应速率的外界条件是
___________________a.降低温度
b.增大压强
c.升高温度
d.减小压强
②如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是
___________;
③若A点对应实验中,SO
2(g)的起始浓度为c
0mol/L,经过

min达到平衡状态,该时段化学反应速率v(NO
2)
___mol/(L·min);
④图中C、D两点对应的实验温度分别为

和
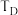
,计算判断
 ______
______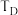
(填>、=、或<)