2020届高三化学二轮每周大题必练— —— 无机物制备实验流程
全国
高三
专题练习
2020-01-11
122次
整体难度:
适中
考查范围:
化学反应原理、常见无机物及其应用、化学实验基础、物质结构与性质
2020届高三化学二轮每周大题必练— —— 无机物制备实验流程
全国
高三
专题练习
2020-01-11
122次
整体难度:
适中
考查范围:
化学反应原理、常见无机物及其应用、化学实验基础、物质结构与性质
一、解答题 添加题型下试题
1. 为了实现资源利用最大化,某化工厂将合成氨、制纯碱和生产尿素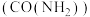 工艺联合,简易流程如下:
工艺联合,简易流程如下:
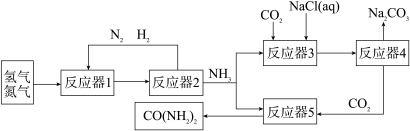
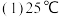 时101kPa时,测得生成17g
时101kPa时,测得生成17g  ,放出
,放出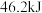 热量,写出合成
热量,写出合成 的热化学方程式
的热化学方程式 ______ .
 合成氨原料气中的杂质硫化氢用稀氨水吸收,副产品是酸式盐.该副产品的化学式为
合成氨原料气中的杂质硫化氢用稀氨水吸收,副产品是酸式盐.该副产品的化学式为 ______ .
 反应器2分离出来的氮气和氢气再通入反应器1,其目的是
反应器2分离出来的氮气和氢气再通入反应器1,其目的是 ______  向反应器3充入原料的顺序是:先加氯化钠溶液,通入氨气至饱和,再通入足量的二氧化碳可制得
向反应器3充入原料的顺序是:先加氯化钠溶液,通入氨气至饱和,再通入足量的二氧化碳可制得 反应器3中的化学方程式为
反应器3中的化学方程式为 ______ .
 工业上可用碳、甲烷与水蒸气反应制氢气
工业上可用碳、甲烷与水蒸气反应制氢气
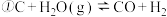 ,
, ,此反应的化学平衡常数表达式为
,此反应的化学平衡常数表达式为
______ ,为了提高碳的转化率,宜采用下列措施中的 填字母编号
填字母编号
______ .
A.增大压强 增加碳的量
增加碳的量  升高温度
升高温度 增加水的量
增加水的量 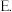 使用催化剂
使用催化剂 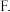 及时移出CO、
及时移出CO、
 有些国家水电丰富,采用惰性电极电解硫酸钠溶液制氢气,电解时阳极上的电极反应式为
有些国家水电丰富,采用惰性电极电解硫酸钠溶液制氢气,电解时阳极上的电极反应式为 ______ .
 若仅以
若仅以 、空气、
、空气、 为原料制尿素
为原料制尿素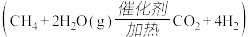 ,标准状况下
,标准状况下
 ,理论上最多能制
,理论上最多能制 ______ 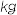 尿素.
尿素.
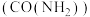 工艺联合,简易流程如下:
工艺联合,简易流程如下: 
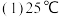 时101kPa时,测得生成17g
时101kPa时,测得生成17g  ,放出
,放出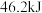 热量,写出合成
热量,写出合成 的热化学方程式
的热化学方程式  合成氨原料气中的杂质硫化氢用稀氨水吸收,副产品是酸式盐.该副产品的化学式为
合成氨原料气中的杂质硫化氢用稀氨水吸收,副产品是酸式盐.该副产品的化学式为  反应器2分离出来的氮气和氢气再通入反应器1,其目的是
反应器2分离出来的氮气和氢气再通入反应器1,其目的是  向反应器3充入原料的顺序是:先加氯化钠溶液,通入氨气至饱和,再通入足量的二氧化碳可制得
向反应器3充入原料的顺序是:先加氯化钠溶液,通入氨气至饱和,再通入足量的二氧化碳可制得 反应器3中的化学方程式为
反应器3中的化学方程式为  工业上可用碳、甲烷与水蒸气反应制氢气
工业上可用碳、甲烷与水蒸气反应制氢气 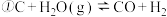 ,
, ,此反应的化学平衡常数表达式为
,此反应的化学平衡常数表达式为
 填字母编号
填字母编号
A.增大压强
 增加碳的量
增加碳的量  升高温度
升高温度 增加水的量
增加水的量 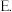 使用催化剂
使用催化剂 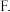 及时移出CO、
及时移出CO、
 有些国家水电丰富,采用惰性电极电解硫酸钠溶液制氢气,电解时阳极上的电极反应式为
有些国家水电丰富,采用惰性电极电解硫酸钠溶液制氢气,电解时阳极上的电极反应式为  若仅以
若仅以 、空气、
、空气、 为原料制尿素
为原料制尿素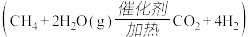 ,标准状况下
,标准状况下
 ,理论上最多能制
,理论上最多能制 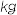 尿素.
尿素.
您最近一年使用:0次
2020-01-07更新
|
133次组卷
|
2卷引用:2020届高三化学二轮每周大题必练— —— 无机物制备实验流程
2. 以明矾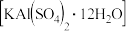 为原料制备Al、
为原料制备Al、 和
和 的工艺流程如下:
的工艺流程如下:
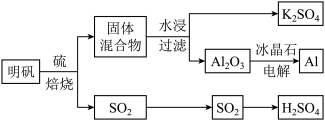
依据上述流程图回答下列问题:
 写出明矾和硫单质混合焙烧发生反应的化学方程式
写出明矾和硫单质混合焙烧发生反应的化学方程式______ .
 从水浸后的滤液中得到
从水浸后的滤液中得到 晶体的方法是蒸发浓缩、
晶体的方法是蒸发浓缩、______ 、过滤,实验室在蒸发浓缩过程中用到的主要仪器有______ .
 电解
电解 时加入冰晶石的作用是
时加入冰晶石的作用是______ .
 以Al和
以Al和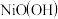 为电极,NaOH溶液为电解液组成一种新型电池,放电时
为电极,NaOH溶液为电解液组成一种新型电池,放电时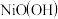 转化为
转化为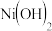 ,该电池反应的化学方程式是
,该电池反应的化学方程式是______ .
 焙烧产生的
焙烧产生的 可用于制硫酸.已知
可用于制硫酸.已知 ,101kPa时:
,101kPa时:
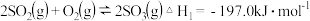

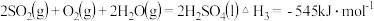
则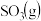 和
和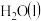 反应的热化学方程式是
反应的热化学方程式是______ .
 焙烧948吨明矾
焙烧948吨明矾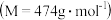 ,若
,若 的利用率为
的利用率为 ,则可生产多少吨质量分数为
,则可生产多少吨质量分数为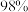 的硫酸?
的硫酸?
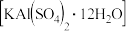 为原料制备Al、
为原料制备Al、 和
和 的工艺流程如下:
的工艺流程如下:
依据上述流程图回答下列问题:
 写出明矾和硫单质混合焙烧发生反应的化学方程式
写出明矾和硫单质混合焙烧发生反应的化学方程式 从水浸后的滤液中得到
从水浸后的滤液中得到 晶体的方法是蒸发浓缩、
晶体的方法是蒸发浓缩、 电解
电解 时加入冰晶石的作用是
时加入冰晶石的作用是 以Al和
以Al和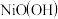 为电极,NaOH溶液为电解液组成一种新型电池,放电时
为电极,NaOH溶液为电解液组成一种新型电池,放电时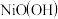 转化为
转化为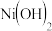 ,该电池反应的化学方程式是
,该电池反应的化学方程式是 焙烧产生的
焙烧产生的 可用于制硫酸.已知
可用于制硫酸.已知 ,101kPa时:
,101kPa时: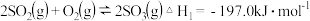

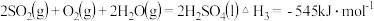
则
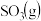 和
和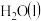 反应的热化学方程式是
反应的热化学方程式是 焙烧948吨明矾
焙烧948吨明矾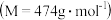 ,若
,若 的利用率为
的利用率为 ,则可生产多少吨质量分数为
,则可生产多少吨质量分数为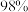 的硫酸?
的硫酸?
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
3. 用硼镁矿 主要成分为
主要成分为 ,含少量
,含少量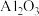 和
和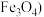 制取粗硼的工艺流程为:
制取粗硼的工艺流程为:
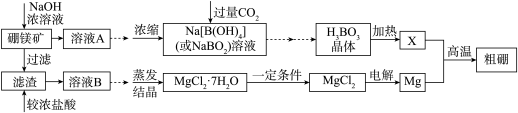
已知: 硼与铝的性质相似,也能与氢氧化钠溶液反应.
硼与铝的性质相似,也能与氢氧化钠溶液反应.
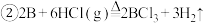
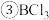 的熔点为
的熔点为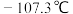 ,沸点为
,沸点为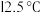 ,在潮湿空气中易形成白雾.
,在潮湿空气中易形成白雾.
I.回答下列问题:
 证明溶液B中含有铁元素的方法是
证明溶液B中含有铁元素的方法是 ______
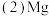 与X反应制取粗硼的化学方程式
与X反应制取粗硼的化学方程式 ______
 上图中制取
上图中制取 的“一定条件”是指
的“一定条件”是指 ______
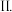 某同学设计如图所示装置制备三氯化硼.
某同学设计如图所示装置制备三氯化硼.
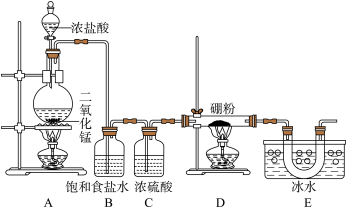
回答下列问题:
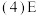 装置的作用是
装置的作用是 ______ .
 如果去掉B装置,可能的后果是
如果去掉B装置,可能的后果是 ______ .
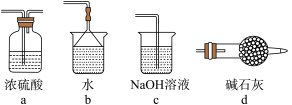
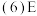 装置后面还应连接的一个装置是
装置后面还应连接的一个装置是 ______ .
 主要成分为
主要成分为 ,含少量
,含少量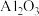 和
和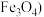 制取粗硼的工艺流程为:
制取粗硼的工艺流程为: 
已知:
 硼与铝的性质相似,也能与氢氧化钠溶液反应.
硼与铝的性质相似,也能与氢氧化钠溶液反应. 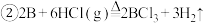
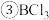 的熔点为
的熔点为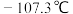 ,沸点为
,沸点为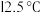 ,在潮湿空气中易形成白雾.
,在潮湿空气中易形成白雾. I.回答下列问题:
 证明溶液B中含有铁元素的方法是
证明溶液B中含有铁元素的方法是 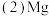 与X反应制取粗硼的化学方程式
与X反应制取粗硼的化学方程式  上图中制取
上图中制取 的“一定条件”是指
的“一定条件”是指 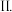 某同学设计如图所示装置制备三氯化硼.
某同学设计如图所示装置制备三氯化硼. 
回答下列问题:
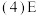 装置的作用是
装置的作用是  如果去掉B装置,可能的后果是
如果去掉B装置,可能的后果是 
 装置后面还应连接的一个装置是
装置后面还应连接的一个装置是 【知识点】 铝土矿提取铝的综合考查解读 物质制备的探究解读
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
4. 金属镓有“电子工业脊梁”的美誉,它与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如下图所示:

(1)元素Ga位于Al的下一周期,写出镓(Ga)的原子结构示意图为____________ CO2的电子式为_____________________
(2)下列有关Al、Ga的说法不正确的是______
A.由流程图可知酸性:Al(OH)3>Ga(OH)3 B.Ga2O3可与盐酸反应生成GaCl3
C.Ga(OH)3可由Ga2O3与水反应得到 D.与酸反应的剧烈程度:Al<Ga
(3)图中涉及到的Al、Na、O三种元素简单离子半径由大到小的顺序_____________
(4)步骤二中不能通入过量的CO2,理由_________________ (用离子方程式表示)
(5)工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含Zn、Fe、Cu杂质,以NaOH水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:Zn2+<Ga3+<Fe2+)
①下列有关电解精炼说法正确的是_______
A.阳极发生氧化反应,其主要电极反应式:Ga-3e- ═ Ga3+
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.在阴极除了析出高纯度的镓之外,还有H2产生
D.电解后,电解槽底部的阳极泥中只有Cu和Fe
②阴极析出高纯度镓的电极反应式__________________________________
(6)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。氮化镓(GaN)的一种制备方法是采用GaCl3与NH3在一定条件下反应,写出该反应的化学方程式__________________

(1)元素Ga位于Al的下一周期,写出镓(Ga)的原子结构示意图为
(2)下列有关Al、Ga的说法不正确的是
A.由流程图可知酸性:Al(OH)3>Ga(OH)3 B.Ga2O3可与盐酸反应生成GaCl3
C.Ga(OH)3可由Ga2O3与水反应得到 D.与酸反应的剧烈程度:Al<Ga
(3)图中涉及到的Al、Na、O三种元素简单离子半径由大到小的顺序
(4)步骤二中不能通入过量的CO2,理由
(5)工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含Zn、Fe、Cu杂质,以NaOH水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:Zn2+<Ga3+<Fe2+)
①下列有关电解精炼说法正确的是
A.阳极发生氧化反应,其主要电极反应式:Ga-3e- ═ Ga3+
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.在阴极除了析出高纯度的镓之外,还有H2产生
D.电解后,电解槽底部的阳极泥中只有Cu和Fe
②阴极析出高纯度镓的电极反应式
(6)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。氮化镓(GaN)的一种制备方法是采用GaCl3与NH3在一定条件下反应,写出该反应的化学方程式
您最近一年使用:0次
2019-04-01更新
|
758次组卷
|
4卷引用:【校级联考】天津市十二重点中学2019届高三下学期毕业班联考(一)化学试题
【校级联考】天津市十二重点中学2019届高三下学期毕业班联考(一)化学试题2020届高三化学二轮每周大题必练— —— 无机物制备实验流程(已下线)第五单元 元素周期表和元素周期律测试题-2021年高考化学一轮复习名师精讲练黑龙江省哈尔滨师范大学青冈实验中学校2020-2021学年高二上学期开学考试化学试题
解答题-工业流程题
|
适中(0.65)
解题方法
5. ZnSe是一种光电性能优异的半导体材料,某研究小组用如图1方法制备了ZnSe.
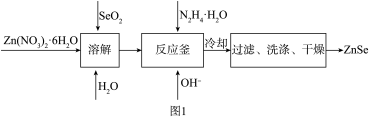
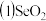 溶于水生成
溶于水生成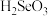 ,下列物质与水反应,跟此反应类型相同的是
,下列物质与水反应,跟此反应类型相同的是 ______

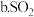

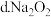
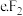
 硒酸
硒酸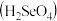 的水溶液按下式发生一级和二级电离:
的水溶液按下式发生一级和二级电离: ;
; ,
,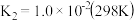
 溶液显
溶液显 ______  填“酸性”、“中性”、“碱性”
填“酸性”、“中性”、“碱性” .
.
 向
向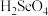 溶液中滴加少量氨水,该反应的离子方程式为
溶液中滴加少量氨水,该反应的离子方程式为 ______ .
 已知
已知 的两级电离常数分别为
的两级电离常数分别为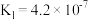 ,
, ,则
,则 和
和 两溶液混合后反应的离子方程式为
两溶液混合后反应的离子方程式为 ______ .
 肼
肼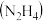 与
与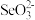 反应的氧化产物是
反应的氧化产物是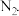 氧化剂与还原剂的物质的量之比为
氧化剂与还原剂的物质的量之比为 ______ .
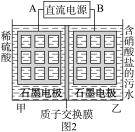
 电化学降解法可用于治理水中硝酸盐的污染,所得产物可直接排入大气.其原理如图2所示,其中B为电源的
电化学降解法可用于治理水中硝酸盐的污染,所得产物可直接排入大气.其原理如图2所示,其中B为电源的 ______ 极,乙池中电极反应式为 ______ ,为使反应持续进行,须适时向甲池中添加 ______ .


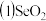 溶于水生成
溶于水生成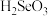 ,下列物质与水反应,跟此反应类型相同的是
,下列物质与水反应,跟此反应类型相同的是 
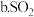

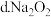
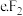
 硒酸
硒酸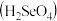 的水溶液按下式发生一级和二级电离:
的水溶液按下式发生一级和二级电离: ;
; ,
,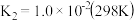
 溶液显
溶液显  填“酸性”、“中性”、“碱性”
填“酸性”、“中性”、“碱性” .
. 向
向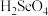 溶液中滴加少量氨水,该反应的离子方程式为
溶液中滴加少量氨水,该反应的离子方程式为  已知
已知 的两级电离常数分别为
的两级电离常数分别为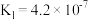 ,
, ,则
,则 和
和 两溶液混合后反应的离子方程式为
两溶液混合后反应的离子方程式为  肼
肼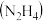 与
与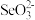 反应的氧化产物是
反应的氧化产物是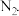 氧化剂与还原剂的物质的量之比为
氧化剂与还原剂的物质的量之比为  电化学降解法可用于治理水中硝酸盐的污染,所得产物可直接排入大气.其原理如图2所示,其中B为电源的
电化学降解法可用于治理水中硝酸盐的污染,所得产物可直接排入大气.其原理如图2所示,其中B为电源的
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
适中(0.65)
6. 学生设计的用氨催化法制取少量HNO3溶液的实验装置如图所示:

(1)实验室制备NH3,下列方法中适宜选用的是_________ (填序号)。
①固态氯化铵与熟石灰混合加热 ②固态氯化铵加热分解
③碱石灰中滴加浓氨水 ④氯化铵溶液与氢氧化钠溶液共热
(2)装置B中发生反应的化学方程式为_________________________________________ ;
(3)装置C的作用是_________________________________________________________ ;
装置C中的现象是____________________________________________________________ ;为确保装置D中尽可能多地生成HNO3,所通入O2和NH3的体积比应大于___________ ;
(4)装置D中发生的反应化学方程式为___________________________________________ 。

(1)实验室制备NH3,下列方法中适宜选用的是
①固态氯化铵与熟石灰混合加热 ②固态氯化铵加热分解
③碱石灰中滴加浓氨水 ④氯化铵溶液与氢氧化钠溶液共热
(2)装置B中发生反应的化学方程式为
(3)装置C的作用是
装置C中的现象是
(4)装置D中发生的反应化学方程式为
您最近一年使用:0次
2016-05-23更新
|
406次组卷
|
2卷引用:2015-2016学年福建省龙海市程溪中学高一下学期期中化学试卷



