工业上合成氨,CO易与铁触媒作用导致铁触媒失去催化活性:Fe+5CO═Fe(CO)5.为了防止催化剂铁触媒中毒,要除去CO,发生的反应为Cu(NH3)2OOCCH3+CO+NH3═Cu(NH3)3(CO)OOCCH3.回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最低的是______ (填字母序号)。
a.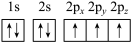 b.
b. 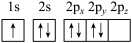
c.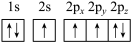 d.
d. 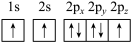
(2)写出CO的一种常见等电子体分子的结构式:______ ;C、N、O的第一电离能由大到小的顺序为______ (用元素符号表示)。
(3)与O同族的元素还有S、Se、Te,它们氢化物的沸点大小为H2O>H2Te>H2Se>H2S,其原因是______ 。
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价,则其中碳原子的杂化轨道类型是______ ,NH3分子的价电子对互斥理论模型是______ 。
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:

①若坐标参数A为(0,0,0),B为(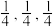 ),则C的坐标参数为
),则C的坐标参数为______ ;
②若阿伏加 德罗常数为NA,该晶胞的边长为a pm,则晶体的密度为______ g•cm-3。
(1)下列氮原子的电子排布图表示的状态中,能量最低的是
a.
 b.
b. 
c.
 d.
d. 
(2)写出CO的一种常见等电子体分子的结构式:
(3)与O同族的元素还有S、Se、Te,它们氢化物的沸点大小为H2O>H2Te>H2Se>H2S,其原因是
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价,则其中碳原子的杂化轨道类型是
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:

①若坐标参数A为(0,0,0),B为(
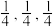 ),则C的坐标参数为
),则C的坐标参数为②若阿伏加 德罗常数为NA,该晶胞的边长为a pm,则晶体的密度为
更新时间:2020-04-27 20:29:36
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】氮化硼(BN)被称为一种“宇宙时代的材料”,具有很大的硬度。
(1)基态硼原子有__________ 个未成对电子,氮离子的电子排布式为__________ 。
(2)部分硼的化合物有以下转化: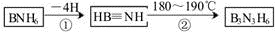
则下列叙述正确的是__________ (填序号);
A.B3N3H6俗称无机苯,但不是平面分子
B.BNH6与乙烷是等电子体
C.HB≡NH中的硼原子、氮原子的杂化类型相同
D.硼、氮、氧三元素的第一电离能比较:B<N<O
(3)下图的晶体结构中,黑球白球分别代表不同的原子、离子或分子,则图1的晶胞中含有的粒子总数为__________ ;图2中的白球的配位数是__________ 。
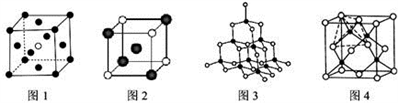
(4)已知图3、4均表示BN晶体的结构,制备氮化硼的原理为:BCl3+2NH3=BN+2HCl+NH4Cl,当该反应中有1mol BN生成时,则反应中可形成__________ mol配位键,比较氮化硼晶体与晶体硅的沸点高低并解释原因________________________
(1)基态硼原子有
(2)部分硼的化合物有以下转化:

则下列叙述正确的是
A.B3N3H6俗称无机苯,但不是平面分子
B.BNH6与乙烷是等电子体
C.HB≡NH中的硼原子、氮原子的杂化类型相同
D.硼、氮、氧三元素的第一电离能比较:B<N<O
(3)下图的晶体结构中,黑球白球分别代表不同的原子、离子或分子,则图1的晶胞中含有的粒子总数为

(4)已知图3、4均表示BN晶体的结构,制备氮化硼的原理为:BCl3+2NH3=BN+2HCl+NH4Cl,当该反应中有1mol BN生成时,则反应中可形成
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】I.锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]____ ,有____ 个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是_____ 。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______ 。
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______ 。
Ⅱ.周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(5)b、c、d中第一电离能最大的是_____ (填元素符号),e的价层电子排布图为______ 。
(6)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为_____ ;分子中既含有极性共价键、又含有非极性共价键的化合物是_____ (填化学式,写出两种)。
(7)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是_____ (任写一种);酸根呈三角锥结构的酸是______ (填化学式)。
(8)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构、阳离子呈轴向狭长的八面体结构(如图所示)。该化合物中,阴离子为_____ ,阳离子中存在的化学键类型有_____ ;该化合物加热时首先失去的组分是____ ,判断理由是_____ 。

(1)基态Ge原子的核外电子排布式为[Ar]
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是
Ⅱ.周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(5)b、c、d中第一电离能最大的是
(6)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为
(7)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是
(8)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构、阳离子呈轴向狭长的八面体结构(如图所示)。该化合物中,阴离子为

您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】铜是人类最早使用的金属之一,其单质及化合物具有广泛的用途。
(1)基态铜原子核外有________ 对自旋相反的电子。
(2)青铜是铜与锡或铅等元素按一定比例熔铸而成的合金。第一电离能I1(Sn)____________ I1(Pb)(填“大于”或“小于”)。
(3)新制的Cu(OH)2能够溶解于浓氨水中,反应的离子方程式是____________________________________ ;
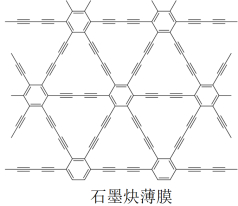
(4)利用铜片表面催化反应,我国研究人员用六炔基苯为原料,在世界上首次通过化学方法获得全碳材料—石墨炔薄膜(结构片段如图所示),开辟了人工化学合成碳同素异形体的先例。石墨炔中碳原子_________________________ 的杂化方式。
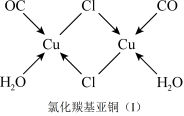
(5)CuCl的盐酸溶液能吸收CO形成氯化羰基亚铜(I),可用于定量测定气体混合物中CO的含量。氯化羰基亚铜(I)中含___________ σ键数目。
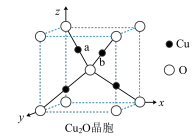
(6)Cu2O可用于半导体材料。
①Cu2O晶胞(如图所示)中,O原子的配位数为________________ ;a位置Cu+坐标为(0.25,0.25,0.75),则b位置Cu+坐标_______________________ 。
②Cu2S与Cu2O具有相似晶体结构,则两者的熔点是Cu2O比Cu2S的_________ (填“高”或“低”),请解释原因___________________ 。
(1)基态铜原子核外有
(2)青铜是铜与锡或铅等元素按一定比例熔铸而成的合金。第一电离能I1(Sn)
(3)新制的Cu(OH)2能够溶解于浓氨水中,反应的离子方程式是
(4)利用铜片表面催化反应,我国研究人员用六炔基苯为原料,在世界上首次通过化学方法获得全碳材料—石墨炔薄膜(结构片段如图所示),开辟了人工化学合成碳同素异形体的先例。石墨炔中碳原子



(5)CuCl的盐酸溶液能吸收CO形成氯化羰基亚铜(I),可用于定量测定气体混合物中CO的含量。氯化羰基亚铜(I)中含
(6)Cu2O可用于半导体材料。
①Cu2O晶胞(如图所示)中,O原子的配位数为
②Cu2S与Cu2O具有相似晶体结构,则两者的熔点是Cu2O比Cu2S的
您最近半年使用:0次
【推荐1】利用钛矿的酸性废液(含TiO2+、Fe2+、Fe3+、 等),可回收获得FeS2纳米材料、Fe2O3和TiO2·nH2O等产品,流程如下:
等),可回收获得FeS2纳米材料、Fe2O3和TiO2·nH2O等产品,流程如下:
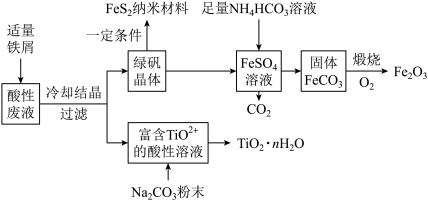
(1)TiO2+中钛元素的化合价为_____ 价。TiO2+只能存在于强酸性溶液中,因为TiO2+易水解生成TiO2·nH2O,写出水解的离子方程式:_____ 。
(2)向富含TiO2+的酸性溶液中加入Na2CO3粉末能得到固体TiO2·nH2O。请用化学反应原理解释:_____ 。
(3)NHHCO3溶液与FeSO4溶液反应的离子方程式为_____ ,该反应需温度在308K以下,其目的是_____ 。
(4)Fe2+的外层电子排布式为_____ 。
(5)实验室常用KSCN溶液来检验Fe3+的存在,与SCN互为等电子体的分子有_____ (写一个物质即可)
 等),可回收获得FeS2纳米材料、Fe2O3和TiO2·nH2O等产品,流程如下:
等),可回收获得FeS2纳米材料、Fe2O3和TiO2·nH2O等产品,流程如下:
(1)TiO2+中钛元素的化合价为
(2)向富含TiO2+的酸性溶液中加入Na2CO3粉末能得到固体TiO2·nH2O。请用化学反应原理解释:
(3)NHHCO3溶液与FeSO4溶液反应的离子方程式为
(4)Fe2+的外层电子排布式为
(5)实验室常用KSCN溶液来检验Fe3+的存在,与SCN互为等电子体的分子有
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】【化学——选修3:物质结构与性质】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的核外电子排布式为 1 ,有 2 个未成对电子。
(2)磷的一种同素异形体——白磷(P4)的立体构型为 3 ,其键角为 4 ,推测其在CS2中的溶解度 5 (填“大于”或“小于”)在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6º和107º,试分析PH3的键角小于NH3的原因 6 。
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为 7 ,其中心原子杂化轨道类型为 8 ,B为 9 。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点 10 (填“高于”或“低于”)金刚石熔点。
已知其B—P键长均为x cm,则其密度为 11 g﹒cm—3(列出计算式即可)。
(1)基态P原子的核外电子排布式为
(2)磷的一种同素异形体——白磷(P4)的立体构型为
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6º和107º,试分析PH3的键角小于NH3的原因

(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点
已知其B—P键长均为x cm,则其密度为
您最近半年使用:0次
【推荐3】盐酸、硝酸、硫酸在工业生产中具有重要的作用。
(1)“王水”是浓盐酸和浓硝酸按体积比3: l组成的混合物,“王水”溶金的原理为HNO3+3HCl=Cl2+NOCl+2H2O,金离子与氯离子形成AuCl4-离子,增强了金属的还原能力。
① 试写出金与王水反应生成H[AuCl4]的化学方程式:_________ ;其中AuCl4-的配位数是________ ;
② 已知:NOCl的熔点-645℃,沸点-5.5℃,NOCl固体的晶体类型是__________ ;
③ 组成NOCl分子的三种元素中,电负性N_____ O(填“>”、“<”或“=”);熔沸点H2O____ NH3(填“>”、“<”或“=”);与NH3互为等电子体的阳离子有________ (写出一种即可)。
(2)硝酸在有机反应中也有重要用途。TNT炸药、苦味酸是硝酸与甲苯、苯酚发生取代反应制成的。其中甲苯分子中碳原子的杂化方式为______ , 1mol甲苯分子中含有σ键的数目为_____ ;试解释在水中苯酚溶解度大于甲苯的原因________ 。
(3)在硝酸工业中有一种重要金属即为Cu,CuCl晶胞结构如图所示。已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,则该晶胞边长为_______ pm (只写计算式)。
(1)“王水”是浓盐酸和浓硝酸按体积比3: l组成的混合物,“王水”溶金的原理为HNO3+3HCl=Cl2+NOCl+2H2O,金离子与氯离子形成AuCl4-离子,增强了金属的还原能力。
① 试写出金与王水反应生成H[AuCl4]的化学方程式:
② 已知:NOCl的熔点-645℃,沸点-5.5℃,NOCl固体的晶体类型是
③ 组成NOCl分子的三种元素中,电负性N
(2)硝酸在有机反应中也有重要用途。TNT炸药、苦味酸是硝酸与甲苯、苯酚发生取代反应制成的。其中甲苯分子中碳原子的杂化方式为

(3)在硝酸工业中有一种重要金属即为Cu,CuCl晶胞结构如图所示。已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,则该晶胞边长为
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】金属钛因为其优越的性能被称为“未来金属”,其工业冶炼涉及到的反应如下:TiO2+2C+2Cl2 TiCl4+2CO
TiCl4+2CO
回答下列相关问题:
(1)钛的价层电子排布式为______________ 。
(2)已知部分物质熔沸点如下:
表中金刚石的晶型为_________ ;自左向右,表中的三种钛的卤化物熔沸点依次升高的原因是_____________ 。
(3)配位数为6,组成为TiCl3·6H2O 的晶体有两种:化学式为[TiCl( H2O)5]Cl2·H2O 的 X呈绿色,定量实验表明,X与AgNO3以1:2物质的量比反应生成沉淀。Y呈紫色,且Y 与AgNO3以1:3物质的量比反应生成沉淀,则Y的化学式为___________ ,Y配离子的空间构型为_________ 。
(4)钙钛矿是重要的含钛矿物之一,其主要成分Z的晶胞如下图所示:
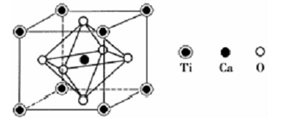
推测Z的化学式为________________ 。
(5)若晶胞参数a=384.1pm,Z晶体的密度为______ g/cm3( 已知 NA≈6.0×1023;3.8413≈ )。
)。
 TiCl4+2CO
TiCl4+2CO回答下列相关问题:
(1)钛的价层电子排布式为
(2)已知部分物质熔沸点如下:
名称 | 金红石 | 金刚石 | 四氯化钛 | 四溴化钛 | 四碘化钛 |
化学式 | TiO2 | C | TiCl4 | TiBr4 | TiI4 |
熔 点 | 1830℃ | 3550℃ | -24.1℃ | 38℃ | 150℃ |
沸点 | 2927℃ | 4827℃ | 136.4℃ | 233.1℃ | 377.2℃ |
晶型 | 离子晶体 | 分子晶体 | |||
表中金刚石的晶型为
(3)配位数为6,组成为TiCl3·6H2O 的晶体有两种:化学式为[TiCl( H2O)5]Cl2·H2O 的 X呈绿色,定量实验表明,X与AgNO3以1:2物质的量比反应生成沉淀。Y呈紫色,且Y 与AgNO3以1:3物质的量比反应生成沉淀,则Y的化学式为
(4)钙钛矿是重要的含钛矿物之一,其主要成分Z的晶胞如下图所示:

推测Z的化学式为
(5)若晶胞参数a=384.1pm,Z晶体的密度为
 )。
)。
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期。
(1)F原子基态的外围核外电子排布式为___________ ;
(2)由A、B、C形成的离子CAB﹣与AC2互为等电子体,则CAB﹣的结构式为___________ ;
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为___________ ;
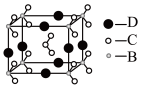
(4)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为___________ ;
(5)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2═CHCHO、HCOOH、CH3COONO2(PAN)等二次污染物。下列说法正确的是___________;
(6)NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4该配合物中心离子的配体为___________ ,其中提供空轨道的是___________ (填微粒符号)。
(1)F原子基态的外围核外电子排布式为
(2)由A、B、C形成的离子CAB﹣与AC2互为等电子体,则CAB﹣的结构式为
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为
(4)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为

(5)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2═CHCHO、HCOOH、CH3COONO2(PAN)等二次污染物。下列说法正确的是___________;
| A.N2O为直线型分子 |
| B.C、N、O的第一电离能依次增大 |
| C.CH2═CH一CHO分子中碳原子均采用sp2杂化 |
| D.相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子 |
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】金属材料在国民经济建设等领域具有重要应用,镁、镍、铬、铜是几种重要的金属元素,请回答下列问题:
(1)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是___ 。
(2)Ni与CO能形成配合物Ni(CO)4,该分子中σ键的个数为__ ,π键个数为____ ,与CO互为等电子体的分子是___ 。
(3)无水CrCl3和氨分子作用能形成某种配合物,该配合物的组成相当于CrCl3·6NH3。已知:若加入AgNO3溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入NaOH溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构简式___ 。
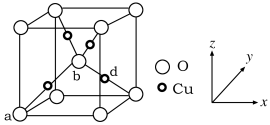
(4)铜与氧元素可形成如图所示的晶胞结构,其中Cu均匀地分散在立方体内部,该晶体的化学式为___ ,a、b的坐标参数依次为(0,0,0)、( ,
, ,
, ),则d的坐标参数为
),则d的坐标参数为___ ,已知该晶体的密度为ρg·cm-3,NA是阿伏加德罗常数值,则晶胞参数为___ cm(用含ρ的代数式表示)。
(1)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是
(2)Ni与CO能形成配合物Ni(CO)4,该分子中σ键的个数为
(3)无水CrCl3和氨分子作用能形成某种配合物,该配合物的组成相当于CrCl3·6NH3。已知:若加入AgNO3溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入NaOH溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构简式
(4)铜与氧元素可形成如图所示的晶胞结构,其中Cu均匀地分散在立方体内部,该晶体的化学式为
 ,
, ,
, ),则d的坐标参数为
),则d的坐标参数为
您最近半年使用:0次



