某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,发生_____ (填“氧化”或“还原”)反应,则该反应的还原剂是________ 。
(2)已知0.2molKBrO3在反应中得到1mol电子生成X,则X的化学式为____ 。
(3)根据上述反应可推知________ (填序号)。
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>HBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目。_____________
 +
+
(1)已知KBrO3在反应中得到电子,发生
(2)已知0.2molKBrO3在反应中得到1mol电子生成X,则X的化学式为
(3)根据上述反应可推知
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>HBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目。
 +
+
更新时间:2020-04-27 19:57:19
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】(一)经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:2NaNO2+ 4HI= 2NO + I2 + 2NaI + 2H2O
(1)在此反应中,氧化剂是________ (填化学式),氧化产物是___________ (填化学式)。
(2)若有1mol还原剂被氧化,则在此反应中发生转移的电子数目为_________ 。
(二)淡黄色粉末A跟无色液体B反应有无色气体C产生,金属D在C中燃烧可生成A,D跟B反应放出气体E,E和C又化合为B。从以上实验现象可判断:
(1)则A的化学式为________________ ;
(2)A与B反应的离子方程式为____________________ ;
(3)属于D在C中燃烧的现象的是(填序号)____________ 。
①A先熔化成闪亮的小球 ②剧烈燃烧 ③产生黄色火焰 ④生成淡黄色固体
(1)在此反应中,氧化剂是
(2)若有1mol还原剂被氧化,则在此反应中发生转移的电子数目为
(二)淡黄色粉末A跟无色液体B反应有无色气体C产生,金属D在C中燃烧可生成A,D跟B反应放出气体E,E和C又化合为B。从以上实验现象可判断:
(1)则A的化学式为
(2)A与B反应的离子方程式为
(3)属于D在C中燃烧的现象的是(填序号)
①A先熔化成闪亮的小球 ②剧烈燃烧 ③产生黄色火焰 ④生成淡黄色固体
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知MnO2与浓盐酸可发生如下反应:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①用双线桥法标明上述反应方程式中电子转移的方向和数目____ 。
②HCl在上述反应中显示出来的性质是___ 。
A.氧化性 B.还原性 C.酸性 D.碱性
③该反应的氧化产物是__ ,还原产物是__ 。
④若生成标准状况下3.36L氯气,则转移的电子个数为___ 。
⑤当有7.3gHCl被氧化时,被还原的物质的质量是___ g。
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O①用双线桥法标明上述反应方程式中电子转移的方向和数目
②HCl在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
③该反应的氧化产物是
④若生成标准状况下3.36L氯气,则转移的电子个数为
⑤当有7.3gHCl被氧化时,被还原的物质的质量是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题。
(一)现有甲、乙、丙三名同学分别进行硅酸胶体的制备实验。
已知:Ⅰ.硅酸钠(Na2SiO3)溶液呈碱性;Ⅱ.常温下硅酸(H2SiO3)的溶解度5×10-5g/100g水试回答下列问题:
(1)成功制备硅酸胶体的是___________ 同学,出现“光亮的通路”这种现象的名称是___________ 。
(2)形成硅酸胶体的离子方程式为___________ 。
(3)根据三位同学的实验操作可得,成功制备硅酸胶体的关键在于___________
(4)丙同学制备实验中溶液出现浑浊的原因是___________ 。
(5)制备的胶体中含有的主要杂质是___________ ,除去此杂质可采取的操作方法为___________ 。
(二)高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(6)该反应中氧化剂是___________ (用化学式表示,下同),___________ 元素被氧化,还原产物为___________ 。
(7)用单线桥在方程式中标出电子转移的情况:___________ 。
(一)现有甲、乙、丙三名同学分别进行硅酸胶体的制备实验。
| 分组 | 实验操作 | 实验现象 |
| 甲 | 将1%硅酸钠溶液滴入沸水中,冷却后用激光笔进行照射 | 无明显现象,未出现“光亮的通路” |
| 乙 | 向1%硅酸钠溶液中加入几滴酚酞溶液,缓慢滴入稀盐酸,溶液红色褪去后停止滴加,用激光笔进行照射 | 出现“光亮的通路” |
| 丙 | 向1%硅酸钠溶液中加入等体积的稀盐酸,用激光笔进行照射 | 未出现“光亮的通路”,溶液中出现浑浊 |
已知:Ⅰ.硅酸钠(Na2SiO3)溶液呈碱性;Ⅱ.常温下硅酸(H2SiO3)的溶解度5×10-5g/100g水试回答下列问题:
(1)成功制备硅酸胶体的是
(2)形成硅酸胶体的离子方程式为
(3)根据三位同学的实验操作可得,成功制备硅酸胶体的关键在于___________
| A.硅酸钠溶液的质量分数 | B.稀盐酸的加入量 |
| C.激光笔进行照射 | D.酚酞溶液加入 |
(5)制备的胶体中含有的主要杂质是
(二)高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(6)该反应中氧化剂是
(7)用单线桥在方程式中标出电子转移的情况:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】电子工业常用30%的FeCl3溶液腐蚀覆在绝缘板上的铜箔,制造印刷电路板。其反应为2FeCl3+Cu=2FeCl2+CuCl2
(1)上述反应中还原剂:___________ ;氧化产物:___________ ;被还原的元素:___________ ;
(2)FeCl3溶液与金属铜发生反应的离子方程式为___________ 。
(3)用双线桥法表示上述反应中电子转移的方向和数目:___________ (双线桥直接画在下方方程式上)
2FeCl3+Cu=2FeCl2+CuCl2
(1)上述反应中还原剂:
(2)FeCl3溶液与金属铜发生反应的离子方程式为
(3)用双线桥法表示上述反应中电子转移的方向和数目:
2FeCl3+Cu=2FeCl2+CuCl2
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.氯酸钾和浓盐酸之间有下列反应:2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2↑+2H2O.
(1)该反应中发生还原反应的物质是________ 。氧化产物是________ 。
(2)用双线桥标出方程式中的电子得失2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2↑+2H2O________
(3)当有0.2 mol电子发生转移时,生成的氯气的体积为________ L (标准状况)。被氧化的HCl的物质的量为________ mol.
(4)若分别用①KMnO4(还原产物是Mn2+)②MnO2(还原产物是Mn2+) ③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是________ 。
Ⅱ.已知反应:Cu+HNO3(稀)——Cu(NO3)2+NO↑+H2O;
(1)配平并用“双线桥法”表示上述反应中电子转移的方向和数目:___Cu+___HNO3(稀) = ___Cu(NO3)2+___NO↑+___H2O。___________
(2)该反应中氧化剂与还原剂的物质的量之比为_______ ;写出该反应的离子方程式______________________________________
(1)该反应中发生还原反应的物质是
(2)用双线桥标出方程式中的电子得失2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2↑+2H2O
(3)当有0.2 mol电子发生转移时,生成的氯气的体积为
(4)若分别用①KMnO4(还原产物是Mn2+)②MnO2(还原产物是Mn2+) ③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是
Ⅱ.已知反应:Cu+HNO3(稀)——Cu(NO3)2+NO↑+H2O;
(1)配平并用“双线桥法”表示上述反应中电子转移的方向和数目:___Cu+___HNO3(稀) = ___Cu(NO3)2+___NO↑+___H2O。
(2)该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】过氧化氢(H2O2,俗名为双氧水)、过氧化银(Ag2O2)广泛应用于抗菌消毒和化学能源等领域。


(1)根据下列三个反应回答问题:
反应Ⅰ.Ag2O+H2O2=2Ag+O2↑+H2O
反应Ⅱ.2H2O2=2H2O+O2↑
反应Ⅲ.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
①从氧化还原反应角度分析,反应Ⅰ中H2O2表现的性质为_____ 。
②上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序为_____ 。
③某强酸反应体系中发生一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、Mn 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:_____ 。
(2)过氧化银(Ag2O2)为活性物质,可用作新型电池材料。用NaClO-NaOH溶液氧化AgNO3,能制得高纯度的纳米级Ag2O2.
①NaClO中Cl的化合价为_____ ,Ag2O2中O的化合价为_____ 。
②写出上述反应的化学方程式:_____ 。


(1)根据下列三个反应回答问题:
反应Ⅰ.Ag2O+H2O2=2Ag+O2↑+H2O
反应Ⅱ.2H2O2=2H2O+O2↑
反应Ⅲ.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
①从氧化还原反应角度分析,反应Ⅰ中H2O2表现的性质为
②上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序为
③某强酸反应体系中发生一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、Mn
 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2.写出该反应的离子方程式:(2)过氧化银(Ag2O2)为活性物质,可用作新型电池材料。用NaClO-NaOH溶液氧化AgNO3,能制得高纯度的纳米级Ag2O2.
①NaClO中Cl的化合价为
②写出上述反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】二氧化硒 (SeO2)是一种氧化剂,单质硒可能成为环境污染物,完成下列问题。
(1)Se和浓 反应的产物为
反应的产物为 和
和 ,其中氧化剂是
,其中氧化剂是_______ ,还原剂是_______ 。化学反应方程式为_______ 。
(2)已知:
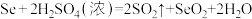 ;
;

则 、
、 (浓)、
(浓)、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是_______ 。
(3)回收得到的 的含量,可以通过下列反应测定。用“双线桥法”标出该反应中电子转移的方向和数目。
的含量,可以通过下列反应测定。用“双线桥法”标出该反应中电子转移的方向和数目。_______
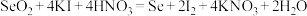
(1)Se和浓
 反应的产物为
反应的产物为 和
和 ,其中氧化剂是
,其中氧化剂是(2)已知:
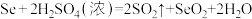 ;
;
则
 、
、 (浓)、
(浓)、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是(3)回收得到的
 的含量,可以通过下列反应测定。用“双线桥法”标出该反应中电子转移的方向和数目。
的含量,可以通过下列反应测定。用“双线桥法”标出该反应中电子转移的方向和数目。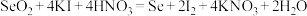
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】硒元素具有抗衰老、抑制癌细胞的功能,其化学性质与硫相似。硒的元素符号为Se,相对原子质量为79,对应的某种含氧酸的化学式为H2SeO3。
(1)这种酸应读作_______________ ;
(2)若将二氧化硫通入H2SeO3的溶液中,会有Se析出,写出该反应的化学方程式:
________________________________________ ;
(3)又已知2HCl + H2SeO4 ="=" H2SeO3 + Cl2+ H2O,则H2SeO4、H2SeO3、H2SO3的氧化性由强到弱的顺序是________________________ 。
(1)这种酸应读作
(2)若将二氧化硫通入H2SeO3的溶液中,会有Se析出,写出该反应的化学方程式:
(3)又已知2HCl + H2SeO4 ="=" H2SeO3 + Cl2+ H2O,则H2SeO4、H2SeO3、H2SO3的氧化性由强到弱的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】某品牌的“84消毒液”的部分标签如下图。回答下列问题:

(1)工业上制备该“84消毒液”的基本反应原理是氯气与烧碱的反应,写出该反应的离子方程式:___________ 。
(2)该“84消毒液”的功能有___________ (填标号)。
a.环境消毒 b.器物杀菌 c.织物漂白 d.发酵食物
(3)测定溶液中NaClO含量的方法有:在淀粉KI酸性溶液中加入次氯酸钠溶液,再用一定浓度的 标准溶液滴定,涉及的反应如下:
标准溶液滴定,涉及的反应如下:
i.
ii.
①配平反应i:___________ 。该反应说明NaClO具有___________ 性(填“氧化”“还原”或“漂白”)。
②反应ii中I-是___________ (填“氧化产物”或“还原产物”)。
(4)向该“84消毒液”中滴入少量醋酸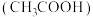 可增强漂白效果,请用化学方程式解释其原因
可增强漂白效果,请用化学方程式解释其原因___________ 。

(1)工业上制备该“84消毒液”的基本反应原理是氯气与烧碱的反应,写出该反应的离子方程式:
(2)该“84消毒液”的功能有
a.环境消毒 b.器物杀菌 c.织物漂白 d.发酵食物
(3)测定溶液中NaClO含量的方法有:在淀粉KI酸性溶液中加入次氯酸钠溶液,再用一定浓度的
 标准溶液滴定,涉及的反应如下:
标准溶液滴定,涉及的反应如下:i.

ii.

①配平反应i:
②反应ii中I-是
(4)向该“84消毒液”中滴入少量醋酸
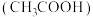 可增强漂白效果,请用化学方程式解释其原因
可增强漂白效果,请用化学方程式解释其原因
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】常温下,二氧化氯(ClO2)为黄绿色气体,具有强氧化性而能用于自来水的消毒。与Cl2相比,ClO2不会产生对人体有潜在危害的有机氯代物,已被联合国世界卫生组织(WHO列为AI级高效安全消毒剂
(1)制备C1O2常用以下几种方法:
方法一:2NaClO3+4HCl=2ClO2↑+C12↑+2NaCl+2H2O
方法二:3NaClO3+3H2SO4(浓)=HClO4+2C1O2↑+3NaHSO4+H2O
①方法一中,HCl的作用是___________ 。
②方法二中,氧化剂和还原剂物质的量之比为___________ 。
(2)工业上常用电解饱和食盐水的方法制备氯气,其反应的化学方程式为2NaCl+2H2O 2NaOH+Cl2↑+H2↑请用单线桥法表示该反应电子转移的方向和数目
2NaOH+Cl2↑+H2↑请用单线桥法表示该反应电子转移的方向和数目________ 。
(3)ClO2尾气用NaOH溶液吸收,生成物质的量之比为1:1的两种盐,一种为NaClO2,另一种为___________ (填序号)
A.NaClO B.NaClO3 C.NaClO4 D.NaCl
(4)ClO2与NaOH反应生成的NaClO2是一种强氧化剂,它容易变质分解为NaClO3和NaCl。等质量的 NaClO2试样,在变质前后,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量______ 。(填“相同”“不同”或“无法判断”)
(5)C1O2可迅速氧化硫化物(自身转化为Cl-)以除去水中硫化物产生的臭味,,取适量ClO2通入到含有H2S的水中,再向其中加入少量的BaCl2溶液,有白色沉淀生成,写出ClO2与H2S水溶液反应的离子方程式___________ 。
(1)制备C1O2常用以下几种方法:
方法一:2NaClO3+4HCl=2ClO2↑+C12↑+2NaCl+2H2O
方法二:3NaClO3+3H2SO4(浓)=HClO4+2C1O2↑+3NaHSO4+H2O
①方法一中,HCl的作用是
②方法二中,氧化剂和还原剂物质的量之比为
(2)工业上常用电解饱和食盐水的方法制备氯气,其反应的化学方程式为2NaCl+2H2O
 2NaOH+Cl2↑+H2↑请用单线桥法表示该反应电子转移的方向和数目
2NaOH+Cl2↑+H2↑请用单线桥法表示该反应电子转移的方向和数目(3)ClO2尾气用NaOH溶液吸收,生成物质的量之比为1:1的两种盐,一种为NaClO2,另一种为
A.NaClO B.NaClO3 C.NaClO4 D.NaCl
(4)ClO2与NaOH反应生成的NaClO2是一种强氧化剂,它容易变质分解为NaClO3和NaCl。等质量的 NaClO2试样,在变质前后,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量
(5)C1O2可迅速氧化硫化物(自身转化为Cl-)以除去水中硫化物产生的臭味,,取适量ClO2通入到含有H2S的水中,再向其中加入少量的BaCl2溶液,有白色沉淀生成,写出ClO2与H2S水溶液反应的离子方程式
您最近一年使用:0次

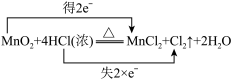
 固体,加入足量
固体,加入足量 溶液,使
溶液,使 全部转化成
全部转化成 ,并放出NO气体。
,并放出NO气体。
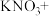
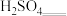

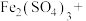

 。
。

