(一)经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:2NaNO2+ 4HI= 2NO + I2 + 2NaI + 2H2O
(1)在此反应中,氧化剂是________ (填化学式),氧化产物是___________ (填化学式)。
(2)若有1mol还原剂被氧化,则在此反应中发生转移的电子数目为_________ 。
(二)淡黄色粉末A跟无色液体B反应有无色气体C产生,金属D在C中燃烧可生成A,D跟B反应放出气体E,E和C又化合为B。从以上实验现象可判断:
(1)则A的化学式为________________ ;
(2)A与B反应的离子方程式为____________________ ;
(3)属于D在C中燃烧的现象的是(填序号)____________ 。
①A先熔化成闪亮的小球 ②剧烈燃烧 ③产生黄色火焰 ④生成淡黄色固体
(1)在此反应中,氧化剂是
(2)若有1mol还原剂被氧化,则在此反应中发生转移的电子数目为
(二)淡黄色粉末A跟无色液体B反应有无色气体C产生,金属D在C中燃烧可生成A,D跟B反应放出气体E,E和C又化合为B。从以上实验现象可判断:
(1)则A的化学式为
(2)A与B反应的离子方程式为
(3)属于D在C中燃烧的现象的是(填序号)
①A先熔化成闪亮的小球 ②剧烈燃烧 ③产生黄色火焰 ④生成淡黄色固体
更新时间:2020-11-06 13:38:52
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】“分类”的思想在化学学习及化学学科发展中起着重要作用。现有下列物质:
① 固体②熔融
固体②熔融 ③淀粉溶液④液态氯化氢⑤NaCl溶液⑥
③淀粉溶液④液态氯化氢⑤NaCl溶液⑥ ⑦金属铜⑧
⑦金属铜⑧ ⑨酒精⑩
⑨酒精⑩
回答下列问题:
(1)以上物质中属于电解质的是_____ (填序号,下同),属于非电解质的是_____ 。
(2)②熔融 能导电,其电离方程式为
能导电,其电离方程式为_____ 。
(3)③淀粉溶液所属分散系为_____ ,⑤NaCl溶液所属分散系为_____ ,二者如果混合,可采用_____ 方法分离。
(4)⑧ 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为_____ ,该反应中 是
是_____ (“氧化剂”“还原剂”或“既是氧化剂又是还原剂”),每当有1mol 参与反应,转移电子数为
参与反应,转移电子数为_____ (设 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。
(5)已知⑨ (次磷酸)与足量KOH溶液反应的化学方程式为
(次磷酸)与足量KOH溶液反应的化学方程式为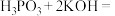
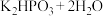 ,
, 属于
属于_____ (填“正盐”或“酸式盐”)。
①
 固体②熔融
固体②熔融 ③淀粉溶液④液态氯化氢⑤NaCl溶液⑥
③淀粉溶液④液态氯化氢⑤NaCl溶液⑥ ⑦金属铜⑧
⑦金属铜⑧ ⑨酒精⑩
⑨酒精⑩
回答下列问题:
(1)以上物质中属于电解质的是
(2)②熔融
 能导电,其电离方程式为
能导电,其电离方程式为(3)③淀粉溶液所属分散系为
(4)⑧
 与水的反应属于氧化还原反应,化学方程式为
与水的反应属于氧化还原反应,化学方程式为 是
是 参与反应,转移电子数为
参与反应,转移电子数为 为阿伏伽德罗常数的值)。
为阿伏伽德罗常数的值)。(5)已知⑨
 (次磷酸)与足量KOH溶液反应的化学方程式为
(次磷酸)与足量KOH溶液反应的化学方程式为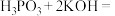
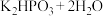 ,
, 属于
属于
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】铁及其化合物在生产生活中有极其重要的用途,请回答下列问题:
(1)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是__________ 。
A. Fe B. C.
C. 
(2)取少量 粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为
粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为__________ ,反应后得到的溶液记为A。
(3)取少量A置于试管中,滴入几滴NaOH溶液,可观察到红褐色沉淀(记为B)生成,反应的离子方程式为__________ 。
(4)在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中滴入__________ (填饱和“A”或“B”),继续煮沸至溶液呈__________ 色,停止加热,即制得 胶体(记为C)。
胶体(记为C)。
(5)另取一只小烧杯也加入25mL蒸馏水,接着向烧杯中加入少量 溶液,振荡均匀后的液体记为D,将C与D一起放置于暗处,分别用激光笔照射,出现
溶液,振荡均匀后的液体记为D,将C与D一起放置于暗处,分别用激光笔照射,出现__________ (填“相同”或“不相同”)的现象,其中C中可以看到__________ (填现象)。
(6)人体血红蛋白分子中含有 ,正是这些
,正是这些 使血红蛋白分子具有载氧功能。亚硝酸钠(
使血红蛋白分子具有载氧功能。亚硝酸钠( )可将人体血红蛋白中的
)可将人体血红蛋白中的 转化为
转化为 ,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中
,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中 发生
发生__________ 反应,说明亚硝酸钠具有__________ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有__________ 性。
(1)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是
A. Fe B.
 C.
C. 
(2)取少量
 粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为
粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为(3)取少量A置于试管中,滴入几滴NaOH溶液,可观察到红褐色沉淀(记为B)生成,反应的离子方程式为
(4)在小烧杯中加入25mL蒸馏水,加热至沸腾后,向沸水中滴入
 胶体(记为C)。
胶体(记为C)。(5)另取一只小烧杯也加入25mL蒸馏水,接着向烧杯中加入少量
 溶液,振荡均匀后的液体记为D,将C与D一起放置于暗处,分别用激光笔照射,出现
溶液,振荡均匀后的液体记为D,将C与D一起放置于暗处,分别用激光笔照射,出现(6)人体血红蛋白分子中含有
 ,正是这些
,正是这些 使血红蛋白分子具有载氧功能。亚硝酸钠(
使血红蛋白分子具有载氧功能。亚硝酸钠( )可将人体血红蛋白中的
)可将人体血红蛋白中的 转化为
转化为 ,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中
,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中 发生
发生
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】K2FeO4是常见的水处理剂,其原理如图所示。请回答下列问题:

(1)高铁酸钾(K2FeO4)中铁元素的化合价为___________ 。
(2)过程a中K2FeO4体现___________ (填“氧化”或“还原”)性,氧化产物是___________ ,反应过程中转移5.418×1022电子,需要___________ molK2FeO4。
(3)过程b反应的离子方程式为___________ ,过程c属于___________ (填“物理”或“化学”)变化。
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:_______ 。
___Fe(OH)3+___KOH+___KClO=___K2FeO4+___KCl+___H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是___________ 。

(1)高铁酸钾(K2FeO4)中铁元素的化合价为
(2)过程a中K2FeO4体现
(3)过程b反应的离子方程式为
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
___Fe(OH)3+___KOH+___KClO=___K2FeO4+___KCl+___H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】钠、氯及其化合物在生产和生活中有广泛的应用。金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制的工业方法,其反应原理:2NaCl(熔融) 2Na+Cl2↑。根据所学知识完成下列各题。
2Na+Cl2↑。根据所学知识完成下列各题。
(1)下列各项中属于保存金属钠的正确方法是___________。
(2)将金属钠放入CuSO4溶液中会产生蓝色沉淀,请用化学方程式解释这一现象___________ 。
(3)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,其现象为___________ 。请写出发生反应的化学方程式:___________ 。
(4)钠的一种氧化物常用于呼吸面具和潜水艇氧气的来源,用化学反应方程式表示其原理:___________ 。
 2Na+Cl2↑。根据所学知识完成下列各题。
2Na+Cl2↑。根据所学知识完成下列各题。(1)下列各项中属于保存金属钠的正确方法是___________。
| A.石蜡封存 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |
(3)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,其现象为
(4)钠的一种氧化物常用于呼吸面具和潜水艇氧气的来源,用化学反应方程式表示其原理:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在实验室里,某同学取一小块金属钠做钠与水反应的实验。试完成下列问题:
(1)切开的金属钠暴露在空气中,最先观察到的现象是_______ ,所发生反应的化学方程式是_______ 。
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是_______ 、_______ 。
(3)钠与水反应的离子方程式为_______ 。
(4)过氧化钠与水反应的化学方程式为_______ 。
(1)切开的金属钠暴露在空气中,最先观察到的现象是
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是
(3)钠与水反应的离子方程式为
(4)过氧化钠与水反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)有一种金属单质A,焰色反应颜色呈黄色,能发生下图所示变化:

上图中淡黄色固体B是_____________ 填化学式)
(2)钠的化合物中,可用于呼吸面具作为O2来源的是______
(3)写出(1)中C溶液与硝酸反应的化学方程式:______

上图中淡黄色固体B是
(2)钠的化合物中,可用于呼吸面具作为O2来源的是
(3)写出(1)中C溶液与硝酸反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】已知过氧化氢具有漂白性。某同学研究过氧化钠跟水的反应,进行如下实验:向盛有少量过氧化钠固体的试管中滴加水,直到气体不再放出,加水稀释,将所得溶液平均盛放在两支试管中。一支试管中滴加酚酞试液,溶液变红,半分钟内红色褪去;另一支试管中加入少量二氧化锰,又有气体放出,待气体不再放出后,再滴加酚酞,溶液变红,持久不褪色。请写出:
(1)过氧化钠跟水反应可能的化学方程式:
①___________ ;
②___________ ;
(2)加入二氧化锰后发生反应的化学方程式为___________ ,反应中二氧化锰的作用是___________ 。
(1)过氧化钠跟水反应可能的化学方程式:
①
②
(2)加入二氧化锰后发生反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表是元素周期表的一部分,所示为1-18号元素。
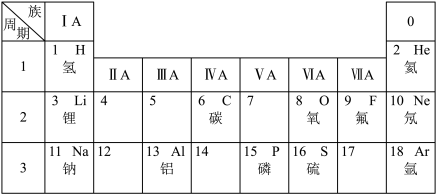
(1)请写出7号元素的名称 和元素符号 _______ ;请写出17号元素的名称 和元素符号 _______ 。
(2)请画出14号元素的原子结构示意图_______ 。
(3)11号钠元素是高中化学的核心元素之一,某课外实验小组从煤油中取出一块钠,用滤纸吸干其表面的煤油,用刀切开,发现钠块切面处迅速变暗,反应的化学方程式为_______ 。已知钠的一种化合物为淡黄色粉末,可用作供氧剂。请写出此化合物与水反应的离子方程式_______ 。
(4)探究钾元素(原子序数为19)的单质与水反应的生成物。甲同学猜想生成物为KOH和H2;乙同学猜想生成物为KOH和O2,你认为_______ 同学的猜想不合理,请从化合价的角度解释原因 _______ 。

(1)请写出7号元素的
(2)请画出14号元素的原子结构示意图
(3)11号钠元素是高中化学的核心元素之一,某课外实验小组从煤油中取出一块钠,用滤纸吸干其表面的煤油,用刀切开,发现钠块切面处迅速变暗,反应的化学方程式为
(4)探究钾元素(原子序数为19)的单质与水反应的生成物。甲同学猜想生成物为KOH和H2;乙同学猜想生成物为KOH和O2,你认为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】I.A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
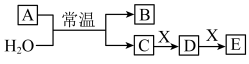
若A的焰色反应为黄色,且A为化合物,回答下列问题:
(1)A与 反应的离子方程式为
反应的离子方程式为___________ 。
(2)若X为具有强还原性的非金属单质,通常为黑色粉末,写出E的化学式___________ 。
(3)若X为一种造成温室效应的气体,则鉴别等浓度的D、E两种溶液,可选择的试剂为_______(填代号)。
II.元素的价类二维图是学习元素及其化合物相关知识的重要模型和工具,如图为铁元素的价类二维图。

(4)图中①处填___________ ,②处填___________ 。
(5)下列说法正确的是___________。
(6) 中铁元素的检验
中铁元素的检验___________ 。

若A的焰色反应为黄色,且A为化合物,回答下列问题:
(1)A与
 反应的离子方程式为
反应的离子方程式为(2)若X为具有强还原性的非金属单质,通常为黑色粉末,写出E的化学式
(3)若X为一种造成温室效应的气体,则鉴别等浓度的D、E两种溶液,可选择的试剂为_______(填代号)。
| A.NaCl溶液 | B. 溶液 溶液 | C.NaOH溶液 | D. 溶液 溶液 |
II.元素的价类二维图是学习元素及其化合物相关知识的重要模型和工具,如图为铁元素的价类二维图。

(4)图中①处填
(5)下列说法正确的是___________。
A.铁与高温水蒸气的反应可转化为 |
B.FeO是一种黑色粉末,在空气中受热可实现转化 |
C.加足量氯水可实现 转化为 转化为 |
D. 、 、 都可由化合反应制备 都可由化合反应制备 |
(6)
 中铁元素的检验
中铁元素的检验
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
(1)火药是中国的“四大发明”之一,永远值得炎黄孙骄傲。 黑火药在发生爆炸时, 发生如下反应:2KNO3+ 3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是_________ ( 填元素名称)。还原产物是________ (填化学式)。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的试纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显_____________ 价。
②以上反应中的氧化剂为______________ ,当有1 molCuI参与反应时,转移电子_______ mol
③用双线桥法标明上述反应电子转移的方向和数目:________ 。
(1)火药是中国的“四大发明”之一,永远值得炎黄孙骄傲。 黑火药在发生爆炸时, 发生如下反应:2KNO3+ 3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的试纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显
②以上反应中的氧化剂为
③用双线桥法标明上述反应电子转移的方向和数目:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化工厂用浓氨水检验氯气管道是否漏气,利用的反应如下: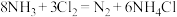
(1)作还原剂的物质是_________ ,氯元素的化合价_________ (填“升高”或“降低”)。
(2)若反应中每生成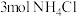 ,则消耗
,则消耗 的物质的量至少为
的物质的量至少为_________  ,转移电子的物质的量为
,转移电子的物质的量为_________  。
。
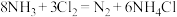
(1)作还原剂的物质是
(2)若反应中每生成
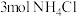 ,则消耗
,则消耗 的物质的量至少为
的物质的量至少为 ,转移电子的物质的量为
,转移电子的物质的量为 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】硫代硫酸钠,又名次亚硫酸钠、大苏打、海波,化学式为 ,是硫酸钠中一个氧原子被硫原子取代的产物,因此两个疏原子的氧化数分别为-2和+6。硫代硫酸钠易溶于水,难溶于乙醇,在中性或碱性溶液中稳定,广泛应用于日常生产生活中。
,是硫酸钠中一个氧原子被硫原子取代的产物,因此两个疏原子的氧化数分别为-2和+6。硫代硫酸钠易溶于水,难溶于乙醇,在中性或碱性溶液中稳定,广泛应用于日常生产生活中。
(1) 离子结构如图所示,其中心硫原子的杂化方式为
离子结构如图所示,其中心硫原子的杂化方式为_______________ 。基态S原子中,核外电子占据的最高能级的符号是___________ ,占据最高能级电子的电子云轮廓图为___________ 形。

(2)关于反应 ,下列说法正确的是
,下列说法正确的是
 ,是硫酸钠中一个氧原子被硫原子取代的产物,因此两个疏原子的氧化数分别为-2和+6。硫代硫酸钠易溶于水,难溶于乙醇,在中性或碱性溶液中稳定,广泛应用于日常生产生活中。
,是硫酸钠中一个氧原子被硫原子取代的产物,因此两个疏原子的氧化数分别为-2和+6。硫代硫酸钠易溶于水,难溶于乙醇,在中性或碱性溶液中稳定,广泛应用于日常生产生活中。(1)
 离子结构如图所示,其中心硫原子的杂化方式为
离子结构如图所示,其中心硫原子的杂化方式为
(2)关于反应
 ,下列说法正确的是
,下列说法正确的是 A. 发生还原反应 发生还原反应 | B. 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
| C.氧化产物与还原产物的物质的盘之比为2∶1 | D.1mol  发生反应,转移2mol电子 发生反应,转移2mol电子 |
您最近一年使用:0次



