某化学科研小组研究在其他条件不变时,改变某一条件对某类反应[aA(g)+bB(g)⇌cC(g)]的化学平衡的影响,得到图像(图中p表示压强,T表示温度,n表示物质的量,α表示转化率)
反应Ⅰ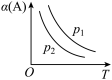 反应Ⅱ
反应Ⅱ
分析图像象,回答下列问题:
(1)在反应I中,若 >
> ,则该反应的正反应为
,则该反应的正反应为__________ (填“放热”或“吸热”)反应,且为气体分子数__________ (填“减小”或“增大”)的反应;若此反应能自发进行,则必须满足的条件是__________
(2)在反应Ⅱ中,
__________ (填“>”,“<”或“=”) ,该反应的正反应为
,该反应的正反应为__________ (填“放热”或“吸热”)反应。
反应Ⅰ
 反应Ⅱ
反应Ⅱ
分析图像象,回答下列问题:
(1)在反应I中,若
 >
> ,则该反应的正反应为
,则该反应的正反应为(2)在反应Ⅱ中,

 ,该反应的正反应为
,该反应的正反应为
更新时间:2020-05-01 23:23:17
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】完成下列问题。
(1)如图表示在密闭容器中反应:2SO2(g)+O2(g) 2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是
2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是___________ ;bc过程中改变的条件可能是___________ ;若增大压强时,反应速度变化情况画在c~d处___________ 。
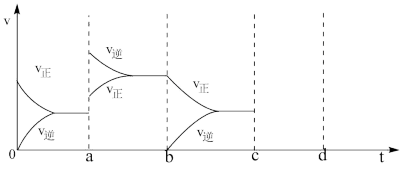
(2)在一定温度下,10L密闭容器中加入5molSO2、4.5molO2,经10min后反应达平衡时有3molSO2发生了反应。试填写下列空格:
①SO2的转化率为___________ 。
②用SO2表示该反应的平均反应速率为___________ 。
③平衡时体系中SO3的百分含量(体积分数)为___________ 。
④平衡常数K为___________ 。
(1)如图表示在密闭容器中反应:2SO2(g)+O2(g)
 2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是
2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是
(2)在一定温度下,10L密闭容器中加入5molSO2、4.5molO2,经10min后反应达平衡时有3molSO2发生了反应。试填写下列空格:
①SO2的转化率为
②用SO2表示该反应的平均反应速率为
③平衡时体系中SO3的百分含量(体积分数)为
④平衡常数K为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】可逆反应:aA(g)+ bB(g) cC(g)+ dD(g);根据图回答:
cC(g)+ dD(g);根据图回答:
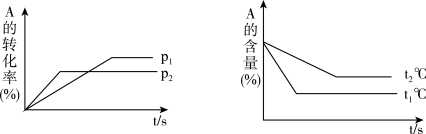
(1)压强p1_________ p2(填“>”或“<”);
(2)a +b__________ c +d(填“>”或“<”);
(3)温度t1℃_________ t2℃(填“>”或“<”);
(4)正反应为_________ 反应。(填吸热或放热)
 cC(g)+ dD(g);根据图回答:
cC(g)+ dD(g);根据图回答:
(1)压强p1
(2)a +b
(3)温度t1℃
(4)正反应为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】一定条件下2L的密闭容器中,反应aA(g)+bB(g) cC(g)+dD(g)达到平衡。
cC(g)+dD(g)达到平衡。
(1)若起始时A为lmol,反应2min达到平衡,A剩余0.4mol,则在0~2min内A的平均反应速率为________ mol/(L·min)
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,则a+b_____ c+d(选填“>”、“<”或“=”),v逆_____ (选填“增大”、“减小”或“不变”)
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是______ 。(选填编号)
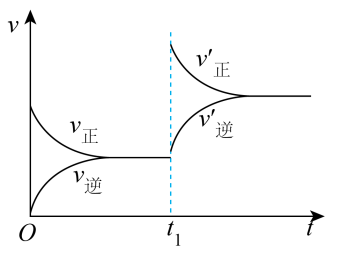
a.增大A的浓度
b.缩小容器体积
c.加入催化剂
d.升高温度
 cC(g)+dD(g)达到平衡。
cC(g)+dD(g)达到平衡。(1)若起始时A为lmol,反应2min达到平衡,A剩余0.4mol,则在0~2min内A的平均反应速率为
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,则a+b
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是

a.增大A的浓度
b.缩小容器体积
c.加入催化剂
d.升高温度
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】2023年杭州亚运会开幕式首次使用“零碳甲醇”作为主火炬塔燃料。NiO-In2O3可催化CO2的氢化,体系中产生CH3OH和CO。现将一定比例的CO2、H2以一定流速通过催化剂,某温度下,得到CO2的转化率、CH3OH或CO的选择性[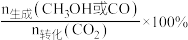 ]与催化剂中NiO质量分数的关系图:
]与催化剂中NiO质量分数的关系图:

(1)曲线_______ (填“X”或“Y”)表示CO2的转化率随催化剂中NiO的质量分数的变化。
(2)有利于提高CH3OH选择性的反应条件是_______ (填标号)。
A.减小压强 B.使用更合适的催化剂 C.原料气中掺入适量的CO
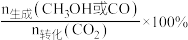 ]与催化剂中NiO质量分数的关系图:
]与催化剂中NiO质量分数的关系图:
(1)曲线
(2)有利于提高CH3OH选择性的反应条件是
A.减小压强 B.使用更合适的催化剂 C.原料气中掺入适量的CO
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】中国首次实现了利用二氧化碳人工合成淀粉,为全球的“碳达峰”、“碳中和”起到重大的支撑作用。其中最关键的一步是以 为原料制
为原料制 。在某
。在某 催化加氢制
催化加氢制 的反应体系中,发生的主要反应有:
的反应体系中,发生的主要反应有:
Ⅰ.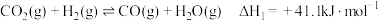
Ⅱ.

Ⅲ.
(1)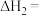
___________  。
。
(2) 时,往某密闭容器中按投料比
时,往某密闭容器中按投料比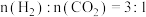 充入
充入 和
和 。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
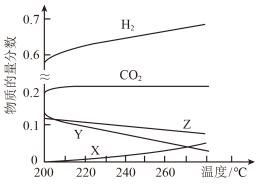
图中Y代表___________ (填化学式)。
(3)我国科研人员研究出在 催化剂上
催化剂上 氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为
氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为___________ 。分析在反应气中加入少量的水能够提升甲醇产率的可能原因是___________ 。

(4)恒压下, 和
和 以物质的量之比
以物质的量之比 投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。
。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。___________

 为原料制
为原料制 。在某
。在某 催化加氢制
催化加氢制 的反应体系中,发生的主要反应有:
的反应体系中,发生的主要反应有:Ⅰ.
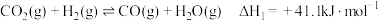
Ⅱ.


Ⅲ.

(1)
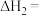
 。
。(2)
 时,往某密闭容器中按投料比
时,往某密闭容器中按投料比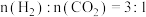 充入
充入 和
和 。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如下图所示。
图中Y代表
(3)我国科研人员研究出在
 催化剂上
催化剂上 氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为
氢化合成甲醇的反应历程如下图所示。反应②的化学方程式为
(4)恒压下,
 和
和 以物质的量之比
以物质的量之比 投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
投料合成甲醇(不考虑副反应),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。
。请在下图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】甲醇是一种重要的化工原料又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
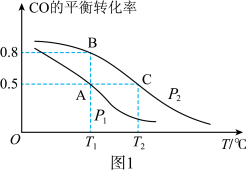
由图可判断△H____ 0,A、B两点对应的平衡常数关系是KA____ KB(填“>、<、=”)。
(2)某温度下,充分反应后,达到平衡时测得c(CO)=0.02mol/L,则此温度下的平衡常数K=____ 。
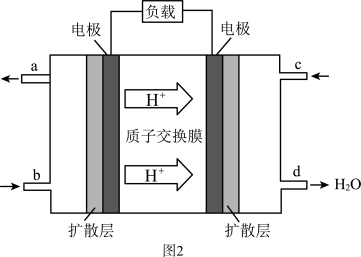
(3)我国在甲醇燃料电池技术方面获得新突破,组装出自呼吸电池及主动式电池。其工作原理如图2所示。该电池工作时,c口通入的物质为___  (填化学式)
(填化学式) ;电池负极的电极反应式为
;电池负极的电极反应式为____ 。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
由图可判断△H
(2)某温度下,充分反应后,达到平衡时测得c(CO)=0.02mol/L,则此温度下的平衡常数K=
(3)我国在甲醇燃料电池技术方面获得新突破,组装出自呼吸电池及主动式电池。其工作原理如图2所示。该电池工作时,c口通入的物质为
 (填化学式)
(填化学式) ;电池负极的电极反应式为
;电池负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
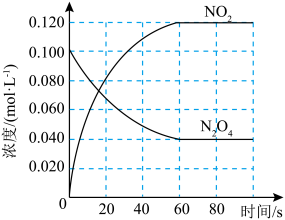
(1)该反应ΔH___________ 0(填“>”、“<”或“=”),在0~60 s时段,反应速率v(N2O4)为___________ mol·L-1·s-1。平衡常数K=___________ (请书写单位)。
(2)在温度不变的情况下向平衡体系中再充入N2O4 0.01mol·L-1和NO20.03mol·L-1此时v(正)___________ v(逆)(填“>”、“<”或“=”)。
(3)下列有利于提高反应N2O4(g) 2NO2(g)平衡转化率的条件是___________(填标号)。
2NO2(g)平衡转化率的条件是___________(填标号)。
 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
(1)该反应ΔH
(2)在温度不变的情况下向平衡体系中再充入N2O4 0.01mol·L-1和NO20.03mol·L-1此时v(正)
(3)下列有利于提高反应N2O4(g)
 2NO2(g)平衡转化率的条件是___________(填标号)。
2NO2(g)平衡转化率的条件是___________(填标号)。| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在容积为2L的恒容密闭容器中,加入1molA(g)、2molB(g)发生如下反应:A(g)+2B(g) C(g)+D(g)。在不同温度下,D的物质的量n(D)和时间t的关系如下图所示。
C(g)+D(g)。在不同温度下,D的物质的量n(D)和时间t的关系如下图所示。

试回答下列问题:
(1)温度为T1℃时,0~5min内,以B表示的平均反应速率为________ 。
(2)T1℃________ (填“<”或“>”)T2℃,该反应的正反应是________ (填“放热”或“吸热”)反应。
(3)T1℃时,向上述平衡体系中再充入1molA、2molB,达到平衡时,D的物质的量n(D)________ (填“>”、“<”或“=”)1.2mol。
 C(g)+D(g)。在不同温度下,D的物质的量n(D)和时间t的关系如下图所示。
C(g)+D(g)。在不同温度下,D的物质的量n(D)和时间t的关系如下图所示。
试回答下列问题:
(1)温度为T1℃时,0~5min内,以B表示的平均反应速率为
(2)T1℃
(3)T1℃时,向上述平衡体系中再充入1molA、2molB,达到平衡时,D的物质的量n(D)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】如图所示,一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g) + 2H2(g) ⇌CH3OH(g)
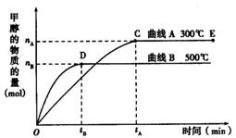
①上述可逆反应正反应为_______ 反应(填“放热”或“吸热”)。
②在500℃,从反应开始到平衡,氢气的平均反应速率v(H2) =_______ (用nB、tB表示)。
③对处于E点的体系,改变外界条件使平衡向正反应方向移动时,下列有关该体系的说法正确的是_______ (填字母)。
A.H2的转化率一定增大 B.v正一定增大,v逆一定减小
C.CH3OH的质量分数一定增加 D.v逆一定小于v正

①上述可逆反应正反应为
②在500℃,从反应开始到平衡,氢气的平均反应速率v(H2) =
③对处于E点的体系,改变外界条件使平衡向正反应方向移动时,下列有关该体系的说法正确的是
A.H2的转化率一定增大 B.v正一定增大,v逆一定减小
C.CH3OH的质量分数一定增加 D.v逆一定小于v正
您最近一年使用:0次



