在2L密闭容器中充入气体A和B,发生A(g)+B(g)⇌C(g)+2D(g) ΔH,所得实验数据如表。下列说法不正确的是
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(A) | n(B) | n(C) | ||
| ① | 300 | 0.40 | 0.10 | 0.090 |
| ② | 500 | 0.40 | 0.10 | 0.080 |
| ③ | 500 | 0.20 | 0.05 | a |
| A.ΔH>0 |
| B.500 ℃该反应的平衡常数K=0.16 mol·L-1 |
| C.③中达到平衡时,A的转化率大于20% |
| D.5min末测得①中n(C)=0.050 mol,则0到5min内v(D)=0.02mol·L-1·min-1 |
更新时间:2020-05-09 11:30:27
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】碘在科研与生活中有重要应用。某兴趣小组用0.20mol/LKI、0.2%淀粉溶液、0.20mol/L(NH4)2S2O8、0.10mol/LNa2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知: +2I-=2SO
+2I-=2SO +I2(慢)
+I2(慢)
2 +I2=
+I2= (无色)+2I-(快)
(无色)+2I-(快)
结合表中数据判断下列说法错误的是
已知:
 +2I-=2SO
+2I-=2SO +I2(慢)
+I2(慢)2
 +I2=
+I2= (无色)+2I-(快)
(无色)+2I-(快)结合表中数据判断下列说法错误的是
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | |
| 试剂用量/(mL) | 0.20mol/L(NH4)2S2O8 | 10.0 | 5.0 | 2.5 | 10.0 | 10.0 |
| 0.20mol/LKI | 10.0 | 10.0 | 10.0 | 5.0 | 2.5 | |
| 0.10mol/LNa2S2O3 | 4.0 | 4.0 | 4.0 | 4.0 | 4.0 | |
| 0.2%淀粉溶液 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | |
| 蒸馏水 | 0.0 | a | 7.5 | b | 7.5 | |
| 显色时间△t/(s) | 35 | 51 | 123 | 56 | 107 | |
| A.a=5,b=5 |
B.实验I中,用Na2S2O3表示的反应速率为 mol/(L·s) mol/(L·s) |
| C.反应液初始浓度越大,反应时间越长,平均反应速率越小 |
D.为确保能观察到蓝色,需满足的关系为n( ):n( ):n( )<2 )<2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定条件下铁可以和 发生反应:
发生反应: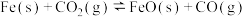 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和CO气体的浓度与时间的关系如图所示下列说法正确的是
气体和CO气体的浓度与时间的关系如图所示下列说法正确的是
 发生反应:
发生反应: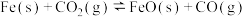 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和CO气体的浓度与时间的关系如图所示下列说法正确的是
气体和CO气体的浓度与时间的关系如图所示下列说法正确的是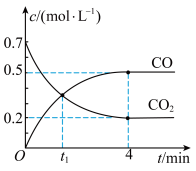
A.在4 min时 |
B. min时该化学反应达到平衡状态 min时该化学反应达到平衡状态 |
C.4 min内, 的转化率约为71.4% 的转化率约为71.4% |
D.4 min内,CO的平均反应速率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
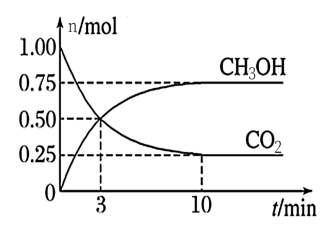
【推荐3】工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
 CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
| A.达到平衡时,H2的转化率为75% |
| B.3 min 时,CH3OH和CO2的浓度相等,达到了化学平衡状态 |
| C.反应进行到10 min后,向容器中再充入CO2,则CO2的转化率会增大 |
| D.反应开始到10 min,用CO2表示的反应速率为0.0375 mol·L-1·min-1 |
您最近一年使用:0次
【推荐1】相同温度下,容积相同的甲,乙两个恒容密闭容器均发生如下反应:N2+3H2 2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是
2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是
 2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是
2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是| 容器编号 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化/kJ | ||
| N2 | 3H2 | NH3 | ||
| 甲 | 1 | 3 | 0 | 放出热量:Q1 |
| 乙 | 0.9 | 2.7 | 0.2 | 放出热量:Q2 |
| A.Q2<Q1=92.4 | B.容器甲先达平衡 |
| C.两容器中反应的平衡常数相等 | D.达到平衡时NH3的体积分数:甲=乙 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】某温度下,在 的密闭容器中,加入
的密闭容器中,加入 和
和 发生反应:
发生反应: ,平衡时,
,平衡时, 、
、 、
、 的体积分数分别为
的体积分数分别为 、
、 、
、 。在此平衡体系中加入
。在此平衡体系中加入 ,再次达到平衡后,
,再次达到平衡后, 、
、 、
、 的体积分数不变。下列叙述
的体积分数不变。下列叙述不正确 的是
 的密闭容器中,加入
的密闭容器中,加入 和
和 发生反应:
发生反应: ,平衡时,
,平衡时, 、
、 、
、 的体积分数分别为
的体积分数分别为 、
、 、
、 。在此平衡体系中加入
。在此平衡体系中加入 ,再次达到平衡后,
,再次达到平衡后, 、
、 、
、 的体积分数不变。下列叙述
的体积分数不变。下列叙述A. | B.该温度下,该反应的平衡常数约为0.009 |
C. 与 与 的平衡转化率之比为 的平衡转化率之比为 | D.第二次平衡时, 的浓度为 的浓度为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】已知:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH=-41 kJ·mol-1,相同温度下,在容积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
CO2(g)+H2(g) ΔH=-41 kJ·mol-1,相同温度下,在容积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
下列说法中,正确的是
 CO2(g)+H2(g) ΔH=-41 kJ·mol-1,相同温度下,在容积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
CO2(g)+H2(g) ΔH=-41 kJ·mol-1,相同温度下,在容积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:| 容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系能量的变化 | |||
| CO | H2O | CO2 | H2 | ||
| ① | 1 | 1 | 0 | 0 | 放出热量:32.8 kJ |
| ② | 0 | 0 | 1 | 1 | 热量变化:Q kJ |
| A.容器①中,反应达平衡时,CO的转化率为80% |
| B.容器①中,CO的转化率等于容器②中CO2的转化率 |
| C.平衡时,两容器中CO2的浓度相等 |
| D.容器②中,反应达平衡过程中,体系吸收32.8 kJ的热量 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度下,在2L的恒容密闭容器中,加入4mol A和2mol B进行如下反应: 。反应t min后达到平衡,测得生成1.6mol C,且反应前后的压强之比为5∶4。下列说法不正确的是
。反应t min后达到平衡,测得生成1.6mol C,且反应前后的压强之比为5∶4。下列说法不正确的是
 。反应t min后达到平衡,测得生成1.6mol C,且反应前后的压强之比为5∶4。下列说法不正确的是
。反应t min后达到平衡,测得生成1.6mol C,且反应前后的压强之比为5∶4。下列说法不正确的是A.该反应的平衡常数表达式为 |
| B.平衡时,B的转化率为40% |
C. 时间内,以C表示的平均速率为 时间内,以C表示的平均速率为 |
| D.将容器体积由2L减小到1L,平衡向右移动 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】相同温度下,在3个均为1L的密闭容器中分别进行反应2X(g)+Y(g)⇌Z(g) △H,达到平衡时相关数据如表。下列说法不正确的是
| 容器 | 温度/K | 物质的起始浓度/mol⋅L−1 | 物质的平衡浓度/mol⋅L−1 | ||
| c(X) | c(Y) | c(Z) | c(Z) | ||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | a |
| Ⅲ | 500 | 0.20 | 0.10 | 0 | 0.025 |
| A.平衡时,X的转化率:Ⅱ>Ⅰ |
| B.平衡常数:K(Ⅱ)>K(Ⅰ) |
| C.达到平衡所需时间:Ⅲ<Ⅰ |
| D.反应的△H>0 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】向 的恒容密闭容器中充入
的恒容密闭容器中充入 ,
, 时发生反应2SO3(g)⇌2SO2(g)+O2(g),其中
时发生反应2SO3(g)⇌2SO2(g)+O2(g),其中 与
与 的物质的量随时间变化如图所示。下列说法正确的是
的物质的量随时间变化如图所示。下列说法正确的是

 的恒容密闭容器中充入
的恒容密闭容器中充入 ,
, 时发生反应2SO3(g)⇌2SO2(g)+O2(g),其中
时发生反应2SO3(g)⇌2SO2(g)+O2(g),其中 与
与 的物质的量随时间变化如图所示。下列说法正确的是
的物质的量随时间变化如图所示。下列说法正确的是
A. 点处存在 点处存在 | B.n(so2):n(o2):n(so3)=1:1:1时,反应达平衡 |
C.达到平衡时, 的浓度为 的浓度为 | D.在 点时, 点时, 的转化率约为 的转化率约为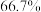 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】在容积为1L的恒容密闭容器中,发生反应A(g)+2B(g) C(g) ΔH<0,在三种不同温度下,不同的
C(g) ΔH<0,在三种不同温度下,不同的 (起始时,A的物质的量均为1mol)与A的平衡转化率的关系曲线如图所示。下列说法错误的是
(起始时,A的物质的量均为1mol)与A的平衡转化率的关系曲线如图所示。下列说法错误的是

 C(g) ΔH<0,在三种不同温度下,不同的
C(g) ΔH<0,在三种不同温度下,不同的 (起始时,A的物质的量均为1mol)与A的平衡转化率的关系曲线如图所示。下列说法错误的是
(起始时,A的物质的量均为1mol)与A的平衡转化率的关系曲线如图所示。下列说法错误的是
| A.Z曲线对应的温度最高 |
| B.a点时,该反应的平衡常数K=4 |
C.随着 增大,B的平衡转化率增大 增大,B的平衡转化率增大 |
| D.绝热条件下发生该反应,容器内的密度先增大后减小 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】常温下,向2L恒容密闭容器中充入0.80molA,发生反应:A(g) B(g)+C(g)△H=akJ/mol,一段时间后达到平衡。反应过程中测定的部分数据如下:
B(g)+C(g)△H=akJ/mol,一段时间后达到平衡。反应过程中测定的部分数据如下:
下列说法正确的是
 B(g)+C(g)△H=akJ/mol,一段时间后达到平衡。反应过程中测定的部分数据如下:
B(g)+C(g)△H=akJ/mol,一段时间后达到平衡。反应过程中测定的部分数据如下:| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(A)/mol | 0.80 | 0.60 | 0.48 | n2 | n3 |
| n(B)/mol | 0.00 | 0.20 | n1 | 0.40 | 0.40 |
| A.该反应在30min时,恰好达到平衡 |
B.反应在前20min内,平均速率为 (C)=0.008mol/(L·min) (C)=0.008mol/(L·min) |
| C.保持其他条件不变,升高温度,平衡时c(A)=0.16mol/L,则a<0 |
D.相同温度下,起始时向容器中充入0.10molA、0.10molB和0.30molC,达到平衡前的反应速率 逆> 逆> 正 正 |
您最近一年使用:0次



