20. 一水硫酸四氨合铜晶体[Cu(NH
3)
4SO
4·H
2O]常用作杀虫剂,媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。常温下该物质可溶于水,难溶于乙醇,在空气中不稳定,受热时易发生分解。某化学兴趣小组以Cu粉、3 mol·L
-1的硫酸、浓氨水、10% NaOH溶液、95%的乙醇溶液、0.500 mol·L
-1稀盐酸、0.500 mol·L
-1 的NaOH溶液来制备一水硫酸四氨合铜晶体并测定其纯度。
I.CuSO
4溶液的制取:
①实验室用铜与浓硫酸制备硫酸铜溶液时,往往会产生有污染的SO
2气体,随着硫酸浓度变小,反应会停止,使得硫酸利用率比较低。
②实际生产中往往将铜片在空气中加热,使其氧化生成CuO,再溶解在稀硫酸中即可得到硫酸铜溶液;这一过程缺点是铜片表面加热易被氧化,而包裹在里面的铜得不到氧化。
③所以工业上进行了改进,可以在浸入硫酸中的铜片表面不断通 O
2,并加热;也可以在硫酸和铜的混合容器中滴加 H
2O
2溶液。
④趁热过滤得蓝色溶液。
(1)某同学在上述实验制备硫酸铜溶液时铜有剩余,该同学将制得的CuSO
4溶液倒入另一蒸发皿中加热浓缩至有晶膜出现,冷却析出的晶体中含有白色粉末,试解释其原因
__________。
(2)若按③进行制备,请写出Cu在H
2O
2 作用下和稀硫酸反应的化学方程式
__________。
(3)H
2O
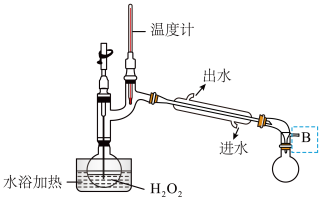
2溶液的浓度对铜片的溶解速率有影响。现通过下图将少量30%的H
2O
2溶液浓缩至40%,在B处应增加一个设备,该设备的作用是
_________________________;馏出物是
________________。
II.晶体的制备:
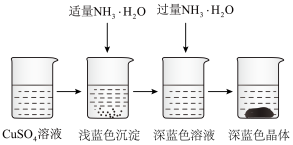
将上述制备的CuSO
4溶液按如图所示进行操作:硫酸铜溶液含有一定的硫酸,呈酸性,加入适量NH
3·H
2O调节溶液pH,产生浅蓝色沉淀,已知其成分为Cu
2(OH)
2SO
4,试写出生成此沉淀的离子反应方程式
_____________________________________________。
Ⅲ.产品纯度的测定:精确称取 m g晶体,加适量水溶解,注入图示的三颈瓶中,然后逐滴加入足量 NaOH 溶液, 通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用 V
1 mL 0.500 mol·L
-1 的盐酸标准溶液完全吸收。取下接收瓶,用 0.500 mol·L
-1 NaOH 标准溶液滴定过剩的 HCl(选用甲基橙作指示剂),到终点时消耗 V
2 mLNaOH溶液。

(1)玻璃管2的作用
________________。
(2)样品中产品纯度的表达式
________________。(不用化简)
(3)下列实验操作可能使氨含量测定结果偏低的原因是
_________________A.滴定时未用 NaOH 标准溶液润洗滴定管
B.滴定过程中选用酚酞作指示剂
C.读数时,滴定前平视,滴定后俯视
D.取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁
E.由于操作不规范,滴定前无气泡,滴定后滴定管中产生气泡