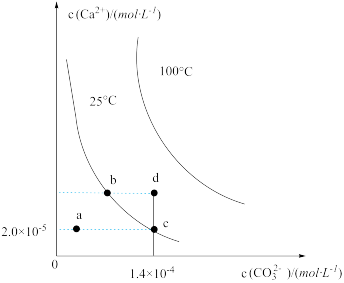
如图是碳酸钙(CaCO3)在25℃和100℃两种情况下,在水中的沉淀溶解平衡曲线。下列有关说法正确的是

A.CaCO3(s) Ca2+(aq)+CO32—(aq)ΔH<0 Ca2+(aq)+CO32—(aq)ΔH<0 |
| B.a、b、c、d四点对应的溶度积Ksp关系:d﹥b﹥c﹥a |
| C.25℃时,蒸发溶剂可能使溶液由a点变为曲线上b、c之间的某一点(不含b、c) |
| D.25℃时CaCO3的Ksp=2.8×10-9,d点无沉淀生成 |
更新时间:2020-05-10 11:59:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知溶液中存在平衡:Ca(OH)2(s) Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是
Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下,向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入Na2CO3溶液,其中固体质量增加
⑦向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
 Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是
Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下,向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入Na2CO3溶液,其中固体质量增加
⑦向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
| A.①⑥ | B.①⑥⑦ | C.②③④⑥ | D.①②⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知常温下Ksp(AgCl)=1.6×10﹣10,Ksp(AgI)=8.3×10﹣17,下列有关说法正确的是
| A.常温下,AgCl在纯水中的Ksp比在AgNO3溶液中的Ksp大 |
| B.向AgCl与AgI等体积混合的饱和溶液中加入足量浓AgNO3溶液,产生的AgCl沉淀的物质的量少于AgI |
| C.在AgCl的饱和溶液中通入HCl,有AgCl析出,且溶液中c(Ag+)=c(Cl﹣) |
D.向AgI与AgCl的悬浊液中加入几滴浓NaCl溶液, 不变 不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25 ℃时,在氢氧化镁悬浊液中存在沉淀溶解平衡:Mg(OH)2(s) Mg2+(aq)+2OH−(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20。下列说法错误的是
Mg2+(aq)+2OH−(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20。下列说法错误的是
 Mg2+(aq)+2OH−(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20。下列说法错误的是
Mg2+(aq)+2OH−(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20。下列说法错误的是| A.若向Mg(OH)2悬浊液中加入少量NH4Cl(s),c(Mg2+)会增大 |
| B.若向Mg(OH)2悬浊液中滴加CuSO4溶液,沉淀将由白色逐渐变为蓝色 |
| C.若向Mg(OH)2悬浊液中加入适量蒸馏水,Ksp保持不变,故上述平衡不发生移动 |
| D.若向Mg(OH)2悬浊液中加入少量Na2S(s),固体质量将增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
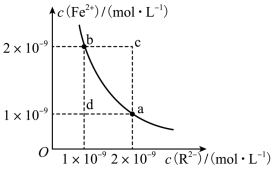
【推荐1】某温度下,难溶物FeR的水溶液中存在平衡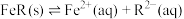 ,其沉淀溶解平衡曲线如图所示。下列说法正确的是
,其沉淀溶解平衡曲线如图所示。下列说法正确的是
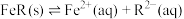 ,其沉淀溶解平衡曲线如图所示。下列说法正确的是
,其沉淀溶解平衡曲线如图所示。下列说法正确的是 
| A.可以通过升温实现由c点变到a点 | B.d点可能有沉淀生成 |
C.a点对应的 等于 等于 点对应的 点对应的 | D.该温度下,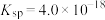 |
您最近一年使用:0次
【推荐2】25℃时, 和
和 的沉淀溶解平衡曲线如图(
的沉淀溶解平衡曲线如图( 代表
代表 或
或 )所示。下列说法
)所示。下列说法不正确 的是
 和
和 的沉淀溶解平衡曲线如图(
的沉淀溶解平衡曲线如图( 代表
代表 或
或 )所示。下列说法
)所示。下列说法
A.a点可表示 的饱和溶液 的饱和溶液 |
B.c点可表示 的过饱和溶液,达新平衡时可到达b点 的过饱和溶液,达新平衡时可到达b点 |
C.d点时溶液中存在 (忽略单位) (忽略单位) |
D.由图可知:同温下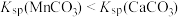 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:298K时,Ksp(MnS)=4.65×10-14,Ksp(MnCO3)=2.24×10-11。298K时,MnS、MnCO3在水中沉淀溶解平衡曲线如图所示。下列说法正确的是( )


| A.图象中e点处溶液c(Mn2+)≈5.0×10-6 |
| B.常温下,加水稀释X溶液可使d点转移到f点 |
| C.其他条件不变,加热含Y固体的Y溶液可使e点升到f点 |
D.在MnS和MnCO3饱和溶液中加少量MnCl2,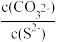 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:298K时,四种物质的溶度积如表所示。下列说法正确的是( )
| 化学式 | CH3COOAg | AgCl | Ag2CrO4 | Ag2S |
| Ksp | 2.3×10-3 | 1.56×10-10 | 1.12×10-12 | 6.3×10-50 |
| A.298K时,将0.001mol⋅L-1的AgNO3溶液逐滴滴入0.001mol⋅L-1的KCl和0.001mol⋅L-1的K2CrO4的混合液中,则先产生Ag2CrO4沉淀 |
| B.298K时,向2.0×10-4mol⋅L-1的K2CrO4溶液中加入等体积的2.0×10-4mol⋅L-1的AgNO3溶液,则有Ag2CrO4沉淀生成(忽略混合时溶液体积的变化) |
| C.298K时,向CH3COOAg悬浊液中加入盐酸,发生反应的离子方程式为CH3COOAg+H++Cl-⇌CH3COOH+AgCl |
D.已知: =0.65,298K时,四种物质的饱和溶液的物质的量浓度:c(CH3COOAg)>c(AgCl)>c(Ag2CrO4)>c(Ag2S) =0.65,298K时,四种物质的饱和溶液的物质的量浓度:c(CH3COOAg)>c(AgCl)>c(Ag2CrO4)>c(Ag2S) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验不能达到预期实验目的的是
| 序号 | 实验内容 | 实验目的 |
| A | 室温下,用pH计测定浓度为0.1 mol·L-1 Na2CO3溶液和0.1 mol·L-1CH3COONa溶液的pH | 比较H2CO3和CH3COOH的酸性强弱 |
| B | 向盛有1 mL AgNO3溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加NaI溶液,出现黄色沉淀 | 说明该温度下Ksp(AgCl)>Ksp(AgI) |
| C | 向AlCl3溶液中滴加饱和NaHCO3溶液,有白色沉淀和大量气体产生 | 验证两者都发生水解反应,且相互促进 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积、不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】自然界中重晶石矿(主要成分为BaSO4)和毒重石矿(主要成分为BaCO3)往往伴生,已知常温下Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.5×10-9。下列说法中错误的是
| A.自然界中若毒重石矿周围有可溶性硫酸盐,则BaCO3可能转化为BaSO4 |
| B.常温下硫酸钡的溶解度大约为2.33×10-4g |
C.含有重晶石矿和毒重石矿的地下水中CO 的浓度约为SO 的浓度约为SO 浓度的25倍 浓度的25倍 |
| D.分别用等体积的水和稀H2SO4洗涤BaSO4,稀H2SO4作洗涤剂时BaSO4损失更大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,Ksp[Fe(OH)3]=4.0×10-38,在pH=4的Fe(OH)3饱和溶液中,c(Fe3+)为
| A.1.0×10-8mol·L-1 |
| B.4.0×10-8mol·L-1 |
| C.1.0×10-26mol·L-1 |
| D.1.3×10-28mol·L-1 |
您最近一年使用:0次
【推荐3】 常用于制造分析试剂、荧光体、光导体材料、染料、涂料、颜料、玻璃、固化油等。以工业废渣锌灰(主要成分为Zn、ZnO,还含有Fe2O3、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
常用于制造分析试剂、荧光体、光导体材料、染料、涂料、颜料、玻璃、固化油等。以工业废渣锌灰(主要成分为Zn、ZnO,还含有Fe2O3、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
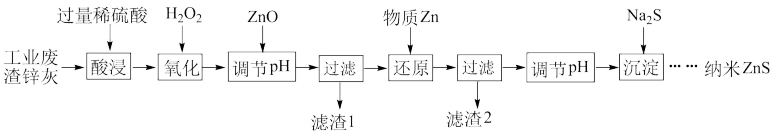
已知:常温下,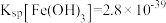 ;
;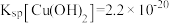 ;
;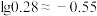 。离子浓度小于10-5时,可认为沉淀完全,下列说法正确的是
。离子浓度小于10-5时,可认为沉淀完全,下列说法正确的是
 常用于制造分析试剂、荧光体、光导体材料、染料、涂料、颜料、玻璃、固化油等。以工业废渣锌灰(主要成分为Zn、ZnO,还含有Fe2O3、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
常用于制造分析试剂、荧光体、光导体材料、染料、涂料、颜料、玻璃、固化油等。以工业废渣锌灰(主要成分为Zn、ZnO,还含有Fe2O3、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
已知:常温下,
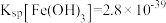 ;
;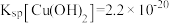 ;
;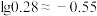 。离子浓度小于10-5时,可认为沉淀完全,下列说法正确的是
。离子浓度小于10-5时,可认为沉淀完全,下列说法正确的是A.常温下使Fe3+沉淀完全的最小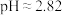 |
| B.“滤渣2”是Fe和Zn |
| C.第二次调节pH也可以用ZnO,但不能用Zn(OH)2、ZnCO3 |
D.沉淀过程中发生反应的离子方程式为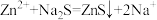 |
您最近一年使用:0次


 )>c(Cl-)
)>c(Cl-)

