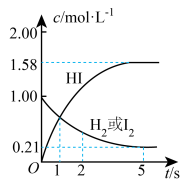
恒温恒容时,NO2和N2O4之间发生反应:N2O4(g)⇌2NO2(g),如图所示。
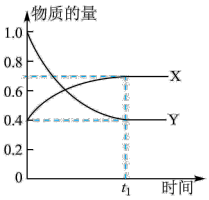
(1)曲线____ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若升高温度,则v(NO2)____ (填“增大”或“减小”)。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3 mol·L-1·min-1,乙中v(N2O4)=0.2 mol·L-1·min-1,则________ 中反应更快。

(1)曲线
(2)若升高温度,则v(NO2)
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3 mol·L-1·min-1,乙中v(N2O4)=0.2 mol·L-1·min-1,则
更新时间:2020-05-11 22:41:28
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:
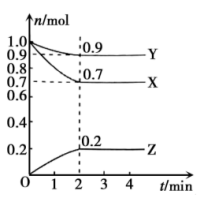
(1)写出该反应的化学方程式___________ 。
(2)反应开始至2min时用X的浓度变化表示的平均反应速率v(X)=___________ 。

(1)写出该反应的化学方程式
(2)反应开始至2min时用X的浓度变化表示的平均反应速率v(X)=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图1所示。根据图中数据,填写下列空白。
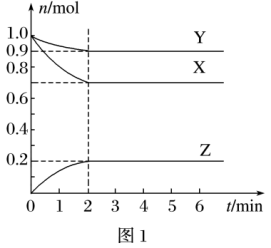
(1)该反应的化学方程式为_______ 。
(2)反应开始至2min,气体Z的平均反应速率v(Z)=_______ 。
II.将等物质的量的A和B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),5min后测得c(D)=1mol·L-1,c(A)∶c(B)=3:5,C的反应速率是0.3mol·L-1·min-1。
(3)A在5min末的浓度是_______ 。
(4)ν(B)=_______ 。
(5)x=_______ 。
(6)5min末A的转化率为_______ 。

(1)该反应的化学方程式为
(2)反应开始至2min,气体Z的平均反应速率v(Z)=
II.将等物质的量的A和B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),5min后测得c(D)=1mol·L-1,c(A)∶c(B)=3:5,C的反应速率是0.3mol·L-1·min-1。
(3)A在5min末的浓度是
(4)ν(B)=
(5)x=
(6)5min末A的转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】在一定体积的密闭容器中进行如下反应: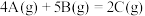
(1)开始时,A为 ,2s后,A为
,2s后,A为 。计算该反应的速率
。计算该反应的速率_______ 。
(2)请用适当的理论模型解释。
①温度升高,反应速率提高_______ 。
②使用催化剂,反应速率提高_______ 。
③增大A的浓度,反应速率提高_______ 。
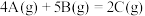
(1)开始时,A为
 ,2s后,A为
,2s后,A为 。计算该反应的速率
。计算该反应的速率(2)请用适当的理论模型解释。
①温度升高,反应速率提高
②使用催化剂,反应速率提高
③增大A的浓度,反应速率提高
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】CO2催化加氢合成二甲醚(CH3OCH3)是一种CO2转化方法,反应原理为:
2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)
(1)加快该反应速率的措施有___________________ (填两条)。
(2)能证明上述反应达到平衡状态是____ (填标号)。
A.v正(CO2)=3v逆(H2) B.CH3OCH3的浓度不再改变
C.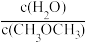 不再变化 D.混合气体的平均相对分子质量不再改变
不再变化 D.混合气体的平均相对分子质量不再改变
(3)某温度下,在体积为2 L的密闭容器中加入2 mol CO2与5 mol H2发生催化反应,经过10 min后CO2的浓度不再变化,测得其体积分数为20%。试计算:
①在0~10 min时段,用CH3OCH3表示的平均反应速率____ 。
②起始状态与平衡状态容器内的压强之比____ 。(无计算过程不给分)
2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)
(1)加快该反应速率的措施有
(2)能证明上述反应达到平衡状态是
A.v正(CO2)=3v逆(H2) B.CH3OCH3的浓度不再改变
C.
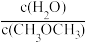 不再变化 D.混合气体的平均相对分子质量不再改变
不再变化 D.混合气体的平均相对分子质量不再改变(3)某温度下,在体积为2 L的密闭容器中加入2 mol CO2与5 mol H2发生催化反应,经过10 min后CO2的浓度不再变化,测得其体积分数为20%。试计算:
①在0~10 min时段,用CH3OCH3表示的平均反应速率
②起始状态与平衡状态容器内的压强之比
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(Ⅰ)某化学反应A B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
(1)该反应属于__________ 反应(填“可逆”或“不可逆”)。
(2)在实验1、2中,有一个实验使用了催化剂。请你利用表中数据判断实验___ (填1或2)使用了催化剂,理由是_______________ 。
(3)该实验表明,影响化学反应速率的因素还有__________ 。
(Ⅱ)下图是1molNO2和1molCO反应生成1molCO2和1molNO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:__________________ 。
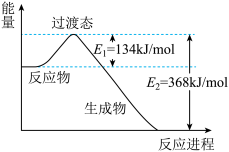
该反应的活化能等于____________________
 B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。
B+C在三种不同条件下进行,B、C的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示,表中温度为摄氏度(℃)。| 实验 序号 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)该反应属于
(2)在实验1、2中,有一个实验使用了催化剂。请你利用表中数据判断实验
(3)该实验表明,影响化学反应速率的因素还有
(Ⅱ)下图是1molNO2和1molCO反应生成1molCO2和1molNO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:

该反应的活化能等于
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】在催化剂存在下, 和
和 发生催化重整反应
发生催化重整反应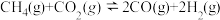 ,既能保护环境,又能利用资源。一定温度下,将
,既能保护环境,又能利用资源。一定温度下,将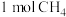 和
和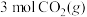 通入体积为10L的恒容密闭容器里,在一定条件下发生上述反应。请回答下列问题:
通入体积为10L的恒容密闭容器里,在一定条件下发生上述反应。请回答下列问题:
(1) 的空间结构为
的空间结构为_______ ,标准状况下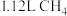 所含电子的数目为
所含电子的数目为_______ 。
(2)下列说法可以判定反应达到化学平衡状态的是_______ (填标号)。
A.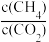 不再改变
不再改变
B.混合气体的密度不再改变
C.相同时间内,断裂 键的数目与生成
键的数目与生成 键的数目比为2∶1
键的数目比为2∶1
D.气体的平均相对分子质量不再改变
(3)若上述反应 后达到化学平衡,容器压强变为起始压强的1.25倍,则
后达到化学平衡,容器压强变为起始压强的1.25倍,则 内,
内, 的平衡转化率为
的平衡转化率为_______ ,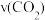
_______  ,
,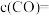
_______  。
。
 和
和 发生催化重整反应
发生催化重整反应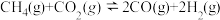 ,既能保护环境,又能利用资源。一定温度下,将
,既能保护环境,又能利用资源。一定温度下,将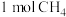 和
和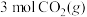 通入体积为10L的恒容密闭容器里,在一定条件下发生上述反应。请回答下列问题:
通入体积为10L的恒容密闭容器里,在一定条件下发生上述反应。请回答下列问题:(1)
 的空间结构为
的空间结构为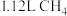 所含电子的数目为
所含电子的数目为(2)下列说法可以判定反应达到化学平衡状态的是
A.
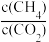 不再改变
不再改变B.混合气体的密度不再改变
C.相同时间内,断裂
 键的数目与生成
键的数目与生成 键的数目比为2∶1
键的数目比为2∶1D.气体的平均相对分子质量不再改变
(3)若上述反应
 后达到化学平衡,容器压强变为起始压强的1.25倍,则
后达到化学平衡,容器压强变为起始压强的1.25倍,则 内,
内, 的平衡转化率为
的平衡转化率为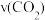
 ,
,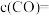
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】I.某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。

请回答下列问题:
(1)该反应的化学反应方程式为_______ 。
(2)1min时,Y的正反应速率_______ Y的逆反应速率(填“>”“<”或“=”)
(3)反应从开始至2min,用X的浓度变化表示的平均反应速率为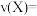
_______ 。
II.油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,通常将其回收生产硫单质(S2)。目前较为普遍的方法是克劳斯工艺和高温热分解H2S,克劳斯工艺的原理是利用以下两步反应生产单质硫:
①
②
请回答下列问题:
(4)下列措施可以加快反应②的速率的是_______。
(5)高温热分解H2S的化学反应方程式是_______ 。
(6)在1470K、100kPa反应条件下,在一容积为2L的恒容容器中充入1molH2S进行高温热分解反应,反应5分钟后达到平衡,平衡时混合气体中H2S与H2的物质的量相等,H2S平衡转化率为_______ 。

请回答下列问题:
(1)该反应的化学反应方程式为
(2)1min时,Y的正反应速率
(3)反应从开始至2min,用X的浓度变化表示的平均反应速率为
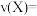
II.油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,通常将其回收生产硫单质(S2)。目前较为普遍的方法是克劳斯工艺和高温热分解H2S,克劳斯工艺的原理是利用以下两步反应生产单质硫:
①

②

请回答下列问题:
(4)下列措施可以加快反应②的速率的是_______。
| A.升高温度 | B.保持容积不变,充入N2使体系压强增大 |
| C.及时从体系中分离出S2(g) | D.加入合适的催化剂 |
(6)在1470K、100kPa反应条件下,在一容积为2L的恒容容器中充入1molH2S进行高温热分解反应,反应5分钟后达到平衡,平衡时混合气体中H2S与H2的物质的量相等,H2S平衡转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】Ⅰ.在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)800℃,反应达到平衡时,NO的转化率是___ 。
(2)用O2表示从0~2s内该反应的平均速率v=___ 。
Ⅱ.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
(1)下列不能判断该分解反应已经达到化学平衡状态的是___ (填选项)。
A.2v生(NH3)=v耗(CO2)
B.密闭容器中氨气的物质的量不变
C.容器中CO2与NH3的物质的量之比保持不变
D.密闭容器中总压强保持不变
E.形成6个N—H键的同时有2C=O键断裂
(2)能使该反应的反应速率增大的是___ (选项)。
A.及时分离出CO2气体 B.适当升高温度
C.加入少量NH2COONH4(s) D.选择高效催化剂
(3)如图所示,上述反应中断开反应物中化学键吸收的能量___ (填“大于”“等于”或“小于”)形成生成物中化学键放出的能量。

 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)用O2表示从0~2s内该反应的平均速率v=
Ⅱ.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)
 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。(1)下列不能判断该分解反应已经达到化学平衡状态的是
A.2v生(NH3)=v耗(CO2)
B.密闭容器中氨气的物质的量不变
C.容器中CO2与NH3的物质的量之比保持不变
D.密闭容器中总压强保持不变
E.形成6个N—H键的同时有2C=O键断裂
(2)能使该反应的反应速率增大的是
A.及时分离出CO2气体 B.适当升高温度
C.加入少量NH2COONH4(s) D.选择高效催化剂
(3)如图所示,上述反应中断开反应物中化学键吸收的能量

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】一定温度下,向一体积为10L的恒容密闭容器中充入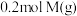 和
和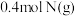 ,发生反应:
,发生反应: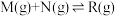 。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。回答下列问题:
。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。回答下列问题:

(1)实验a从反应开始至达到平衡时:
①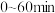 内,
内,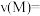
_______  。
。
②R的物质的量浓度为_______  。
。
③该反应的平衡常数
_______ 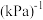 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
④反应达到平衡后,保持其他条件不变,向该容器中再充入0.05molM和0.15molR,此时v(正)_______ (填“>”、“<”或“=”)v(逆),判断的理由是_______ (写出计算过程)。
(2)若起始时只发生某一条件的改变,实验b改变的条件可能是_______ 。
(3)图中a、b、c三组实验从开始反应至达到平衡时的反应速率v(R)由大到小的顺序为_______ (填实验标号)。
(4)对于反应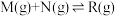 ,下列叙述能表明该反应已达到平衡状态的是_______(填标号)。
,下列叙述能表明该反应已达到平衡状态的是_______(填标号)。
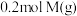 和
和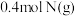 ,发生反应:
,发生反应: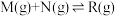 。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。回答下列问题:
。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。回答下列问题:
(1)实验a从反应开始至达到平衡时:
①
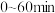 内,
内,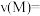
 。
。②R的物质的量浓度为
 。
。③该反应的平衡常数

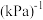 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。④反应达到平衡后,保持其他条件不变,向该容器中再充入0.05molM和0.15molR,此时v(正)
(2)若起始时只发生某一条件的改变,实验b改变的条件可能是
(3)图中a、b、c三组实验从开始反应至达到平衡时的反应速率v(R)由大到小的顺序为
(4)对于反应
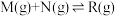 ,下列叙述能表明该反应已达到平衡状态的是_______(填标号)。
,下列叙述能表明该反应已达到平衡状态的是_______(填标号)。| A.混合气体的密度不随时间改变 |
| B.N的物质的量分数不随时间改变 |
| C.单位时间内生成1molN的同时消耗1molR |
| D.混合气体的平均相对分子质量不随时间改变 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在100℃时,将0.1mol的四氧化二氮气体充入1 L抽空的密闭容器中,发生反应,隔一定时间对该容器内的物质进行分析,得到如下数据:
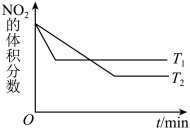
(1)该反应的化学方程式为______________________ ,表中c2_____ c3_____ a______ b(选填“>”、“<”、“==”)。
(2)20 s时四氧化二氮的浓度c1=____________ mol·l—1依据图象可以判断该反应的 ΔH___ 0(填“>”或“<”)
| 浓度 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol·L—1 | 0.1 | c1 | 0.05 | c3 | a | b |
| c(NO2)/mol·L—1 | 0 | 0.06 | c2 | 0.12 | 0.12 | 0.12 |

(1)该反应的化学方程式为
(2)20 s时四氧化二氮的浓度c1=
您最近一年使用:0次

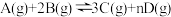 ,开始时A为
,开始时A为 ,B为
,B为 ,
, 末反应达到化学平衡,此时测得C的物质的量为
末反应达到化学平衡,此时测得C的物质的量为 ,用D表示的化学反应速率
,用D表示的化学反应速率 为
为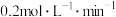 。计算:
。计算: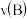 为
为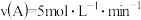
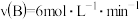

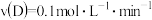
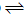 2HI(g)
2HI(g)