已知氯化铝的熔点为190℃(2.202×l05Pa),但它在180℃即开始升华。
(1)氯化铝是____________ 。(填“离子化合物”或“共价化合物”)
(2)在500K和1.01×105Pa时,它的蒸气密度(换算为标准状况时)为11.92g·L-1,试确定氯化铝在蒸气状态时的化学式为____________ 。
(3)无水氯化铝在空气中强烈的“发烟”,其原因是__________ 。
(1)氯化铝是
(2)在500K和1.01×105Pa时,它的蒸气密度(换算为标准状况时)为11.92g·L-1,试确定氯化铝在蒸气状态时的化学式为
(3)无水氯化铝在空气中强烈的“发烟”,其原因是
更新时间:2020-04-28 10:25:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】30克甲烷和乙烯的混合气体,在标准状况下33.6升。求:
(1)甲烷的质量_______
(2)甲烷和乙烯的体积比_______
(1)甲烷的质量
(2)甲烷和乙烯的体积比
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有21.6g由CO和CO2组成的混合气体,在标准状况下其体积为13.44 L。回答下列问题:
(1)该混合气体中CO与CO2的分子数之比________________ ;
(2)混合气体中氧原子的物质的量为______________________ ;
(3)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。
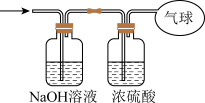
① 气球中收集到的气体的摩尔质量为______ ;
② 气球中收集到的气体中,电子总数为___ (用NA表示阿伏加德罗常数的值)。
③ 气球的体积为___________________ L。
(1)该混合气体中CO与CO2的分子数之比
(2)混合气体中氧原子的物质的量为
(3)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。

① 气球中收集到的气体的摩尔质量为
② 气球中收集到的气体中,电子总数为
③ 气球的体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.已知1mol不同气体在不同条件下的体积:
(1)从表中分析得出的结论:
①1mol任何气体,在标准状况下的体积都约为_______ 。
②1mol不同的气体,在不同的条件下,体积_______ (填序号)。
A.一定相等 B.一定不相等 C.不一定相等
(2)理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是①_______ ,②_______ 。
(3)应用:在标准状况下,4g氧气的体积是_______ ;0℃,202kPa时,4g氧气的体积是_______ 。
Ⅱ.在标准状况下15gCO与CO2的混合气体,体积为11.2L。则:
(4)混合气体的密度是_______ g/L。(取小数点后两位)
(5)CO2和CO的体积之比是_______ 。
(6)混合气体中所含碳原子的物质的量是_______ 。
| 化学式 | 条件 | 1mol气体的体积/L |
| H2 | 0℃,101kPa | 22.4 |
| O2 | 22.4 | |
| CO | 22.4 | |
| H2 | 0℃,202kPa | 11.2 |
| CO2 | 11.2 | |
| N2 | 11.2 | |
| NH3 | 273℃,202kPa | 22.4 |
①1mol任何气体,在标准状况下的体积都约为
②1mol不同的气体,在不同的条件下,体积
A.一定相等 B.一定不相等 C.不一定相等
(2)理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是①
(3)应用:在标准状况下,4g氧气的体积是
Ⅱ.在标准状况下15gCO与CO2的混合气体,体积为11.2L。则:
(4)混合气体的密度是
(5)CO2和CO的体积之比是
(6)混合气体中所含碳原子的物质的量是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上制备丙烯腈(CH2=CHC≡N)的绿色工艺有乙炔法。
乙炔法: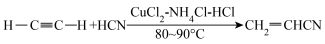
(1)下列说法正确的是____________ (不定项选择):
a. NH4+空间构型呈正四面体
b. CH2=CHCN分子中只有碳、氢原子位于同一平面
c. C2H2、HCN分子中所有原子均位于同一直线
d. NH3极易溶于H2O,主要是因为它们都是极性分子
(2)与NH3互为等电子体的阳离子为______________ (写化学式)。
(3)1mol丙烯腈分子中含有 键的数目为
键的数目为__________________ 。
(4)铜能与浓盐酸缓慢发生置换反应产生氢气,有配合物H[CuCl2]生成。该反应的化学方程式为____________________ 。
乙炔法:
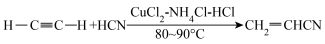
(1)下列说法正确的是
a. NH4+空间构型呈正四面体
b. CH2=CHCN分子中只有碳、氢原子位于同一平面
c. C2H2、HCN分子中所有原子均位于同一直线
d. NH3极易溶于H2O,主要是因为它们都是极性分子
(2)与NH3互为等电子体的阳离子为
(3)1mol丙烯腈分子中含有
 键的数目为
键的数目为(4)铜能与浓盐酸缓慢发生置换反应产生氢气,有配合物H[CuCl2]生成。该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)溴的基态原子的价电子排布图为___________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是____________。
(3)请根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是___________。
(4)已知高碘酸有两种形式,化学式分别为H5IO6( )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4。(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4。(填“>”、“<”或“=”)
(5)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大,这是由于溶液中发生下列反应:I-+I2
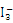 。
。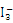 的中心原子周围的σ键电子对对数为__________,孤电子对对数为_________。
的中心原子周围的σ键电子对对数为__________,孤电子对对数为_________。
(6)写出一个ClO2-的等电子体:_________________。
(1)溴的基态原子的价电子排布图为___________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是____________。
(3)请根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是___________。
| 元素名称 | 氟 | 氧 | 溴 | 碘 | 铍 |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
(4)已知高碘酸有两种形式,化学式分别为H5IO6(
 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4。(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6_____HIO4。(填“>”、“<”或“=”)(5)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大,这是由于溶液中发生下列反应:I-+I2

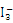 。
。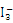 的中心原子周围的σ键电子对对数为__________,孤电子对对数为_________。
的中心原子周围的σ键电子对对数为__________,孤电子对对数为_________。(6)写出一个ClO2-的等电子体:_________________。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】砷化镓(GaAs)是优良的半导体材料或用于制作微型激光器或太阳能电池的材料等。部分元素在周期表中位置如下:
回答下列问题:
(1)六种元素中,非金属性最强的元素是:________ .写出As原子的最外层的电子排布式_________ ,As原子核外有_____ 个未成对电子。
(2)根据元素周期律,可判断原子半径Ga_____ As。(选填“>”、 “<”或“=”)。写出铝的最高价氧化物对应水化物的电离方程式:________________
(3)NH3 的分子构型是_______ 。GaF3的熔点高于1000°C,GaCl3的熔点为77.9°C,可能的原因是_______ .写出C2H2的电子式为:_________
(4)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因___________
| A1 | Si | P |
| Ga | Ge | As |
回答下列问题:
(1)六种元素中,非金属性最强的元素是:
(2)根据元素周期律,可判断原子半径Ga
(3)NH3 的分子构型是
(4)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/°C | -49.5 | 26 | 146 |
| 沸点/°C | 83.1 | 186 | 约400 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在下列化合物中:H2O2、Na2O、I2、NaCl、CO2、NH4Cl、Na2O2,用化学式回答下列问题:
①只由非金属组成的离子化合物是_________________ ;
②只有极性共价键的共价化合物是_________________ ;
③只含有非极性共价键的是_____________________ ;
④既有离子键又有非极性键的化合物是________________________ 。
①只由非金属组成的离子化合物是
②只有极性共价键的共价化合物是
③只含有非极性共价键的是
④既有离子键又有非极性键的化合物是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】下面是A~G七种元素的电子排布
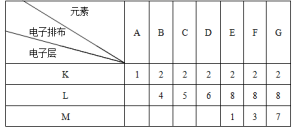
试由上述元素构成的物质的化学式回答:
(1)写出四种常见的由非极性键形成的双原子分子_____ ,
(2)写出三种由极性键形成的双原子分子___________ ,
(3)写出由极性键构成的直线形的三原子分子__ ,
(4)写出由三原子以极性键构成的空间构型为V形的三原子分子__ ,其电子式为___ ,
(5)写出一种由三个原子组成的既含离子键又含共价键的化合物___ ,其电子式为__________ 。
(6)写出一种既含离子键又含非极性键的化合物_____ ,其电子式为______ 。

试由上述元素构成的物质的化学式回答:
(1)写出四种常见的由非极性键形成的双原子分子
(2)写出三种由极性键形成的双原子分子
(3)写出由极性键构成的直线形的三原子分子
(4)写出由三原子以极性键构成的空间构型为V形的三原子分子
(5)写出一种由三个原子组成的既含离子键又含共价键的化合物
(6)写出一种既含离子键又含非极性键的化合物
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答下列问题:
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是______________ 。
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S。只由离子键构成的物质是_________ ;只由极性共价键构成的物质是_____ ;由极性键和非极性键构成的物质是_______ ;由离子键和极性键构成的物质是_______ 。(填序号)。
(3)写出下列物质的电子式:CaF2:______________ CO2:______________ NH4Cl:________________ 。
(4) 用电子式表示下列化合物的形成过程:H2S:__________________________________ ;MgCl2:_____________________________ 。
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S。只由离子键构成的物质是
(3)写出下列物质的电子式:CaF2:
(4) 用电子式表示下列化合物的形成过程:H2S:
您最近半年使用:0次



