室温下,向25.00 mL 0.1000 mol∙L−1氨水中滴加0.1000 mol∙L−1盐酸,溶液的pH随盐酸体积的变化如图。下列说法不正确的是( )
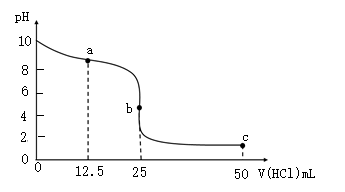

| A.如选甲基橙为指示剂,终点的判断为溶液颜色由黄色恰好变为橙色且半分钟不变色 |
| B.a→b,水的电离程度逐渐增大 |
C.a点溶液中, c(H+) c(H+) |
D.c点溶液中,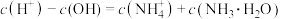 |
更新时间:2020-06-18 16:35:16
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】常温下,下列各溶液中水的电离程度最大的是
| A.pH=1的硫酸溶液 | B.1 mol/L氯化钠溶液 |
| C.0.01mol/L的烧碱溶液 | D.c(H+ )=10-2 mol/L的硫酸氢钠溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知实验室常用NaCl饱和溶液洗去Cl2中的HCl并减少Cl2的损失。将氯气通入纯水中时存在的平衡有
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】设 为阿伏加德罗常数值。下列有关叙述正确的是
为阿伏加德罗常数值。下列有关叙述正确的是
 为阿伏加德罗常数值。下列有关叙述正确的是
为阿伏加德罗常数值。下列有关叙述正确的是A. , , 的 的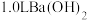 溶液中含有 溶液中含有 的数目为 的数目为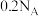 |
B. 与 与 反应生成的 反应生成的 分子数为 分子数为 |
C.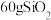 晶体中 晶体中 键数目为 键数目为 |
D.标准状况下,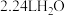 含有的共价键数为 含有的共价键数为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关电解质溶液的说法正确的是
| A.将Ca(ClO)2和Na2SO3溶液蒸干均得不到原溶质 |
| B.保存FeCl2溶液时,在溶液中放少量铁粉,以防止Fe2+水解 |
| C.室温下,向0.2 mol/L的CH3COOH溶液中加入少量水溶液呈碱性的物质,CH3COOH的电离程度一定增大 |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同。 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】其它条件不变,增大反应体系的压强,下列数据会明显增大的是( )
| A.二氧化硫与氧气反应生成三氧化硫气体的化学反应速率v |
| B.醋酸的电离度α |
| C.合成氨的化学平衡常数K |
| D.水的离子积常数Kw |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】某学生用已知物质的量浓度的NaOH溶液来测定未知物质的量浓度的H2C2O4溶液,下列说法正确的是( )
| A.碱式滴定管旋塞处应抹上少许凡士林,可防止漏液 |
| B.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移 |
| C.滴定时,通常用左手控制玻璃珠,使液体流速先快后慢,右手同一方向摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化 |
| D.可选择甲基橙作指示剂 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列各组离子在给定溶液中一定能大量共存的是
A.在0.1mol·L−1氨水中: 、 、 、 、 、 、 |
B.在0.1mol·L−1氯化钠溶液中: 、 、 、 、 、 、 |
C.在0.1mol·L−1醋酸溶液中: 、 、 、 、 、 、 |
D.在能使甲基橙显黄色的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
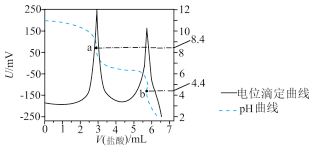
【推荐1】电位滴定法是根据滴定过程中被测离子浓度发生突跃,指示电极电位也产生突跃,从而确定滴定终点的一种滴定分析方法。常温下,利用盐酸滴定一定物质的量浓度的碳酸钠溶液,其电位滴定曲线与pH曲线如图所示(已知:碳酸的电离常数 )。下列说法不正确的是
)。下列说法不正确的是
 )。下列说法不正确的是
)。下列说法不正确的是
| A.该实验中,需先后用酚酞和甲基橙作指示剂 |
B.a点: |
| C.水的电离程度:a点>b点 |
D.b点: 比值为 比值为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列与滴定实验有关的说法中正确的是( )
| A.用NaOH滴定盐酸时,只能用酚酞作指示剂 |
| B.锥形瓶用蒸馏水洗干净后,直接加入一定体积的待测液,进行中和滴定 |
| C.用滴定管准确量取20.0mL盐酸 |
| D.用NaOH滴定盐酸时,若滴定结束时俯视刻度,会导致测定结果偏高 |
您最近一年使用:0次



 的物质的量一样多
的物质的量一样多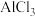 溶液能到得纯净的无水氯化铝
溶液能到得纯净的无水氯化铝

